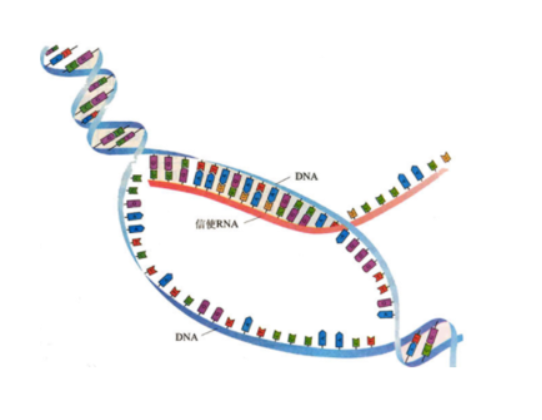
RNA是以DNA的(de)一條鏈爲模闆,以堿基互補配對(duì)原則,轉錄而形成的(de)一條單鏈,主要功能是實現遺傳信息在蛋白質上的(de)表達,是遺傳信息傳遞過程中的(de)橋梁。mRNA是基因(DNA)轉錄後的(de)産物(wù),有基因(DNA)不一定能轉錄,相同的(de)基因在不同的(de)狀況下(xià)轉錄得(de)到mRNA的(de)量也(yě)不一樣。所以檢測mRNA,可(kě)以在一定程度上反應該基因的(de)表達情況。
RNA的(de)提取便是我們研究基因表達和(hé)調控的(de)第一步,也(yě)是非常關鍵的(de)一步。得(de)到高(gāo)質量的(de)RNA對(duì)于後續很多(duō)實驗的(de)結果十分(fēn)重要,例如RT-qPCR、實時(shí)熒光(guāng)定量PCR、northernblot等。目前最常用(yòng)的(de)RNA提取方法是Trizol法,Trizol 試劑是由苯酚和(hé)異硫氰酸胍配制而成的(de)快(kuài)速抽提總RNA的(de)試劑。在勻漿和(hé)裂解樣品的(de)過程中,Trizol 試劑能夠保持RNA的(de)完整性,同時(shí)能破碎細胞、降解細胞其它成分(fēn)。在氯仿抽提、離心分(fēn)離後,RNA處于水(shuǐ)相中,将水(shuǐ)相轉管後用(yòng)異丙醇沉澱RNA。将組織在液氮中磨碎,每50-100mg組織加入1ml TRIzol,用(yòng)勻漿儀進行勻漿處理(lǐ)。樣品體積不應超過TRIzol體積10%。如果是培養細胞,則直接在培養皿中加入TRIzol裂解細胞,每10cm2面積(即3.5cm直徑的(de)培養闆)加1ml,用(yòng)移液器吸打幾次。将樣品在室溫(15-30℃)放置5分(fēn)鐘(zhōng),使核酸-蛋白複合物(wù)完全分(fēn)離。1 ml Trizol加入200ul預冷(lěng)的(de)氯仿,上下(xià)振蕩15s,室溫孵育5min。4℃,12000 g,離心15 min。分(fēn)離得(de)到三層,下(xià)層紅色的(de)酚-氯仿相、中間相以及上層無色水(shuǐ)相,RNA存在于水(shuǐ)相。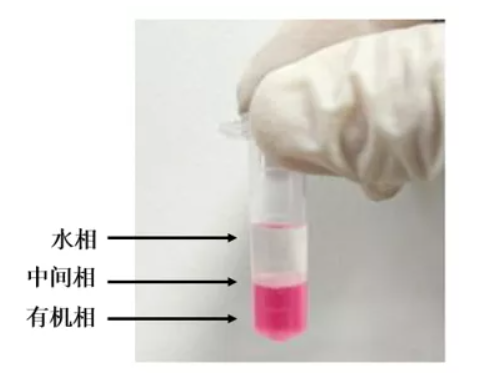
轉移約400~500ul水(shuǐ)相至新的(de)離心管,加入等體積預冷(lěng)的(de)異丙醇,上下(xià)輕慢(màn)的(de)混勻,室溫靜置10分(fēn)鐘(zhōng)後,4℃,12000g離心10min,棄上清。加入1ml預冷(lěng)的(de)75%乙醇,輕輕将整塊沉澱吹起懸浮, 4℃,7500 g,離心5 min。此時(shí),試管底部可(kě)見少量白色沉澱,盡量吸盡上清,室溫幹燥3-5min,待沉澱周圍無明(míng)顯殘留液體時(shí),視沉澱大(dà)小加入30-50ul RNase free水(shuǐ),充分(fēn)溶解沉澱,保存于-80℃。以無RNase水(shuǐ)作空白對(duì)照(zhào),測OD260/280值。1 OD=40μg RNA。OD260/280值在1.8-2.0視爲純度很高(gāo)。一般濃度在1000ng/ml較準。濃度太高(gāo)要稀釋以後再測定。甲醛變性瓊脂糖電泳,确定抽提RNA完整性和(hé)DNA污染情況。若RNA質量較好,可(kě)見18S和(hé)28S兩條明(míng)顯的(de)RNA條帶,且28S條帶亮度更高(gāo),最理(lǐ)想的(de)是28S亮度爲18S的(de)2倍。
1.最好使用(yòng)新鮮組織,或者-80℃(液氮)保存半年内的(de)組織,避免RNA降解影(yǐng)響RNA提取的(de)效果。2.提取過程盡量在冰上操作,低溫離心,防止在操作過程中RNA降解。3.所用(yòng)器材均需經過DEPC浸泡,高(gāo)壓滅菌後才能使用(yòng),所有試劑均需保證無RNA酶污染。4.在吸取水(shuǐ)相時(shí)需注意少吸、輕吸,不能吸到中間相,避免中間相中的(de)蛋白和(hé)基因組DNA造成污染和(hé)RNA降解。
返回列表





