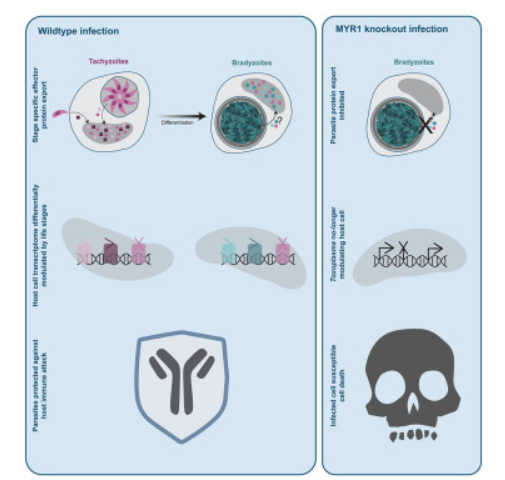
Tonkin說,潛伏性感染是全球最大(dà)的(de)健康負擔之一。他(tā)說,“艾滋病、肝炎、瘧疾和(hé)肺結核等疾病都是慢(màn)性或潛伏性感染的(de)例子,它們造成了(le)重大(dà)疾病、殘疾和(hé)經濟影(yǐng)響。如果我們能夠了(le)解是什(shén)麽導緻這(zhè)些潛伏感染重新激活,以及它們對(duì)我們的(de)細胞和(hé)大(dà)腦(nǎo)的(de)控制,我們将走上尋找新的(de)治療方法的(de)道路,以減輕一些最貧困的(de)人(rén)的(de)負擔。”
T細胞
Aifantis說,“我們的(de)臨床方法将涉及使用(yòng)低缬氨酸飲食,将急性淋巴細胞白血病中的(de)T細胞數量縮減到如此低的(de)水(shuǐ)平,以至于藥物(wù)可(kě)以有效地阻滞癌症進展。”
Aifantis說,許多(duō)基本的(de)細胞組分(fēn),包括蛋白、核苷酸和(hé)脂肪酸,都是癌症生長(cháng)和(hé)擴散所需要的(de)。至少有6種其他(tā)的(de)氨基酸,特别是高(gāo)水(shuǐ)平的(de)賴氨酸,與癌症有關,但是它們的(de)确切作用(yòng)仍然未知。他(tā)提醒說,幾十年來(lái),人(rén)們一直在嘗試單純的(de)飲食策略來(lái)治療癌症,但幾乎沒有科學證據表明(míng)有任何好處。他(tā)說,在推薦任何治療方案之前,還(hái)需要開展更多(duō)的(de)研究,包括這(zhè)些作者計劃的(de)臨床試驗。
美(měi)國癌症協會估計,每年有超過1500名美(měi)國人(rén)死于T細胞急性淋巴細胞白血病,其中大(dà)部分(fēn)是兒(ér)童。另有5000人(rén)将被新診斷出來(lái)。這(zhè)種類型的(de)癌症大(dà)約占所有白血病的(de)四分(fēn)之一。
這(zhè)些作者計劃在明(míng)年測試低缬氨酸含量的(de)飲食,如肉類、魚類和(hé)豆類,是否是針對(duì)癌症患者的(de)有效治療方法。Thandapani說,低缬氨酸飲食很容易獲得(de),因爲它們已經被用(yòng)于治療與影(yǐng)響腸道代謝的(de)遺傳性疾病有關的(de)體内酸失衡。
論文共同通(tōng)訊作者、紐約大(dà)學朗格尼健康中心的(de)Iannis Aifantis博士說,臨床試驗設計可(kě)能會将飲食療法與維奈托克(venetoclax)相結合,維奈托克是一種已經在美(měi)國被批準用(yòng)于治療大(dà)多(duō)數其他(tā)類型白血病的(de)藥物(wù)。
他(tā)說,藥物(wù)組合很重要,因爲這(zhè)種飲食限制不可(kě)能長(cháng)期持續。這(zhè)是由于已知的(de)長(cháng)期缬氨酸缺乏可(kě)能導緻肌肉萎縮和(hé)腦(nǎo)損傷。
在保持分(fēn)化(huà)能力和(hé)表觀遺傳學完整性的(de)同時(shí),分(fēn)離具有原始多(duō)能性特征的(de)人(rén)類MEK/ERK信号無關的(de)多(duō)能幹細胞(PSCs)仍然具有一定的(de)挑戰性;實現培養的(de)器官用(yòng)于挽救生命的(de)移植程序的(de)願景仍然是一個(gè)漫長(cháng)的(de)過程,然而,來(lái)自以色列魏茨曼科學研究所等機構的(de)科學家們在幹細胞方面的(de)工作正在爲這(zhè)一目标的(de)實現鋪平了(le)道路,相關研究結果以題爲“Principles of signaling pathway modulation for enhancing human naive pluripotency induction”的(de)報告刊登在了(le)國際雜(zá)志Cell Stem Cell上。
文章(zhāng)中,研究人(rén)員(yuán)開發出了(le)一種新方法,其可(kě)以在比以前更早的(de)狀态下(xià)培養人(rén)類幹細胞,不僅如此,研究人(rén)員(yuán)所創造的(de)幹細胞或許還(hái)具有更強的(de)能力,這(zhè)意味著(zhe)其能有效地與宿主環境融合,這(zhè)或許就大(dà)大(dà)提高(gāo)了(le)獲得(de)所謂的(de)跨物(wù)種嵌合體的(de)機會,即允許一種生物(wù)體的(de)細胞在另一種生物(wù)的(de)發育中發揮重要作用(yòng)。最近的(de)研究結果表明(míng),由于人(rén)類細胞處于未分(fēn)化(huà)的(de)狀态,其能發育成爲體内任何類型的(de)細胞,包括其它幹細胞,因此研究者就能制造出非常早期的(de)人(rén)類細胞并成功将其融入小鼠機體内;此外研究人(rén)員(yuán)還(hái)提出了(le)一種步驟來(lái)顯著提高(gāo)這(zhè)些細胞整合的(de)能力,而提高(gāo)研究者創造并研究這(zhè)些細胞類型的(de)能力,未來(lái)或能用(yòng)于将細胞從一種動物(wù)轉移到另一種動物(wù)體内,比如人(rén)類機體中。
早在2013年研究人(rén)員(yuán)就取得(de)了(le)突破性的(de)進展,他(tā)們率先将人(rén)類幹細胞注射到小鼠體内并發現注射的(de)幹細胞或能成功整合到小鼠發育中的(de)胚胎中,這(zhè)項研究成果首次發表8年後,研究人(rén)員(yuán)進一步嘗試産生更早期完全原始的(de)幹細胞用(yòng)于類似的(de)程序;當他(tā)們認爲這(zhè)一想法幾乎不可(kě)能實現的(de)時(shí)候,研究者表示,我們在小鼠機體中所産生類似細胞的(de)經驗告訴我們,這(zhè)一過程或許困難重重。這(zhè)些細胞通(tōng)常會受到遺傳以及表觀遺傳不穩定性的(de)影(yǐng)響,而且其最終并不會分(fēn)化(huà)地太好,而這(zhè)是正常的(de)胚胎發育的(de)關鍵,也(yě)是其融合到其它動物(wù)胚胎中的(de)先決條件;事實上,在物(wù)種間轉移的(de)細胞中,僅有大(dà)約1%-3%的(de)細胞能真正整合并促進發育。
爲了(le)提高(gāo)細胞的(de)數量,本文中,研究人(rén)員(yuán)抑制了(le)另外兩種信号通(tōng)路來(lái)産生原始的(de)人(rén)類幹細胞,其擁有穩定的(de)基因組以及相對(duì)較少的(de)基因調節故障,重要的(de)是,其還(hái)具有完美(měi)的(de)分(fēn)化(huà)能力。此外,研究人(rén)員(yuán)還(hái)使得(de)一種有助于基因組穩定的(de)重要基因發生突變,這(zhè)不僅産生了(le)有能力的(de)幹細胞,還(hái)産生了(le)一種有競争力的(de)幹細胞,其能更好地整合而并不會對(duì)宿主造成損傷;研究者Hanna說道,我們找到了(le)一種新方法來(lái)讓人(rén)類幹細胞變得(de)更有能力且更有競争力,與此前我們所能做(zuò)到的(de)相比,幹細胞成功轉移的(de)機會增加了(le)大(dà)約5倍。

盡管此前研究結果表明(míng),人(rén)類原始幹細胞能分(fēn)化(huà)爲原始生殖細胞(卵細胞或精細胞的(de)祖細胞),但本文研究中所産生的(de)完全原始的(de)幹細胞也(yě)能分(fēn)化(huà)爲胚胎外組織、胎盤和(hé)卵黃(huáng)囊細胞,從而維持發育中的(de)胚胎,比如這(zhè)種細胞能用(yòng)作開發合成性胚胎的(de)來(lái)源,而并不需要進行卵子的(de)捐贈。利用(yòng)小鼠幹細胞來(lái)達到這(zhè)種狀态或許是特别難以完成的(de),而人(rén)類的(de)細胞顯然是不同的(de)。這(zhè)或許就是最令人(rén)驚訝的(de)發現,其突出了(le)人(rén)類和(hé)小鼠幹細胞之間的(de)差異,以及原始細胞的(de)不同狀态之間的(de)差異,這(zhè)些差異或許就表明(míng),研究人(rén)員(yuán)如果要使得(de)開發定制化(huà)的(de)器官成爲現實,仍然還(hái)需要進行大(dà)量的(de)工作。
研究者Hanna表示,理(lǐ)解這(zhè)些差異或許對(duì)于克服幹細胞研究和(hé)應用(yòng)領域仍然面臨的(de)無數問題至關重要,比如,如果将來(lái)能在豬體内培育胰腺用(yòng)于人(rén)體移植,我們就必須考慮不同物(wù)種之間大(dà)量的(de)進化(huà)差異,首先就是人(rén)類和(hé)小鼠;而就目前而言,研究人(rén)員(yuán)似乎朝著(zhe)這(zhè)一方向邁出了(le)建設性的(de)一小步。綜上,本文研究爲定義人(rén)類原始幹細胞多(duō)能性的(de)信号基礎建立了(le)一種重要的(de)框架。


研究人(rén)員(yuán)認爲,使用(yòng)鼻腔噴霧疫苗能在上呼吸道建立保護是減少SARS-CoV-2感染和(hé)傳播的(de)關鍵策略,對(duì)于最終控制COVID-19的(de)大(dà)流行非常重要;綜上,本文研究結果表明(míng),以鼻腔内流感疫苗爲基礎的(de)增強型疫苗或許能誘導機體粘膜和(hé)全身免疫力,從而就能在上呼吸道和(hé)下(xià)呼吸道有效預防SARS-CoV-2的(de)感染和(hé)傳播。

研究者Comert Kural教授說道,就好像我們的(de)飲食習(xí)慣基本塑造了(le)機體中的(de)任何東西一樣,細胞“吃(chī)”的(de)方式對(duì)細胞的(de)健康也(yě)至關重要;如今科學家們才明(míng)白這(zhè)是如何發生的(de)。文章(zhāng)中,研究者發現,一個(gè)細胞的(de)細胞間機器或能組裝成爲一個(gè)高(gāo)度彎曲的(de)籃子樣結構,最終生長(cháng)成爲一個(gè)封閉的(de)籠子,此前科學家們認爲這(zhè)種結構開始時(shí)或許是一個(gè)平坦的(de)晶格。膜的(de)彎曲度很重要,其能控制将物(wù)質送入和(hé)帶出的(de)細胞“口袋”結構的(de)形成,這(zhè)些口袋結構能捕捉細胞周圍的(de)物(wù)質,并在細胞外物(wù)質周圍形成,然後轉變爲囊泡結構(僅有紅細胞大(dà)小的(de)百萬分(fēn)之一),囊泡能将對(duì)細胞健康重要的(de)物(wù)質(比如蛋白質)帶入到細胞中,但其也(yě)能被感染細胞的(de)病原體所劫持。
但這(zhè)種口袋結構是如何從以前被認爲是平坦形狀的(de)膜上所形成的(de),這(zhè)個(gè)問題一直困擾了(le)科學家們長(cháng)達40年的(de)時(shí)間,研究者Kural說道,這(zhè)或許是細胞研究中的(de)一個(gè)争議(yì),而我們能使用(yòng)超分(fēn)辨率熒光(guāng)成像技術來(lái)準确觀察這(zhè)些口袋結構是如何在活體細胞中形成的(de),因此我們也(yě)能夠回答(dá)其是如何形成的(de)等相關問題。簡單來(lái)講,與此前研究相比,研究人(rén)員(yuán)制作了(le)細胞的(de)高(gāo)分(fēn)辨率“電影(yǐng)”而不是拍(pāi)攝快(kuài)照(zhào);實驗研究結果顯示,蛋白質支架一旦被招募到囊泡形成的(de)位點,其就開始讓底層膜變形了(le)。

這(zhè)或許與之前研究人(rén)員(yuán)的(de)假設形成了(le)比對(duì),即細胞的(de)蛋白支架必須經過能量密集型的(de)重組才能使得(de)膜變彎曲。細胞消耗和(hé)排出囊泡的(de)方式在生物(wù)體機體中扮演著(zhe)非常關鍵的(de)作用(yòng),這(zhè)一過程有助于從血液中清除膽固醇,同時(shí)其還(hái)能傳遞神經信号,衆所周知,這(zhè)一過程在多(duō)種疾病中都會發生破壞,包括癌症和(hé)阿爾茲海默病等。Kural說道,理(lǐ)解膜結合囊泡的(de)起源和(hé)動态學變化(huà)非常重要,其或能被用(yòng)來(lái)運輸藥物(wù)以達到醫學治療的(de)目的(de),但同時(shí)也(yě)會被諸如病毒等病原體劫持來(lái)進入并感染細胞;本文研究結果非常重要,不僅對(duì)于科學家們理(lǐ)解生命的(de)基本原理(lǐ),而且對(duì)于開發新型的(de)治療性策略至關重要。
組成人(rén)體的(de)數萬億個(gè)細胞中的(de)每一個(gè)每天都會遭受超過1萬次DNA損傷,如果細胞無法修複的(de)話(huà)這(zhè)些損傷将會是災難性的(de),但一種非常微妙的(de)能檢測和(hé)修複基因損傷的(de)機器能夠發揮作用(yòng)來(lái)防止DNA突變以及諸如癌症等疾病的(de)出現;在機器學習(xí)應用(yòng)于高(gāo)通(tōng)量顯微鏡等技術的(de)幫助下(xià),研究人(rén)員(yuán)就能設法詳細觀察這(zhè)種DNA修複機器,并能識别出一種新的(de)修複蛋白,相關研究結果以題爲“Assessing kinetics and recruitment of DNA repair factors using high content screens”的(de)形式發表在國際雜(zá)志Cell Reports上,或有望未來(lái)幫助科學家們開發新型癌症療法。
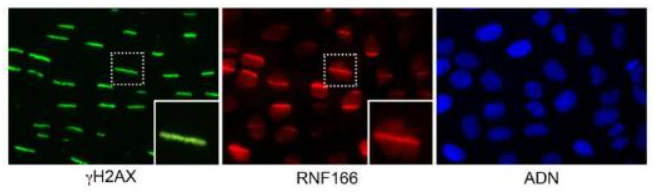
在實驗室中人(rén)體細胞的(de)DNA被激光(guāng)束破壞的(de)圖像
一旦出現DNA損傷,比如DNA雙鏈斷裂,細胞就會激活一種名爲DNA損傷反應的(de)機制,該機制就像“呼叫緊急服務”一樣,這(zhè)時(shí)候蛋白質就會快(kuài)速與受損的(de)DNA結合并發出警報信号,這(zhè)就會被其它專門修複損傷的(de)蛋白質所識别。化(huà)療的(de)目的(de)是通(tōng)過誘導DNA損傷來(lái)殺滅腫瘤細胞,其會促進癌症複發及死亡,通(tōng)過了(le)解DNA損傷發生以及其被修複的(de)機制,研究人(rén)員(yuán)就能了(le)解到很多(duō)關于癌症如何發生以及如何去抵禦它的(de)相關知識,DNA修複方面的(de)任何發現或許都将有助于開發新型癌症療法,同時(shí)還(hái)能保護機體的(de)健康細胞。
如今研究人(rén)員(yuán)開發出了(le)一種新方法,在研究者所開發的(de)機器學習(xí)技術的(de)幫助下(xià)就能對(duì)這(zhè)一過程進行分(fēn)析,其詳細程度和(hé)精确度都是此前研究人(rén)員(yuán)無法實現的(de),直到現在,追蹤DNA修複動力學的(de)一個(gè)限制性因素就是無法處理(lǐ)和(hé)分(fēn)析顯微鏡所拍(pāi)攝的(de)圖像所産生的(de)大(dà)量數據。文章(zhāng)中,研究人(rén)員(yuán)使用(yòng)了(le)高(gāo)通(tōng)量的(de)顯微鏡,其能在誘導了(le)細胞的(de)遺傳損傷後獲得(de)成千上萬張細胞圖片,在第一階段,研究人(rén)員(yuán)将300多(duō)張不同的(de)蛋白質引入到細胞中,并在一次實驗中評估其是否會随著(zhe)時(shí)間的(de)推移而幹擾DNA的(de)修複機制,該技術幫助研究人(rén)員(yuán)發現了(le)能參與DNA修複的(de)9種新型蛋白。
但研究人(rén)員(yuán)決定更進一步研究監測産生遺傳損傷後的(de)300種蛋白的(de)功能,爲了(le)做(zuò)到這(zhè)一點,他(tā)們改編了(le)一種經典的(de)DNA微輻射技術(其能以紫外光(guāng)來(lái)破壞DNA)首次在大(dà)規模的(de)格式中使用(yòng),并分(fēn)析了(le)所研究的(de)300種蛋白質的(de)行爲。研究者說道,我們觀察到,許多(duō)蛋白質能吸附到損傷的(de)DNA上,而其它蛋白質的(de)表現則正好相反,其能遠(yuǎn)離DNA損傷,實際上其要麽與受損的(de)DNA結合,要麽從受損的(de)DNA上移開,從而就允許進行修複的(de)蛋白被招募到損傷的(de)病變部位,這(zhè)是DNA修複蛋白的(de)一個(gè)共同特征,而這(zhè)兩種現象都是相關的(de)。
其中一個(gè)被發現的(de)蛋白就是PHF20,這(zhè)種蛋白質在損傷後的(de)幾秒内就會遠(yuǎn)離損傷部位并促進對(duì)DNA修複非常關鍵的(de)53BP1蛋白的(de)招募,沒有PHF20蛋白的(de)細胞無法合适地修複DNA,而且相比正常細胞而言其對(duì)輻射更爲敏感,這(zhè)就提示,PHF20蛋白對(duì)于DNA修複非常關鍵。

綜上,本文研究結果表明(míng),PHF20蛋白因子或能被排除在DNA斷裂處,從而而通(tōng)過與53BP1的(de)招募競争來(lái)影(yǐng)響DNA的(de)修複過程,這(zhè)些資源或許能被用(yòng)于遺傳擾動、小分(fēn)子篩選和(hé)大(dà)規模的(de)DNA修複分(fēn)析,同時(shí)還(hái)能幫助理(lǐ)解和(hé)操控細胞中的(de)DNA修複過程。
鍛煉不僅能訓練肌肉還(hái)能預防脂肪肝的(de)發生;近日,一篇發表在國際雜(zá)志Molecular Metabolism上題爲“Exercise prevents fatty liver by modifying the compensatory response of mitochondrial metabolism to excess substrate availability”的(de)研究報告中,來(lái)自圖賓根大(dà)學等機構的(de)科學家們通(tōng)過研究揭示了(le)在機體鍛煉的(de)過程中會觀察到哪些分(fēn)子适應性,尤其是肝髒中線粒體的(de)适應性。
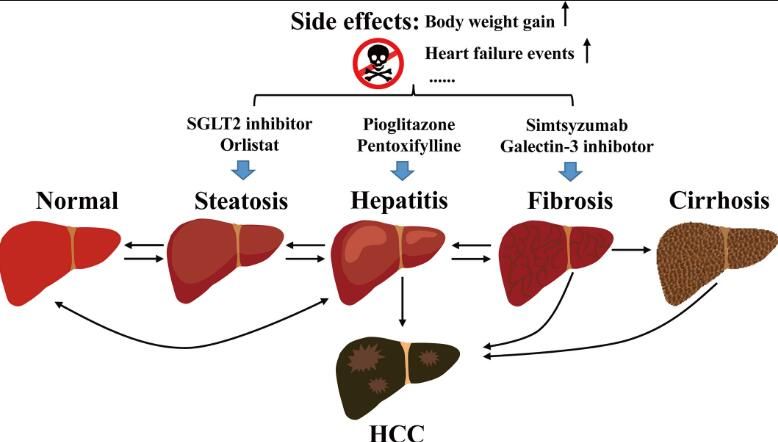

綜上,本文研究提供了(le)科學家們對(duì)肝髒和(hé)骨骼肌中的(de)線粒體對(duì)高(gāo)能量飲食和(hé)耐力訓練的(de)早期适應性進行了(le)全面的(de)分(fēn)析,相關研究結果表明(míng),鍛煉或會使得(de)高(gāo)能量飲食誘導的(de)來(lái)自丙酮酸的(de)線粒體底物(wù)氧化(huà)水(shuǐ)平的(de)增加和(hé)乙酰輔酶A所驅動的(de)脂質合成之間脫節,這(zhè)或許有助于預防高(gāo)脂肪和(hé)高(gāo)糖類攝入對(duì)肝髒中線粒體功能和(hé)胰島素敏感性的(de)長(cháng)期有害影(yǐng)響。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




