在一項新的(de)研究中,研究人(rén)員(yuán)通(tōng)過結合核酸細胞儀、微流控技術和(hé)液滴分(fēn)選,開發出FIND-seq,可(kě)根據數字液滴PCR檢測的(de)mRNA生物(wù)标志物(wù)的(de)表達來(lái)分(fēn)離和(hé)分(fēn)析感興趣的(de)罕見細胞。
罕見的(de)細胞類型可(kě)能對(duì)人(rén)類健康産生不适當的(de)影(yǐng)響。以前的(de)研究已表明(míng)大(dà)腦(nǎo)和(hé)脊髓中的(de)星形膠質細胞的(de)一個(gè)亞群可(kě)能是導緻多(duō)發性硬化(huà)症(MS)的(de)原因。在這(zhè)種疾病中,免疫系統會攻擊保護神經的(de)覆蓋層。
但要找到這(zhè)些罕見的(de)細胞并非易事,科學家們需要确定獨特的(de)表面标志物(wù),以将這(zhè)些罪魁禍首細胞與其他(tā)細胞區(qū)分(fēn)開來(lái)。單細胞RNA測序可(kě)以幫助找到它們,即使在沒有區(qū)分(fēn)性的(de)表面标志物(wù)的(de)情況下(xià),也(yě)是如此,但是這(zhè)種技術可(kě)能變得(de)極其昂貴。

爲了(le)解決這(zhè)個(gè)問題,在一項新的(de)研究中,來(lái)自美(měi)國布萊根婦女(nǚ)醫院和(hé)加州大(dà)學舊(jiù)金山分(fēn)校等研究機構的(de)研究人(rén)員(yuán)通(tōng)過結合核酸細胞儀、微流控技術和(hé)液滴分(fēn)選,開發出FIND-seq,可(kě)根據數字液滴PCR檢測的(de)mRNA生物(wù)标志物(wù)的(de)表達來(lái)分(fēn)離和(hé)分(fēn)析感興趣的(de)罕見細胞。相關研究結果于2023年1月(yuè)3日在線發表在Nature期刊上,論文标題爲“Identification of astrocyte regulators by nucleic acid cytometry”。
通(tōng)過使用(yòng)這(zhè)種方法,這(zhè)些作者非常詳細地分(fēn)析了(le)驅動中樞神經系統炎症和(hé)神經退化(huà)的(de)星形膠質細胞群體。當與其他(tā)工具結合使用(yòng)時(shí),FIND-seq确定了(le)由鹽皮質激素受體NR3C2和(hé)NCOR2(nuclear receptor corepressor 2)控制的(de)信号通(tōng)路,這(zhè)些信号通(tōng)路在小鼠和(hé)人(rén)類的(de)緻病性星形膠質細胞的(de)産生中起著(zhe)重要作用(yòng)。在另一項研究中,他(tā)們利用(yòng)FIND-seq确定了(le)HIV在接受抗逆轉錄病毒療法治療的(de)患者中用(yòng)來(lái)“躲藏”免疫細胞的(de)機制(Nature, 2023, doi:10.1038/s41586-022-05556-6)。
論文共同通(tōng)訊作者、布萊根婦女(nǚ)醫院神經學系的(de)Francisco Quintana博士說,“這(zhè)些發現爲針對(duì)諸如多(duō)發性硬化(huà)症類的(de)神經系統疾病的(de)治療幹預确定了(le)新的(de)靶标。”這(zhè)些作者正在努力開發新的(de)可(kě)用(yòng)于在治療上靶向該信号通(tōng)路的(de)小分(fēn)子。
在一項新的(de)研究中,研究人(rén)員(yuán)報告了(le)允許對(duì)單細胞進行多(duō)維表征(單細胞蛋白基因組分(fēn)析)的(de)新技術的(de)應用(yòng),研究了(le)直接從HIV-1感染者身上分(fēn)離的(de)HIV病毒庫細胞。
感染後不久,HIV-1通(tōng)過在體内形成病毒庫(viral reservoir)---感染了(le)HIV但不積極産生新病毒的(de)細胞,從而建立起終身感染。抗逆轉錄病毒療法(ART)降低了(le)血液中的(de)HIV水(shuǐ)平,但是一小部分(fēn)感染這(zhè)種病毒的(de)細胞會無限期地存在,使HIV感染成爲一種不治之症。那些能夠在停止ART治療後重新觸發感染的(de)細胞極其罕見,而且直到現在還(hái)沒有被識别和(hé)表征。
在一項新的(de)研究中,來(lái)自美(měi)國國家過敏與傳染病研究所、拉根研究所和(hé)麻省總醫院的(de)研究人(rén)員(yuán)報告了(le)允許對(duì)單細胞進行多(duō)維表征(單細胞蛋白基因組分(fēn)析)的(de)新技術的(de)應用(yòng),研究了(le)直接從HIV-1感染者身上分(fēn)離的(de)HIV病毒庫細胞。通(tōng)過這(zhè)種新的(de)技術方法,他(tā)們發現了(le)标志性的(de)表面标志物(wù),這(zhè)可(kě)能解釋了(le)一些HIV病毒庫細胞如何能夠長(cháng)期存在并抵抗宿主的(de)免疫反應。這(zhè)一發現可(kě)能爲未來(lái)治愈HIV感染的(de)策略提供參考。相關研究結果于2023年1月(yuè)4日在線發表在Nature期刊上,論文标題爲“Phenotypic signatures of immune selection in HIV-1 reservoir cells”。

論文通(tōng)訊作者、哈佛醫學院醫學教授Mathias Lichterfeld博士說,“高(gāo)通(tōng)量單細胞測序如今使我們能夠精确地研究極少數受感染細胞的(de)表面特征,盡管接受了(le)ART治療,這(zhè)些細胞仍能終身存在,并且在停止治療後會促進HIV反彈。有了(le)這(zhè)些知識,我們就能了(le)解它們的(de)易感性和(hé)脆弱性,并能開發出靶向這(zhè)些細胞的(de)定制免疫反應。”
這(zhè)些作者收集了(le)5名HIV陽性研究參與者的(de)外周血細胞。其中的(de)四名參與者已接受了(le)大(dà)約10年的(de)ART治療,還(hái)有1人(rén)是盡管沒有接受ART治療但血液中的(de)HIV水(shuǐ)平卻無法檢測出來(lái)的(de)“精英控制者(elite controller)”。他(tā)們還(hái)分(fēn)析了(le)其中的(de)兩名參與者在接受ART治療僅1-2年後的(de)早期血液樣本。他(tā)們還(hái)收集了(le)三名已接受了(le)10~15年ART治療的(de)HIV陽性研究參與者的(de)淋巴結細胞。從這(zhè)些樣本中,他(tā)們分(fēn)離出了(le)CD4+記憶T細胞,即在對(duì)感染作出反應時(shí)産生的(de)白細胞,它們是HIV的(de)主要靶細胞。
這(zhè)些作者開發了(le)一種新的(de)實驗策略,稱爲表型和(hé)前病毒測序(phenotypic and proviral sequencing, PheP-Seq),這(zhè)是一種單細胞下(xià)一代測序技術,用(yòng)于評估單個(gè)病毒感染細胞表面上的(de)生物(wù)标志物(wù)。利用(yòng)PheP-Seq,他(tā)們分(fēn)析了(le)53萬多(duō)個(gè)外周血細胞和(hé)39.6萬個(gè)淋巴結細胞。
含有完整HIV前病毒---完整的(de)HIV病毒基因組整入宿主細胞DNA---的(de)HIV病毒庫細胞的(de)表面生物(wù)标志物(wù)經常與對(duì)細胞毒性T細胞和(hé)NK細胞---兩種通(tōng)常能保護免受病毒感染的(de)免疫細胞---殺傷的(de)抵抗力增加有關。這(zhè)些HIV病毒庫細胞也(yě)有限制病毒基因轉錄的(de)免疫檢查點标志物(wù)的(de)高(gāo)表達。這(zhè)意味著(zhe)一些HIV-1病毒庫細胞具有特定的(de)特性,這(zhè)些特性可(kě)能會減少暴露于免疫系統并被免疫系統殺死,這(zhè)可(kě)能解釋爲什(shén)麽它們會持續存在于體内。研究參與者開始ART治療1~2年後收集的(de)一些HIV-1病毒庫細胞已經顯示出這(zhè)些生物(wù)标志物(wù)和(hé)免疫檢查點标志物(wù)的(de)表達增加,盡管相對(duì)于ART治療後期,這(zhè)些變化(huà)并不明(míng)顯,而在ART治療後期,這(zhè)些抵抗性病毒庫細胞變得(de)更容易被識别。來(lái)自淋巴結的(de)帶有完整病毒的(de)細胞顯示出促進細胞存活的(de)表面标志物(wù)的(de)上調,使得(de)這(zhè)些抵抗性病毒庫細胞具有選擇性優勢。
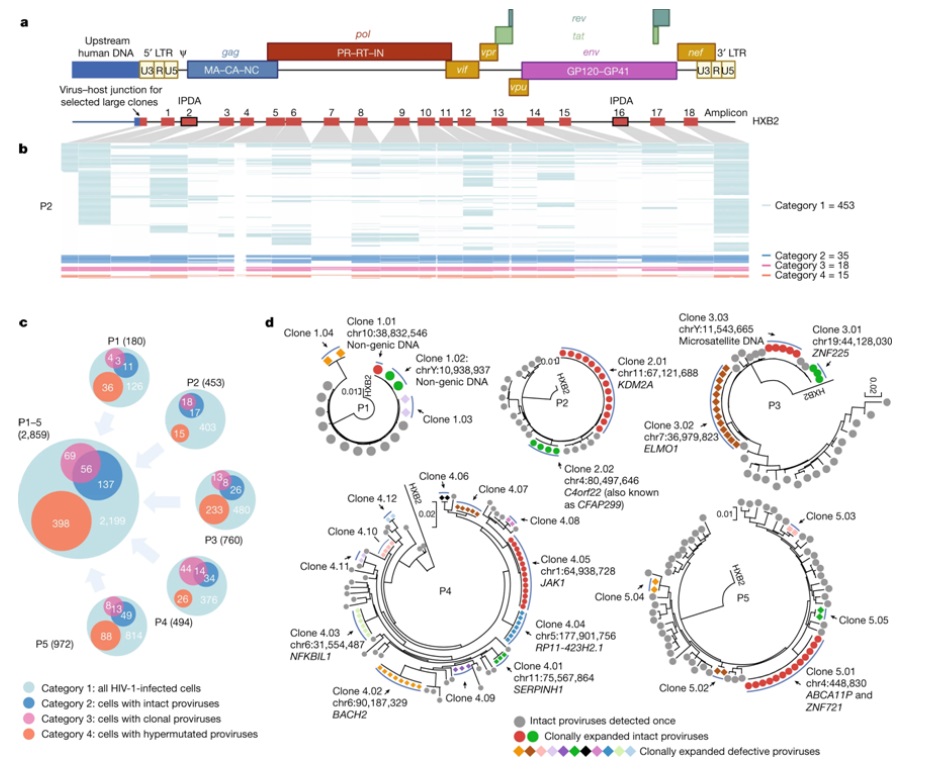
圖爲 來(lái)自外周血的(de)HIV-1感染細胞的(de)細胞表型和(hé)前病毒序列的(de)聯合評估(PheP-seq)
總體來(lái)說,這(zhè)些結果表明(míng),隻有一小部分(fēn)受感染的(de)病毒庫細胞能以最佳方式躲避免疫系統,并在長(cháng)期ART治療中存活下(xià)來(lái)。此外,這(zhè)些數據表明(míng),人(rén)類免疫系統能夠對(duì)大(dà)多(duō)數HIV病毒庫細胞施加有效的(de)免疫選擇壓力。
這(zhè)些作者指出,這(zhè)些生物(wù)标志物(wù)不太可(kě)能在所有接受ART治療的(de)HIV感染者中普遍存在,因爲免疫選擇壓力可(kě)能因個(gè)體免疫反應的(de)差異而不同。盡管如此,識别區(qū)分(fēn)HIV病毒庫細胞的(de)表型生物(wù)标志物(wù)可(kě)能爲未來(lái)的(de)HIV-1治愈研究提供信息。如果科學家們能夠開發出旨在加強和(hé)加快(kuài)對(duì)HIV-1病毒庫細胞的(de)免疫選擇的(de)臨床策略,他(tā)們可(kě)能能夠減少HIV的(de)長(cháng)期持續存在并誘發無藥緩解。
論文共同作者、拉根研究所所長(cháng)Bruce Walker博士說,“四十多(duō)年來(lái),HIV已緩慢(màn)但逐步地揭示了(le)它的(de)秘密,而這(zhè)是另一個(gè)被揭示的(de)關鍵秘密。将單個(gè)病毒庫細胞進行可(kě)視化(huà)觀察的(de)能力曾是一個(gè)白日夢,而如今已成爲現實。如今我們必須在這(zhè)些信息的(de)基礎上根除這(zhè)些病毒庫細胞。”
兩篇Nature論文描述了(le)一種新發現的(de)CRISPR-Cas免疫系統的(de)結構和(hé)功能,與更知名的(de)讓外來(lái)基因滅活來(lái)保護細胞的(de)CRISPR-Cas系統不同,這(zhè)種新的(de)系統關閉受感染的(de)細胞來(lái)阻擋感染。
像人(rén)類一樣,細菌和(hé)古生菌也(yě)會受到病毒的(de)攻擊。這(zhè)些微生物(wù)已進化(huà)出自己的(de)免疫防禦策略,以對(duì)抗它們的(de)病原體。細菌防禦系統,如CRISPR-Cas系統,具有多(duō)樣化(huà)的(de)蛋白和(hé)功能,幫助細菌保護自己免受外來(lái)入侵者入侵。
這(zhè)種免疫防禦基于一個(gè)共同的(de)機制:CRISPR核糖核酸(CRISPR ribonucleic acid, crRNA)作爲“向導RNA(gRNA)”,幫助檢測外來(lái)基因組(比如病毒DNA)的(de)區(qū)域,以便進行靶向切割。由crRNA指導的(de)CRISPR相關(Cas)核酸酶可(kě)以像一把剪刀(dāo)一樣切割它的(de)靶标:這(zhè)是人(rén)類在許多(duō)技術中利用(yòng)的(de)一種自然策略。

美(měi)國猶他(tā)州立大(dà)學的(de)生物(wù)化(huà)學學者Thomson Hallmark和(hé)Ryan Jackson與他(tā)們的(de)合作者一起,發表了(le)兩篇具有開創性的(de)論文。他(tā)們的(de)研究結果描述了(le)一種新發現的(de)CRISPR-Cas免疫系統的(de)結構和(hé)功能,與更知名的(de)讓外來(lái)基因滅活來(lái)保護細胞的(de)CRISPR-Cas系統不同,這(zhè)種新的(de)系統關閉受感染的(de)細胞來(lái)阻擋感染。相關研究結果于2023年1月(yuè)4日在線發表在Nature期刊上,論文标題分(fēn)别爲“Cas12a2 elicits abortive infection through RNA-triggered destruction of dsDNA”和(hé)“RNA targeting unleashes indiscriminate nuclease activity of CRISPR–Cas12a2”。

作爲第一篇論文第一作者的(de)Oleg Dmytrenko博士說,“我們正在探索最初與Cas12a歸類在一起的(de)CRISPR核酸酶,這(zhè)類核酸酶通(tōng)過識别和(hé)切割侵入性DNA來(lái)保護細菌。一旦我們發現了(le)更多(duō)的(de)它們,我們就意識到它們與Cas12a有足夠的(de)不同,可(kě)以進行更深入的(de)研究。這(zhè)種探索使我們發現這(zhè)些我們稱之爲Cas12a2的(de)核酸酶,它們不僅與Cas12a有很大(dà)的(de)不同,而且與任何其他(tā)已知的(de)CRISPR核酸酶也(yě)有很大(dà)的(de)不同。”
關鍵的(de)區(qū)别在于它們的(de)防禦行動機制。當Cas12a2識别入侵的(de)RNA時(shí),該核酸酶會對(duì)它進行切割,但也(yě)能破壞細胞内的(de)其他(tā)RNA和(hé)DNA,破壞該細胞的(de)生長(cháng)并限制感染的(de)擴散。Dmytrenko說,“一般來(lái)說,這(zhè)種稱爲頓挫性感染的(de)防禦策略在細菌中已經被發現。其他(tā)一些CRISPR-Cas系統以這(zhè)種方式工作。然而,一種基于CRISPR的(de)防禦機制,依靠單一的(de)核酸酶來(lái)識别入侵者并降解細胞DNA和(hé)RNA,以前還(hái)沒有被觀察到。”
Cas12a2的(de)蛋白序列和(hé)結構将這(zhè)種核酸酶與Cas12a區(qū)分(fēn)開來(lái)。在一種前間隔序列側翼位點(protospacer-flanking sequence, PFS)的(de)激活下(xià),Cas12a2能識别與它的(de)gRNA互補的(de)靶RNA。靶向靶RNA會引發附帶的(de)核酸裂解,降解RNA、單鏈DNA和(hé)雙鏈DNA。這(zhè)種活性導緻細胞停滞,可(kě)能是通(tōng)過破壞細胞中的(de)DNA和(hé)RNA,從而損害生長(cháng)。Cas12a2可(kě)用(yòng)于分(fēn)子診斷和(hé)RNA生物(wù)标記物(wù)的(de)直接檢測,這(zhè)已得(de)到原理(lǐ)證明(míng)。
Jackson和(hé)Hallmark是正在破譯CRISPR-Cas系統的(de)基本結構,以及是什(shén)麽讓它們運作的(de)全球研究人(rén)員(yuán)中的(de)一員(yuán)。Jackson說,“我們在這(zhè)兩篇論文中報道的(de)研究結果幾乎是在六年内完成的(de)。”
在過去五年中被确認爲一種獨特的(de)免疫系統,CRISPR-Cas12a2在某種程度上類似于更知名的(de)CRISPR-Cas9,後者與目靶DNA結合并像分(fēn)子剪刀(dāo)一樣切割它,從而有效地關閉靶基因。但是CRISPR-Cas12a2與CRISPR-Cas9結合的(de)靶标不同,而且這(zhè)種結合具有非常不同的(de)效果。
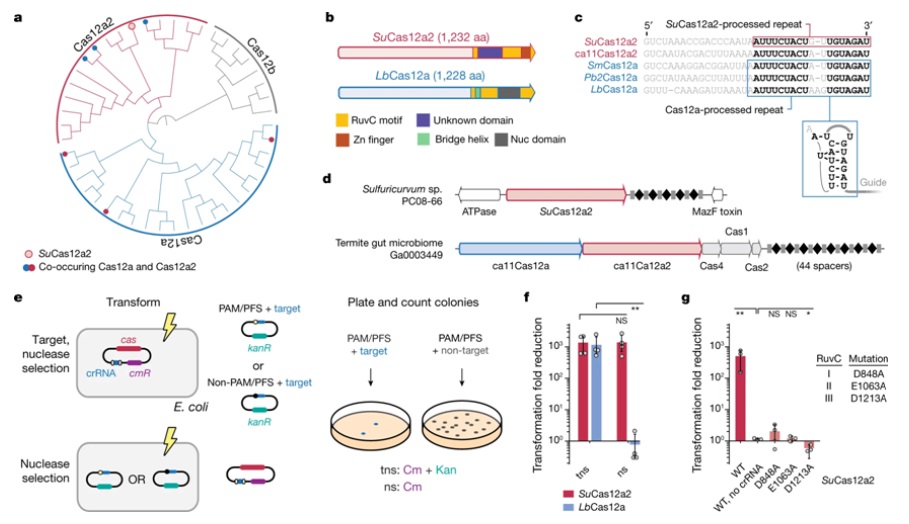
圖爲 Cas12a2核酸酶在V型Cas12核酸酶中形成了(le)一個(gè)獨特的(de)分(fēn)支
Jackson說,“Cas12a2蛋白在與RNA結合時(shí)發生了(le)重大(dà)的(de)構象變化(huà),爲DNA的(de)破壞打開了(le)一個(gè)不加區(qū)分(fēn)的(de)活性位點。Cas12a2破壞了(le)靶細胞中的(de)DNA和(hé)RNA,導緻它們衰老。”
通(tōng)過使用(yòng)低溫電鏡(cryo-electron microscopy, cryo-EM),這(zhè)些作者展示了(le)CRISPR-Cas12a2的(de)這(zhè)一獨特方面,包括它的(de)RNA觸發的(de)單鏈RNA、單鏈DNA和(hé)雙鏈DNA的(de)降解,從而導緻一種自然發生的(de)防禦策略,即頓挫性感染(abortive infection,也(yě)譯爲流産性感染)。
Hallmark說,“頓挫性感染是細菌和(hé)古生菌用(yòng)來(lái)限制病毒和(hé)其他(tā)病原體傳播的(de)一種天然噬菌體抵抗策略。比如,頓挫性感染可(kě)以阻止已感染了(le)宿主細胞的(de)病毒成分(fēn)進行複制。”
Jackson說,該團隊在Cas12a2切割雙鏈DNA的(de)過程中捕捉到了(le)它的(de)結構。他(tā)說,“令人(rén)難以置信的(de)是,Cas12a2核酸酶将通(tōng)常筆直的(de)一段雙螺旋DNA彎曲了(le)90度,以迫使這(zhè)段雙螺旋DNA的(de)骨架進入這(zhè)種核酸酶的(de)活性位點,并在那裏遭受切割。這(zhè)是一種結構上的(de)變化(huà),觀察起來(lái)很不尋常---這(zhè)種現象引起了(le)科學家同行的(de)驚呼。”
在進一步結構分(fēn)析中,他(tā)們發現Cas12a在免疫反應的(de)不同階段與它的(de)靶RNA結合後會發生重大(dà)結構變化(huà)。這(zhè)反過來(lái)又導緻核酸酶出現一個(gè)暴露的(de)裂縫,可(kě)以粉碎它遇到的(de)任何核酸--無論是RNA、單鏈DNA還(hái)是雙鏈DNA。他(tā)們還(hái)發現了(le)一種讓Cas12a2發生突變以改變它在識别它的(de)RNA靶标後降解的(de)核酸的(de)方法。這(zhè)些具體細節爲未來(lái)開辟了(le)潛在的(de)廣泛技術應用(yòng)。
Jackson說,健康細胞和(hé)惡性細胞或被感染的(de)細胞之間存在遺傳上的(de)區(qū)别。他(tā)說,“如果可(kě)以利用(yòng)Cas12a2在遺傳水(shuǐ)平上識别、靶向和(hé)摧毀細胞,那麽它的(de)潛在治療應用(yòng)意義重大(dà)。”
此外,這(zhè)兩篇論文中描述的(de)CRISPR-Cas12a2的(de)RNA診斷能力,可(kě)能推動阻止一些遺傳性疾病影(yǐng)響的(de)努力。
Jackson說,“我們隻是觸及表面,但我們相信CRISPR-Cas12a2可(kě)能導緻改進其他(tā)CRISPR-Cas技術,這(zhè)将大(dà)大(dà)有利于社會。”
在一項新的(de)研究中,來(lái)自美(měi)國艾倫細胞科學研究所(Allen Institute for Cell Science)的(de)研究人(rén)員(yuán)通(tōng)過處理(lǐ)數十萬張高(gāo)分(fēn)辨率圖像,對(duì)人(rén)類細胞的(de)内部組織(internal organization)---一種迄今爲止被證明(míng)非常難以定量确定的(de)生物(wù)學概念---進行了(le)統計。他(tā)們還(hái)捕捉到了(le)關于細胞形狀豐富變化(huà)的(de)細節,即使是在相同條件下(xià)生長(cháng)的(de)基因完全一緻的(de)細胞。相關研究結果于2023年1月(yuè)4日在線發表在Nature期刊上,論文标題爲“Integrated intracellular organization and its variations in human iPS cells”。

論文通(tōng)訊作者、艾倫細胞科學研究所副主任Susanne Rafelski博士說,“細胞的(de)組織方式告訴我們一些關于它們的(de)行爲和(hé)身份的(de)信息。當我們都試圖了(le)解細胞在健康和(hé)疾病中如何變化(huà)時(shí),這(zhè)個(gè)領域一直缺少的(de)是處理(lǐ)這(zhè)種細胞内部組織的(de)嚴格方法。我們還(hái)沒有挖掘出這(zhè)種信息。”
Rafelski說,這(zhè)項新的(de)研究爲生物(wù)學家們提供了(le)一個(gè)路線圖,以一種可(kě)測量的(de)、定量的(de)方式了(le)解不同類型的(de)細胞的(de)内部組織。它還(hái)揭示了(le)這(zhè)些作者研究的(de)稱爲人(rén)類誘導性多(duō)能幹細胞(human induced pluripotent stem cell, iPS細胞)的(de)細胞的(de)一些關鍵組織原則。
了(le)解細胞在健康條件下(xià)如何組織自己---以及“正常”狀态下(xià)所包含的(de)全部變化(huà)---可(kě)以幫助科學家們更好地了(le)解疾病中的(de)問題所在。這(zhè)項新研究中的(de)圖像數據集、經過基因改造的(de)幹細胞和(hé)代碼都是公開的(de),供科學界中的(de)其他(tā)科學家使用(yòng)。
加州大(dà)學舊(jiù)金山分(fēn)校生物(wù)化(huà)學與生物(wù)物(wù)理(lǐ)學教授、艾倫細胞科學研究所科學顧問委員(yuán)會成員(yuán)Wallace Marshall博士說,“使得(de)細胞生物(wù)學看起來(lái)難以解決的(de)部分(fēn)原因是,每個(gè)細胞看起來(lái)都不一樣,即使它們是同一類型的(de)細胞。這(zhè)項新的(de)研究表明(míng),這(zhè)種長(cháng)期困擾該領域的(de)可(kě)變性實際上是研究細胞内部組成規則的(de)一個(gè)機會。這(zhè)種方法幾乎可(kě)以推廣到任何細胞,我期望其他(tā)許多(duō)人(rén)也(yě)能采用(yòng)同樣的(de)方法。”
計算(suàn)我們的(de)細胞的(de)梨形度(pear-ness)
在七年多(duō)前啓動的(de)一項研究中,這(zhè)些作者首先構建了(le)一組經過基因改造後在熒光(guāng)顯微鏡下(xià)可(kě)以照(zhào)亮不同的(de)内部結構的(de)幹細胞。有了(le)對(duì)25種結構進行了(le)熒光(guāng)标記的(de)細胞系,他(tā)們随後捕獲了(le)20萬多(duō)個(gè)不同細胞的(de)高(gāo)分(fēn)辨率三維圖像。
所有這(zhè)些都是爲了(le)提出一個(gè)看似簡單的(de)問題:我們的(de)細胞是如何組織其内部的(de)?他(tā)們的(de)研究結果發現,要找到答(dá)案真地很複雜(zá)。想象一下(xià),你的(de)辦公室裏有數百件不同的(de)家具,所有這(zhè)些家具都需要随時(shí)取用(yòng),而且許多(duō)家具需要自由移動或根據它們的(de)任務進行相互作用(yòng)。現在想象一下(xià),你的(de)辦公室是一個(gè)被一層薄膜包裹著(zhe)的(de)液體囊,而這(zhè)數百件家具中的(de)許多(duō)件甚至是更小的(de)液體袋。這(zhè)是室内設計的(de)噩夢。
這(zhè)些作者想知道:所有這(zhè)些微小的(de)細胞結構彼此之間是如何排列的(de)?“A結構”總是在同一個(gè)地方,還(hái)是随機的(de)?
他(tā)們在比較兩個(gè)不同細胞之間的(de)相同結構時(shí)遇到了(le)挑戰。即使被研究的(de)細胞在基因上是完全相同的(de),并在相同的(de)實驗室環境中培養,它們的(de)形狀也(yě)有很大(dà)的(de)不同。他(tā)們意識到,如果一個(gè)細胞很短,呈斑點狀,另一個(gè)細胞很長(cháng),呈梨形,就不可(kě)能比較兩個(gè)不同細胞中A結構的(de)位置。因此,他(tā)們在那些短粗的(de)斑點和(hé)細長(cháng)的(de)梨上标注了(le)數字。
利用(yòng)計算(suàn)分(fēn)析,這(zhè)些作者開發了(le)他(tā)們所謂的(de)“形狀空間(shape space)”,客觀地描述每個(gè)幹細胞的(de)外部形狀。這(zhè)種形狀空間包括八個(gè)不同的(de)形狀變化(huà)維度,如高(gāo)度、體積、伸長(cháng)率,以及恰如其分(fēn)描述的(de)“梨形度”和(hé)“豆形度(bean-ness)”。然後,他(tā)們可(kě)以将蘋果與蘋果(或豆子與豆子)進行比較,觀察所有類似形狀的(de)細胞内部的(de)結構組織。
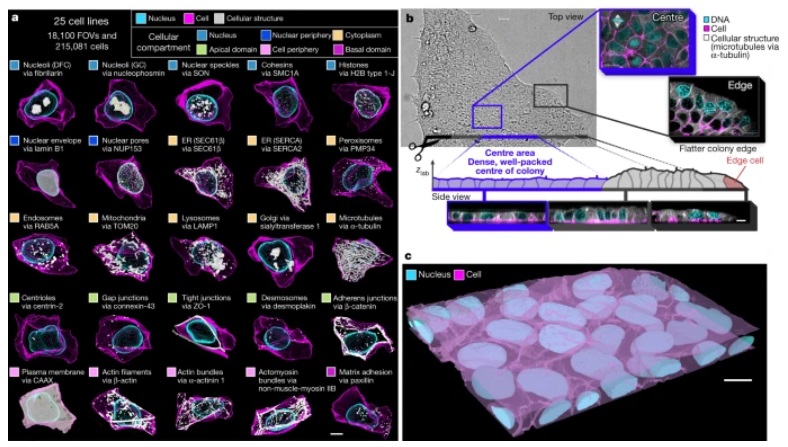
圖爲 WTC-11 hiPSC單細胞圖像數據集v1包括25種代表位于細胞所有主要區(qū)室的(de)關鍵細胞結構的(de)細胞系
論文第一作者、艾倫細胞科學研究所的(de)Matheus Viana博士說,“我們知道,在生物(wù)學中,形狀和(hé)功能是相互關聯的(de),了(le)解細胞形狀對(duì)了(le)解細胞的(de)功能很重要。我們提出了(le)一個(gè)框架,使我們能夠測量一個(gè)細胞的(de)形狀,在你這(zhè)樣做(zuò)的(de)那一刻,你可(kě)以找到形狀相似的(de)細胞,對(duì)于這(zhè)些細胞,你就可(kě)以看裏面的(de)東西是如何排列的(de)。”
嚴格的(de)組織
當他(tā)們觀察這(zhè)25種經過熒光(guāng)标記的(de)結構的(de)位置,比較一組具有類似形狀的(de)細胞中的(de)這(zhè)些結構時(shí),他(tā)們發現所有的(de)細胞都以非常相似的(de)方式工作。盡管細胞形狀存在巨大(dà)的(de)差異,但它們的(de)内部組織卻驚人(rén)地一緻。
如果你觀察一下(xià)高(gāo)層辦公大(dà)樓裏成千上萬的(de)白領如何擺放家具,就好像每個(gè)人(rén)都把辦公桌放在辦公室的(de)正中央,而把文件櫃正好放在最左邊的(de)角落,無論辦公室的(de)大(dà)小或形狀如何。如果你發現一間辦公室裏的(de)文件櫃被扔在地上,文件散落一地---這(zhè)可(kě)能會告訴你關于那間特定辦公室和(hé)它的(de)使用(yòng)者的(de)一些情況。
細胞的(de)情況也(yě)是如此。發現偏離正常狀态的(de)情況可(kě)能爲科學家們提供重要信息,了(le)解細胞從靜止狀态過渡到移動狀态、準備分(fēn)裂時(shí)的(de)變化(huà),或者了(le)解在疾病中微觀層面出現的(de)問題。這(zhè)些作者觀察了(le)他(tā)們的(de)數據集中的(de)兩種變化(huà)--處于細胞集落邊緣的(de)細胞,以及正在進行分(fēn)裂以産生新子細胞的(de)細胞,這(zhè)一過程被稱爲有絲分(fēn)裂。在這(zhè)兩種狀态下(xià),他(tā)們能夠找到與細胞的(de)不同環境或活動相關的(de)内部組織變化(huà)。
艾倫細胞科學研究所執行主任Ruwanthi N. Gunawardane博士說,“這(zhè)項研究彙集了(le)我們在艾倫細胞科學研究所成立以來(lái)所做(zuò)的(de)一切。我們從頭開始建立所有這(zhè)些,包括測量和(hé)比較細胞組織方式的(de)不同方面的(de)指标。我真正感到興奮的(de)是,我們和(hé)科學界中的(de)其他(tā)人(rén)如今可(kě)以在此基礎上,提出我們以前無法提出的(de)關于細胞生物(wù)學的(de)問題。”
在一項新的(de)研究中,研究人(rén)員(yuán)構建出一個(gè)包含在人(rén)類細胞中發現的(de)300多(duō)種蛋白激酶的(de)綜合圖譜,并确定了(le)它們可(kě)能靶向和(hé)控制哪些蛋白。相關研究結果于2023年1月(yuè)11日在線發表在Nature期刊上。
人(rén)類最重要的(de)酶之一是蛋白激酶,它們是調節幾乎所有細胞活動(包括生長(cháng)、細胞分(fēn)裂和(hé)代謝)的(de)信号分(fēn)子。這(zhè)些細胞途徑的(de)功能失調可(kě)導緻多(duō)種疾病,特别是癌症。
識别參與細胞功能障礙和(hé)癌症發展的(de)蛋白激酶可(kě)以産生許多(duō)新的(de)藥物(wù)靶标,但是對(duì)于這(zhè)些激酶中的(de)絕大(dà)多(duō)數,科學家們并沒有清楚地了(le)解它們參與了(le)哪些細胞途徑,或者它們的(de)底物(wù)是什(shén)麽。
美(měi)國麻省理(lǐ)工學院精準癌症醫學中心主任Michael Yaffe教授說,“我們有大(dà)量的(de)癌症基因組測序數據,但我們缺少的(de)是對(duì)癌症中信号通(tōng)路和(hé)蛋白激酶激活狀态的(de)大(dà)規模研究。如果我們有這(zhè)些信息,我們就會對(duì)如何治療特定的(de)腫瘤有更好的(de)想法。”

在一項新的(de)研究中,Yaffe、耶魯大(dà)學醫學院的(de)Benjamin E. Turk博士和(hé)威爾康乃爾醫學院的(de)Lewis C. Cantley博士及其同事們構建出一個(gè)包含在人(rén)類細胞中發現的(de)300多(duō)種蛋白激酶的(de)綜合圖譜,并确定了(le)它們可(kě)能靶向和(hé)控制哪些蛋白。這(zhè)些信息可(kě)能幫助科學家們破譯許多(duō)細胞信号通(tōng)路,并幫助他(tā)們發現當細胞發送癌變或用(yòng)特定藥物(wù)治療時(shí),這(zhè)些信号通(tōng)路會發生什(shén)麽變化(huà)。相關研究結果于2023年1月(yuè)11日在線發表在Nature期刊上,論文标題爲“An atlas of substrate specificities for the human serine/threonine kinome”。
可(kě)靠線索
人(rén)類基因組包括500多(duō)種蛋白激酶,它們通(tōng)過給其他(tā)蛋白标記上稱爲磷酸基團的(de)化(huà)學修飾來(lái)激活或失活這(zhè)些蛋白。對(duì)于這(zhè)些激酶中的(de)大(dà)多(duō)數,它們所靶向的(de)蛋白是未知的(de),盡管對(duì)MEK和(hé)RAF等激酶的(de)研究已導緻了(le)抑制這(zhè)些激酶的(de)新癌症藥物(wù),其中MEK和(hé)RAF這(zhè)兩種激酶都參與了(le)控制生長(cháng)的(de)細胞途徑。
爲了(le)确定癌細胞中失調的(de)其他(tā)途徑,這(zhè)些作者依靠使用(yòng)質譜的(de)磷酸化(huà)蛋白質組學(phosphoproteomics)來(lái)發現癌細胞或健康細胞中磷酸化(huà)程度較高(gāo)的(de)蛋白。然而,在此之前,還(hái)沒有一種簡單的(de)方法來(lái)研究質譜數據,以确定哪些蛋白激酶負責磷酸化(huà)這(zhè)些蛋白。正因爲如此,這(zhè)些蛋白在疾病中是如何受到調控或遭受異常調控的(de)仍是未知的(de)。
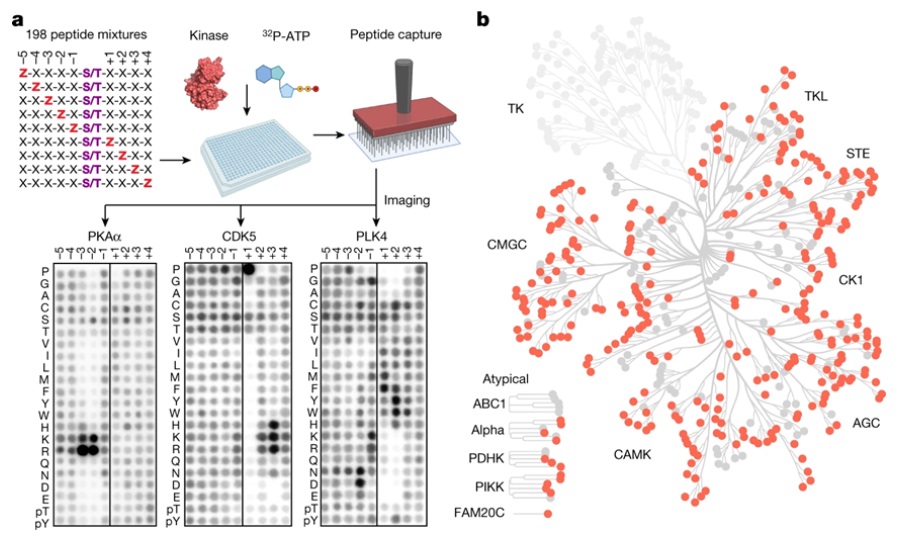
圖爲 分(fēn)析人(rén)類絲氨酸/蘇氨酸激酶組的(de)底物(wù)特異性
Yaffe說,“對(duì)于大(dà)多(duō)數被測量的(de)磷酸肽(phosphopeptide),我們不知道它們在信号傳導途徑中的(de)位置。我們沒有有效線索用(yòng)來(lái)觀察這(zhè)些磷酸肽,然後說,這(zhè)是這(zhè)些數據告訴我們的(de)信号傳導途徑。原因是對(duì)于大(dà)多(duō)數蛋白激酶,我們不知道它們的(de)底物(wù)是什(shén)麽。”
在這(zhè)項新的(de)研究中,這(zhè)些作者分(fēn)析了(le)兩類激酶---絲氨酸激酶和(hé)蘇氨酸激酶,這(zhè)兩類激酶構成了(le)人(rén)體中大(dà)約85%的(de)蛋白激酶。他(tā)們利用(yòng)Cantley和(hé)Turk之前創建的(de)一個(gè)肽庫來(lái)尋找與激酶相互作用(yòng)的(de)基序,随後測量了(le)這(zhè)些肽與所有303種已知的(de)絲氨酸激酶和(hé)蘇氨酸激酶的(de)相互作用(yòng)。對(duì)于這(zhè)兩類激酶而言,通(tōng)過使用(yòng)一種計算(suàn)模型來(lái)分(fēn)析他(tā)們觀察到的(de)相互作用(yòng),他(tā)們能夠識别出能夠使人(rén)類細胞中已報道的(de)9萬個(gè)已知磷酸化(huà)位點中的(de)每一個(gè)磷酸化(huà)的(de)激酶。
令他(tā)們吃(chī)驚的(de)是,這(zhè)些作者發現許多(duō)具有非常不同的(de)氨基酸序列的(de)激酶已經進化(huà)到能夠結合和(hé)磷酸化(huà)其底物(wù)上的(de)相同基序。他(tā)們還(hái)發現,他(tā)們所研究的(de)激酶中約有一半靶向三大(dà)類基序之一,而剩下(xià)的(de)一半則靶向大(dà)約十幾個(gè)小類基序之一。
解碼網絡
Yaffe說,這(zhè)種新的(de)激酶圖譜可(kě)以幫助科學家們識别正常細胞和(hé)癌細胞之間,或經過治療的(de)癌細胞和(hé)未經治療的(de)癌細胞之間不同的(de)信号通(tōng)路。他(tā)說,“這(zhè)個(gè)激酶基序圖譜現在可(kě)以讓我們解讀信号傳導網絡。我們可(kě)以看看所有這(zhè)些磷酸化(huà)的(de)肽,我們可(kě)以把它們對(duì)應到一種特定的(de)激酶上。”
爲了(le)展示這(zhè)種方法,這(zhè)些作者分(fēn)析了(le)用(yòng)一種抗癌藥物(wù)處理(lǐ)的(de)細胞,這(zhè)種藥物(wù)抑制一種叫做(zuò)Plk1的(de)激酶,該激酶調節細胞分(fēn)裂。當他(tā)們分(fēn)析磷酸化(huà)蛋白的(de)表達時(shí),他(tā)們發現許多(duō)受影(yǐng)響的(de)蛋白是由Plk1控制的(de),正如他(tā)們預期的(de)那樣。令他(tā)們吃(chī)驚的(de)是,他(tā)們還(hái)發現這(zhè)種處理(lǐ)增加了(le)兩種激酶的(de)活性,這(zhè)兩種激酶參與了(le)細胞對(duì)DNA損傷的(de)反應。
Yaffe實驗室如今有興趣使用(yòng)這(zhè)種圖譜來(lái)嘗試尋找其他(tā)驅動癌症發展的(de)功能失調的(de)信号通(tōng)路,特别是在某些沒有發現遺傳驅動因素的(de)癌症類型中。
他(tā)說,“我們如今可(kě)以用(yòng)磷蛋白組學說,也(yě)許在這(zhè)個(gè)病人(rén)的(de)腫瘤中,這(zhè)些途徑是上調的(de),或者這(zhè)些途徑是下(xià)調的(de)。我們現在可(kě)以利用(yòng)磷酸化(huà)蛋白質組學來(lái)判斷,也(yě)許在這(zhè)名患者的(de)腫瘤中,這(zhè)些通(tōng)路上調或下(xià)調。它可(kě)能會确定在由不明(míng)顯的(de)遺傳因素導緻癌症的(de)情況下(xià)驅動癌症的(de)信号通(tōng)路。”
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




