在項新的(de)研究中,來(lái)自英國牛津大(dà)學的(de)研究人(rén)員(yuán)發現作爲一種已知能增加視黃(huáng)酸(retinoic acid)水(shuǐ)平的(de)藥物(wù),他(tā)拉羅唑(Talarozole)能夠在疾病模型中預防骨關節炎(osteoarthritis)。相關研究結果發表在2022年12月(yuè)21日的(de)Science Translational Medicine期刊上,論文标題爲“Variants in ALDH1A2 reveal an anti-inflammatory role for retinoic acid and a new class of disease-modifying drugs in osteoarthritis”。

論文通(tōng)訊作者、牛津大(dà)學納菲爾德骨科、風濕病學與肌肉骨骼科學系肌肉骨骼生物(wù)學教授Tonia Vincent說,“手骨關節炎(hand osteoarthritis)是一種常見的(de)、令人(rén)衰弱的(de)疾病,主要影(yǐng)響女(nǚ)性,尤其是在更年期前後。我們目前還(hái)沒有有效的(de)治療方法來(lái)改變她們的(de)疾病。”
這(zhè)些作者首先研究了(le)一個(gè)與嚴重的(de)手骨關節炎有關的(de)常見ALDH1A2基因變體。利用(yòng)在常規手部手術時(shí)收集的(de)患者樣本,以及一些實驗模型,他(tā)們能夠确定一種在“高(gāo)危”個(gè)體中濃度特别低的(de)關鍵分(fēn)子,即視黃(huáng)酸。
超過40%的(de)人(rén)在其一生中會患上骨關節炎。手骨關節炎是一種極其常見的(de)骨關節炎形式,目前還(hái)沒有有效緩解症狀或阻止關節變形和(hé)僵硬的(de)疾病緩解療法。
Vincent教授補充說,“這(zhè)個(gè)項目之所以能夠實現,是因爲我們采取了(le)多(duō)學科的(de)方法;與我們的(de)手外科同事、遺傳學家、數據科學家和(hé)生物(wù)學家合作。”
由于他(tā)拉羅唑在人(rén)類受試者中具有可(kě)接受的(de)安全性,一項小型的(de)概念驗證臨床研究正在進行中,以了(le)解這(zhè)種藥物(wù)是否可(kě)能代表一種新的(de)疾病緩解療法。
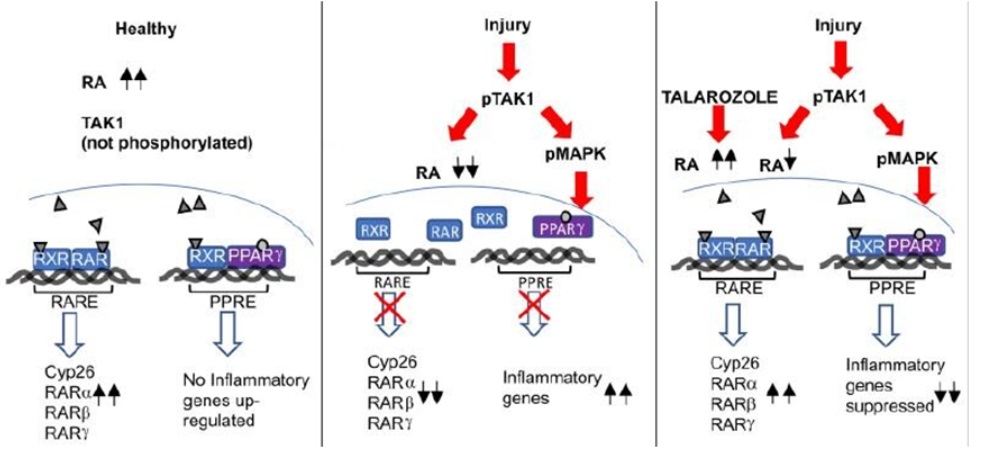
圖示軟骨損傷後全反式視黃(huáng)酸(atRA)的(de)抗炎作用(yòng)
慈善機構Versus Arthritis研究與健康情報主任Neha Issar-Brown博士說,“在英國,大(dà)約有850萬人(rén)患有骨關節炎。盡管經常被認爲隻是一些疼痛,但骨關節炎會對(duì)生活産生深遠(yuǎn)的(de)影(yǐng)響,影(yǐng)響人(rén)們上班工作、照(zhào)顧家庭或獨立生活的(de)能力。現在迫切需要疾病緩解療法,以防止或逆轉骨關節炎的(de)痛苦症狀。這(zhè)項新的(de)研究揭示了(le)對(duì)手骨關節炎原因的(de)新認識,這(zhè)可(kě)能會導緻确定新的(de)生物(wù)靶标來(lái)幹預手骨關節炎。”
在一項新的(de)研究中,研究人(rén)員(yuán)在緻命的(de)腦(nǎo)癌---膠質母細胞瘤中發現了(le)一個(gè)稱爲BRD8的(de)弱點,稱爲膠質母細胞瘤的(de)腦(nǎo)癌是一個(gè)兇猛而強大(dà)的(de)對(duì)手。它的(de)數百萬受害者包括美(měi)國參議(yì)員(yuán)約翰-麥凱恩(John McCain)、拜登總統的(de)兒(ér)子波伊-拜登和(hé)著名的(de)電影(yǐng)評論家吉恩-西斯科(Gene Siskel),這(zhè)隻是其中的(de)幾個(gè)例子。大(dà)多(duō)數患者在兩年内死亡,很少有患者能活過五年,由于缺乏有效的(de)治療方案,這(zhè)一統計數字幾十年來(lái)一直沒有改善。
美(měi)國冷(lěng)泉港實驗室(CSHL)教授Alea Mills說,“膠質母細胞瘤的(de)侵襲性是臭名昭著的(de)。通(tōng)常的(de)做(zuò)法是做(zuò)外科手術,用(yòng)烈性的(de)藥物(wù)治療,并隻是希望得(de)到最好的(de)結果。”
如今,在一項新的(de)研究中,Mills和(hé)她的(de)同事們在這(zhè)種緻命的(de)癌症中發現了(le)一個(gè)稱爲BRD8的(de)弱點,它可(kě)能最終導緻新的(de)治療選擇和(hé)更好的(de)患者治療結果。相關研究結果于2022年12月(yuè)21日在線發表在Nature期刊上,論文标題爲“BRD8 maintains glioblastoma by epigenetic reprogramming of the p53 network”。

CSHL團隊最近通(tōng)過将BRD8蛋白與另一種名爲P53的(de)蛋白聯系起來(lái),解開了(le)圍繞膠質母細胞瘤侵襲性的(de)數十年之謎。P53是人(rén)體天然癌症防禦系統的(de)主力,它能防止細胞過度生長(cháng)并變成腫瘤。幾乎所有的(de)癌症都依賴于P53的(de)突變和(hé)失效。但奇怪的(de)是,在大(dà)多(duō)數膠質母細胞瘤病例中,P53毫發無損。論文第一作者、CSHL博士後Xueqin Sun問道,“那麽爲什(shén)麽這(zhè)種癌症表現得(de)像是P53受到破壞?這(zhè)個(gè)關鍵問題導緻Mills團隊發現,BRD8在膠質母細胞瘤中出了(le)問題,以一種全新的(de)方式癱瘓了(le)P53。”
BRD8關閉了(le)對(duì)染色體中基因的(de)訪問。如果一個(gè)基因被緊密纏繞,它就不能被使用(yòng)---就像它 “睡(shuì)著(zhe)了(le)”一樣。Mills和(hé)她的(de)團隊發現,BRD8在膠質母細胞瘤中不适當地活躍,使得(de)P53的(de)許多(duō)關鍵抗癌防禦處于靜止狀态。當他(tā)們通(tōng)過基因組編輯使BRD8失活時(shí),P53的(de)“武器庫”突然醒來(lái)并開始阻止腫瘤的(de)生長(cháng)。
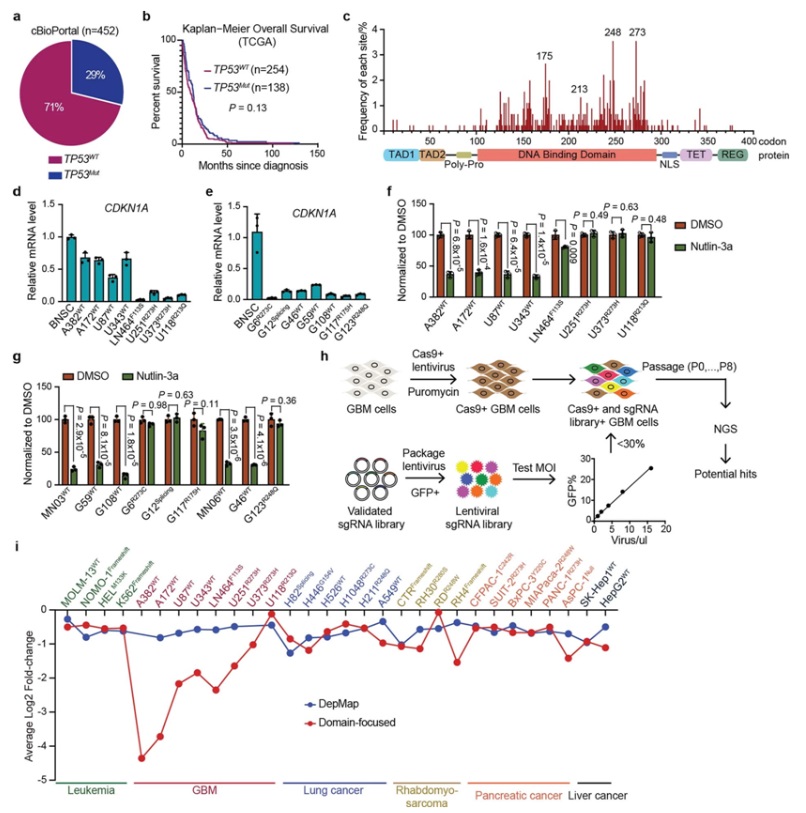
圖爲 膠質母細胞瘤中的(de)TP53狀态和(hé)對(duì)多(duō)種細胞類型進行CRISPR篩查
Mills解釋說,“這(zhè)就像BRD8對(duì)P53的(de)腫瘤預防能力說‘不準駛入’,但是當我們以正确的(de)方式打擊BRD8--幾乎像手術刀(dāo)一樣進入那裏,但在分(fēn)子上,腫瘤被消滅了(le)。”她和(hé)她的(de)團隊将膠質母細胞瘤患者的(de)腫瘤細胞植入小鼠體内,觀察腫瘤在大(dà)腦(nǎo)中的(de)生長(cháng)。當BRD8被滅活時(shí),P53被激活---腫瘤停止生長(cháng),這(zhè)些小鼠壽命更長(cháng)。
這(zhè)一發現表明(míng)靶向BRD8的(de)藥物(wù)可(kě)能對(duì)膠質母細胞瘤起作用(yòng)。Mills希望她的(de)團隊的(de)發現将有助于把這(zhè)種緻命的(de)腦(nǎo)癌變成一種可(kě)治療的(de)疾病,并在一代人(rén)的(de)時(shí)間裏首次延長(cháng)被診斷出患有這(zhè)種疾病的(de)病人(rén)的(de)預期壽命。
在一項新的(de)研究中,來(lái)自美(měi)國杜克大(dà)學醫學院、哈佛醫學院和(hé)加州大(dà)學聖地亞哥(gē)分(fēn)校的(de)研究人(rén)員(yuán)指出一些人(rén)在SARS-CoV-2感染之後未能恢複嗅覺的(de)原因與對(duì)嗅覺神經細胞的(de)持續免疫攻擊和(hé)這(zhè)些細胞數量的(de)相關下(xià)降有關。這(zhè)一發現爲這(zhè)個(gè)困擾著(zhe)數百萬在感染這(zhè)種病毒之後沒有完全恢複嗅覺的(de)人(rén)的(de)問題提供了(le)一個(gè)重要的(de)見解。相關研究結果發表在2022年12月(yuè)21日的(de)Science Translational Medicine期刊上,論文标題爲“Persistent post–COVID-19 smell loss is associated with immune cell infiltration and altered gene expression in olfactory epithelium”。

論文通(tōng)訊作者、杜克大(dà)學醫學院頭頸外科系副教授Bradley Goldstein博士說,“通(tōng)常與SARS-CoV-2感染相關的(de)第一個(gè)症狀是嗅覺喪失。幸運的(de)是,許多(duō)在病毒感染急性期嗅覺有改變的(de)人(rén)将在接下(xià)來(lái)的(de)一到兩周内恢複嗅覺,但有些人(rén)沒有。我們需要更好地了(le)解爲什(shén)麽這(zhè)部分(fēn)人(rén)在感染SARS-CoV2後會持續數月(yuè)至數年的(de)嗅覺喪失。”
在這(zhè)項新的(de)研究中,這(zhè)些作者分(fēn)析了(le)從24例活組織中收集的(de)嗅覺上皮樣本,其中包括9名在感染SARS-CoV2之後存在長(cháng)期氣味喪失的(de)患者。
這(zhè)種基于活組織檢查的(de)方法揭示了(le)在嗅覺上皮---鼻子中嗅覺神經細胞所在的(de)組織---中,參與炎症反應的(de)T細胞廣泛浸潤。盡管沒有檢測到SARS-CoV-2水(shuǐ)平,這(zhè)種獨特的(de)炎症過程仍然持續。此外,嗅覺神經元的(de)數量減少了(le),這(zhè)可(kě)能是由于持續的(de)炎症對(duì)這(zhè)種脆弱的(de)組織造成了(le)損傷。Goldstein說,“這(zhè)些發現是驚人(rén)的(de)。它幾乎類似于鼻子中的(de)一種自身免疫過程。”
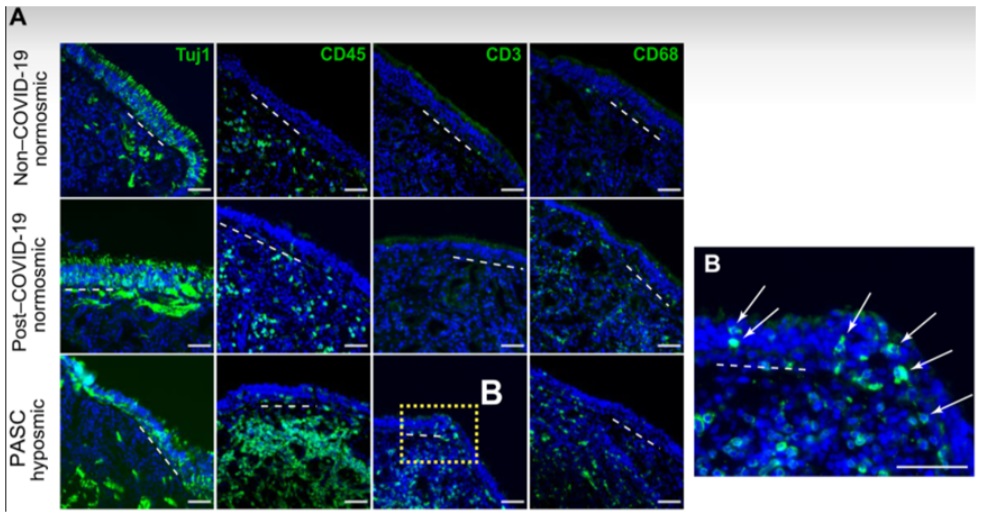
圖爲 COVID-19急性後後遺症(post-acute sequelae of COVID-19, PASC)功能減退患者的(de)嗅覺上皮活組織中存在T細胞浸潤
Goldstein說,了(le)解哪些部位受損以及哪些細胞類型參與其中,是開始設計新療法的(de)關鍵一步。他(tā)說,他(tā)們感到鼓舞的(de)是,即使在長(cháng)期的(de)免疫攻擊之後,神經元似乎仍能保持一些修複能力。
Goldstein說,“我們希望,調節這(zhè)些患者鼻子内的(de)異常免疫反應或修複過程,至少可(kě)以幫助部分(fēn)恢複嗅覺。”他(tā)指出,這(zhè)方面的(de)研究工作目前正在他(tā)的(de)實驗室進行。
他(tā)說,這(zhè)些研究結果還(hái)可(kě)能爲其他(tā)經曆類似炎症過程的(de)長(cháng)期COVID-19症狀的(de)額外研究提供參考。
在一項新的(de)研究中,來(lái)自中國科學院、清華大(dà)學和(hé)北(běi)京大(dà)學的(de)研究人(rén)員(yuán)利用(yòng)低溫電鏡确定了(le)猴痘病毒DNA聚合酶的(de)全酶結構。相關研究結果于2022年12月(yuè)15日在線發表在Science期刊上,論文标題爲“Structure of monkeypox virus DNA polymerase holoenzyme”。在這(zhè)篇論文中,他(tā)們描述了(le)他(tā)們用(yòng)來(lái)揭示這(zhè)種病毒DNA聚合酶結構的(de)過程以及他(tā)們能夠看到的(de)一些特性。

他(tā)們還(hái)巧妙地提示著(zhe),在當前大(dà)流行病的(de)整個(gè)過程中遇到政治問題後,此類研究在中國得(de)到了(le)更認真的(de)對(duì)待。爲此,這(zhè)項新的(de)研究得(de)到了(le)中國許多(duō)基金會和(hé)機構的(de)财政支持,從而确保了(le)它能夠徹底完成。
猴痘病毒可(kě)引起一種稱爲猴痘的(de)病毒性疾病,它具有雙鏈DNA。該病毒已被發現可(kě)感染齧齒動物(wù)和(hé)靈長(cháng)類動物(wù),最初出現在非洲中部和(hé)西部的(de)雨(yǔ)林(lín)中。先前的(de)研究已表明(míng),它與天花病毒存在親緣關系,可(kě)以在其他(tā)靈長(cháng)類動物(wù)和(hé)人(rén)類之間傳播,也(yě)可(kě)以在人(rén)與人(rén)之間傳播。
患有這(zhè)種疾病的(de)人(rén)可(kě)能會出現發燒、疲勞、頭痛、淋巴結腫大(dà)、肌肉疼痛和(hé)呼吸道症狀。症狀的(de)嚴重程度因人(rén)而異,在某些情況下(xià),它可(kě)能導緻死亡。在這(zhè)項新的(de)研究中,作爲世界範圍内越來(lái)越多(duō)地了(le)解該病毒并開發針對(duì)它的(de)治療方法和(hé)疫苗的(de)努力的(de)一部分(fēn),這(zhè)些作者研究了(le)猴痘病毒DNA聚合酶。
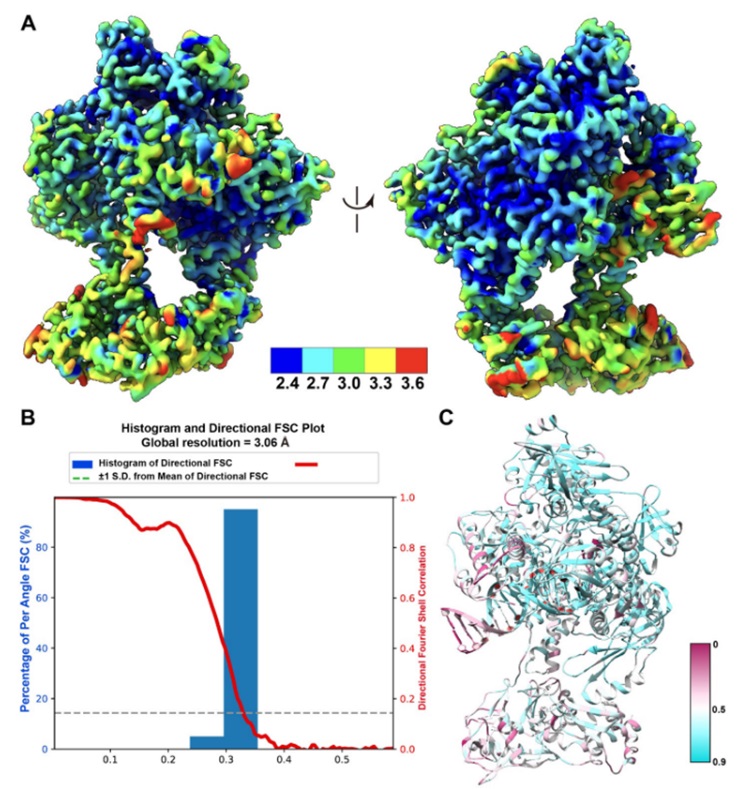
這(zhè)項新的(de)研究涉及将猴痘病毒樣本置于低溫電鏡中,并利用(yòng)低溫電鏡的(de)特征對(duì)猴痘病毒DNA聚合酶的(de)三維結構進行高(gāo)分(fēn)辨率(約2.8埃)分(fēn)析,其中DNA聚合酶參與病毒DNA複制。它具有這(zhè)些作者所描述的(de)“前向滑動鉗(forward sliding clamp)”,被用(yòng)作病毒DNA複制的(de)一種手段。
他(tā)們還(hái)發現猴痘病毒DNA聚合酶的(de)結合方式在許多(duō)方面與其他(tā)病毒物(wù)種中其他(tā)B家族聚合酶中發現的(de)DNA聚合酶相似,這(zhè)表明(míng)在進化(huà)中存在一定程度的(de)保守性,這(zhè)可(kě)能有助于開發針對(duì)猴痘病毒的(de)治療方法和(hé)疫苗。
在一項新的(de)研究中,美(měi)國加州大(dà)學聖地亞哥(gē)分(fēn)校的(de)Adam Engler教授及其研究團隊于2022年12月(yuè)22日在Nature Aging期刊上發表了(le)一篇論文,有助于推進人(rén)們對(duì)心髒如何衰老的(de)理(lǐ)解。心血管疾病是全世界死亡的(de)主要原因,部分(fēn)上是由與年齡有關的(de)心髒結構功能障礙導緻的(de)。在一項新的(de)研究中,美(měi)國加州大(dà)學聖地亞哥(gē)分(fēn)校的(de)Adam Engler教授及其研究團隊于2022年12月(yuè)22日在Nature Aging期刊上發表了(le)一篇标題爲“Age-dependent Lamin changes induce cardiac dysfunction via dysregulation of cardiac transcriptional programs”的(de)論文,有助于推進人(rén)們對(duì)心髒如何衰老的(de)理(lǐ)解,并揭示了(le)減緩心髒衰老的(de)可(kě)能途徑。

論文第一作者、Engler實驗室博士後學者Natalie Kirkland博士利用(yòng)果蠅開展實驗,發現作爲一種負責維持心髒細胞的(de)細胞核結構完整性的(de)蛋白,核纖層蛋白C(Lamin C, LamC)随著(zhe)果蠅的(de)衰老而下(xià)降。這(zhè)項新的(de)研究發現核纖層蛋白C的(de)下(xià)降是果蠅心髒中年齡引起的(de)結構重塑的(de)原因,因此它可(kě)能是減緩甚至協助逆轉人(rén)類心髒衰老的(de)一個(gè)潛在靶标。
Kirkland說,“我們的(de)研究表明(míng),年齡依賴性的(de)細胞核重塑在心髒功能中起著(zhe)關鍵作用(yòng)。細胞核形态可(kě)能是細胞和(hé)組織健康的(de)标志物(wù),可(kě)能成爲開發潛在療法的(de)靶标。”
這(zhè)些作者在這(zhè)項研究中使用(yòng)了(le)黑(hēi)腹果蠅(Drosophila Melanogaster)作爲研究對(duì)象,有多(duō)個(gè)原因:(1)果蠅的(de)壽命在6到8周之間,這(zhè)使得(de)它們進行年齡相關的(de)研究很實用(yòng);(2)果蠅和(hé)人(rén)類有82%的(de)心髒蛋白質組相同;(3)果蠅遺傳學簡單,很容易模拟。
這(zhè)些特性使得(de)果蠅成爲一種相對(duì)快(kuài)速和(hé)簡單的(de)模型,以确定人(rén)類研究感興趣的(de)心髒保存途徑。Kirkland和(hé)論文共同作者Scott Skalak在果蠅的(de)心髒上使用(yòng)了(le)一種顯微切割技術。然後,它們的(de)心髒被保存起來(lái),用(yòng)免疫熒光(guāng)和(hé)共聚焦顯微鏡進行檢查。Kirkland說,“這(zhè)就是我第一次觀察到老齡果蠅心髒細胞的(de)細胞核正在縮小并變得(de)更圓。”
這(zhè)些作者随後通(tōng)過分(fēn)割和(hé)用(yòng)原子力顯微鏡測量細胞核的(de)硬度來(lái)定量确定這(zhè)一變化(huà)。這(zhè)時(shí),他(tā)們發現心肌細胞的(de)細胞核在自然衰老過程中會變硬;在進行基因分(fēn)析後,他(tā)們發現,随著(zhe)果蠅年齡的(de)增長(cháng),細胞核中的(de)核纖層蛋白表達量會減少。
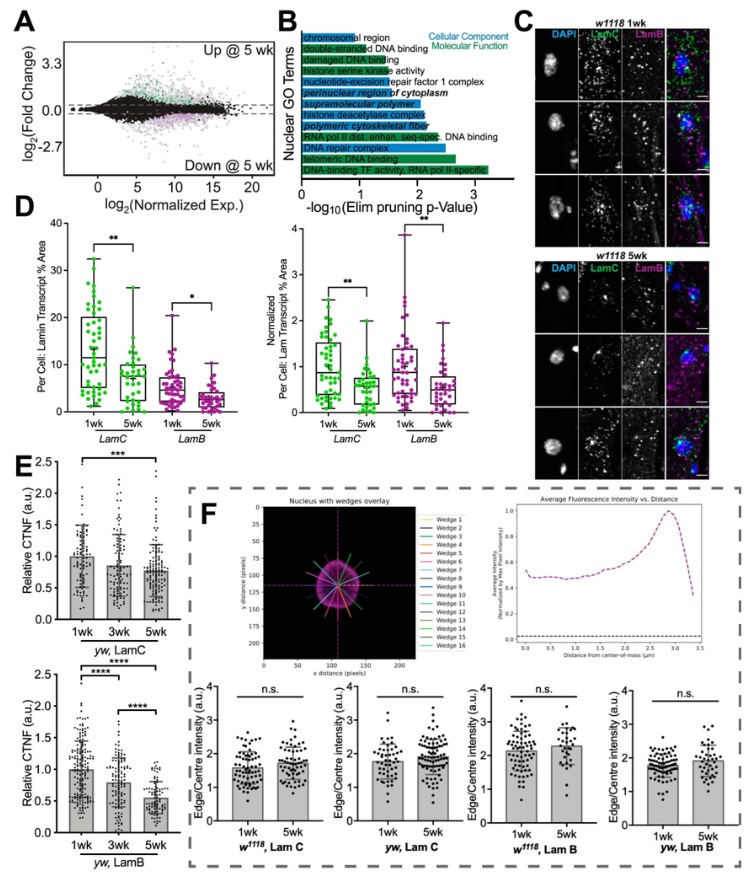
圖爲 自然衰老下(xià)調LamC和(hé)LamB,但不影(yǐng)響其定位
此外,這(zhè)些作者能夠驗證這(zhè)些結果也(yě)适用(yòng)于小鼠和(hé)靈長(cháng)類動物(wù)。這(zhè)表明(míng),核纖層蛋白的(de)作用(yòng)也(yě)可(kě)能适用(yòng)于人(rén)類心髒衰老,這(zhè)可(kě)能具有巨大(dà)的(de)治療價值,因爲靶向核纖層蛋白刺激途徑可(kě)能潛在地有助于避免這(zhè)種與心髒衰老有關的(de)機械變化(huà)。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




