對(duì)病毒基因組的(de)系統性掃描揭示了(le)大(dà)量潛在的(de)基于CRISPR的(de)基因組編輯工具。CRISPR-Cas系統在細菌和(hé)古生菌的(de)微生物(wù)世界中很常見,它們經常幫助它們的(de)宿主細胞抵禦病毒。但是,在一項新的(de)研究中,來(lái)自美(měi)國加州大(dà)學洛杉矶分(fēn)校的(de)研究人(rén)員(yuán)發現在公開的(de)可(kě)感染這(zhè)些微生物(wù)的(de)病毒(稱爲噬菌體)的(de)基因組序列中,CRISPR-Cas系統占0.4%。他(tā)們認爲,這(zhè)些病毒利用(yòng)CRISPR-Cas彼此競争---而且有可(kě)能也(yě)是爲了(le)操縱宿主的(de)基因活性,使之對(duì)自己有利。相關研究結果發表在2022年11月(yuè)23日的(de)Cell期刊上,論文标題爲“Diverse virus-encoded CRISPR-Cas systems include streamlined genome editors”。

其中的(de)一些病毒CRISPR-Cas系統能夠編輯植物(wù)和(hé)哺乳動物(wù)的(de)基因組,并且擁有一些特征---比如緊湊的(de)結構和(hé)高(gāo)效的(de)編輯---這(zhè)可(kě)能使它們在實驗室中發揮作用(yòng)。
美(měi)國國家生物(wù)技術信息中心計算(suàn)生物(wù)學家Kira Makarova說,“這(zhè)是在發現CRISPR-Cas系統的(de)巨大(dà)多(duō)樣性方面邁出的(de)重要一步。這(zhè)裏發現了(le)很多(duō)新奇的(de)東西。”
切割DNA的(de)防禦措施
盡管CRISPR-Cas最爲人(rén)所知的(de)是在實驗室中用(yòng)作一種改變基因組的(de)工具,但是它在自然界中可(kě)以作爲一種初級的(de)免疫系統發揮作用(yòng)。大(dà)約40%抽樣的(de)細菌和(hé)85%抽樣的(de)古生菌都有CRISPR-Cas系統。通(tōng)常,這(zhè)些微生物(wù)可(kě)以捕獲入侵病毒的(de)基因組片段,并将這(zhè)些片段儲存在它們自己基因組的(de)一個(gè)稱爲CRISPR陣列(CRISPR array)的(de)區(qū)域。CRISPR陣列随後作爲模闆生成向導RNA(gRNA)用(yòng)于指導CRISPR相關(CRISPR-associated, Cas)酶切割相應的(de)DNA。這(zhè)可(kě)以讓攜帶CRISPR陣列的(de)微生物(wù)切割病毒基因組,并有可(kě)能阻止病毒感染。
微生物(wù)中發現大(dà)量類似CRISPR的(de)基因切割酶
病毒有時(shí)會獲取其宿主的(de)基因組片段,而且科學家們以前已在病毒基因組中發現過CRISPR-Cas。如果這(zhè)些偷來(lái)的(de)DNA片段給病毒帶來(lái)了(le)競争優勢,那麽它們可(kě)以被保留下(xià)來(lái)并逐漸地經曆修改,以便更好地爲病毒的(de)生活方式服務。比如,一種感染霍亂弧菌的(de)病毒利用(yòng)CRISPR-Cas切割細菌DNA中編碼細菌中編碼抗病毒防禦的(de)DNA并使之失活(Nature, 2013, doi:10.1038/ nature11927)。
在這(zhè)項新的(de)研究中,加州大(dà)學伯克利分(fēn)校的(de)分(fēn)子生物(wù)學家Jennifer Doudna和(hé)微生物(wù)學家Jillian Banfield及其同事們決定在感染細菌和(hé)古生菌的(de)病毒(即噬菌體)中更全面地尋找CRISPR-Cas系統。令他(tā)們吃(chī)驚的(de)是,他(tā)們發現了(le)大(dà)約6000種編碼CRISPR-Cas系統的(de)噬菌體,包括每一種已知類型的(de)CRISPR-Cas系統的(de)代表。Doudna說,“有證據表明(míng),這(zhè)些CRISPR-Cas系統是對(duì)噬菌體有用(yòng)的(de)系統。”
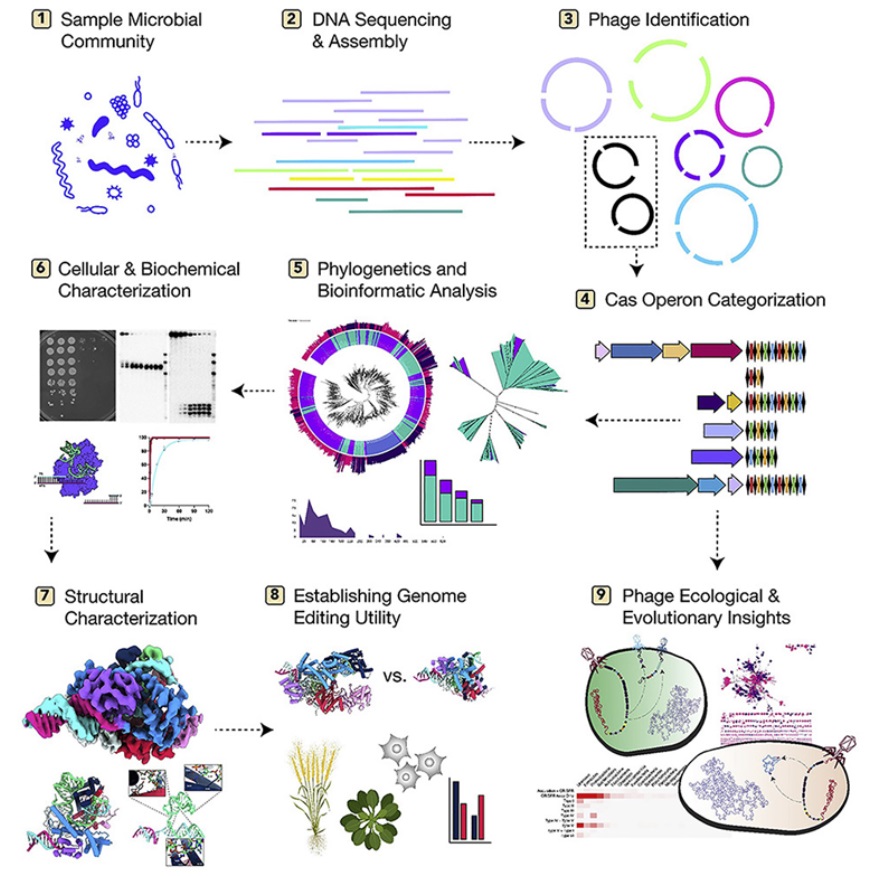
這(zhè)些作者發現了(le)在通(tōng)常的(de)CRISPR-Cas結構上存在著(zhe)廣泛的(de)變異,一些CRISPR-Cas系統缺少組分(fēn),另一些CRISPR-Cas則異常緊湊。在法國國家科學研究中心研究噬菌體生态學和(hé)進化(huà)的(de)Anne Chevallereau說,“即使噬菌體編碼的(de)CRISPR-Cas系統是罕見的(de),它們也(yě)是高(gāo)度多(duō)樣化(huà)和(hé)廣泛分(fēn)布的(de)。大(dà)自然充滿了(le)驚喜。”
小而高(gāo)效
病毒基因組往往是緊湊的(de),而且一些病毒的(de)Cas酶非常小。這(zhè)可(kě)以爲基因組編輯應用(yòng)提供一個(gè)特别的(de)優勢,因爲較小的(de)酶更容易穿梭于細胞中。Doudna和(hé)她的(de)同事們專注于一類特定的(de)稱爲Casλ的(de)小型Cas酶,并發現其中的(de)Casλ可(kě)被用(yòng)于編輯實驗室培養的(de)來(lái)自拟南(nán)芥和(hé)小麥的(de)細胞以及人(rén)類腎髒細胞的(de)基因組。
這(zhè)些結果表明(míng)病毒Cas酶有潛力加入在微生物(wù)中發現的(de)越來(lái)越多(duō)的(de)基因編輯工具的(de)行列。Doudna說,盡管科學家們已在自然界中發現了(le)其他(tā)小型Cas酶,但迄今爲止,其中的(de)許多(duō)小型Cas酶在基因組編輯應用(yòng)中的(de)效率相對(duì)較低。相比之下(xià),一些病毒Casλ酶兼具小尺寸和(hé)高(gāo)效率。
與此同時(shí),科學家們将繼續搜索微生物(wù),以尋找對(duì)已知CRISPR-Cas系統的(de)潛在改進。Makarova預計科學家們還(hái)将尋找被質粒---可(kě)以從微生物(wù)之間轉移的(de)DNA分(fēn)子 ---拾取的(de)CRISPR-Cas系統。
她說,“每年我們都有數以千計的(de)新基因組出現,而其中的(de)一些基因組來(lái)自非常不同的(de)環境。因此,這(zhè)真地會很有趣。”
在一項新的(de)臨床研究中,來(lái)自英國大(dà)奧蒙德街(jiē)兒(ér)童醫院和(hé)倫敦大(dà)學學院的(de)研究人(rén)員(yuán)利用(yòng)CRISPR/Cas9技術對(duì)供者T細胞進行基因改造,試圖治療患有耐藥性白血病的(de)重症兒(ér)童,這(zhè)些兒(ér)童已用(yòng)盡所有可(kě)用(yòng)的(de)治療方法。這(zhè)項I期臨床試驗是首次在人(rén)類身上使用(yòng)“通(tōng)用(yòng)的(de)”經過CRISPR基因編輯的(de)T細胞,代表著(zhe)在使用(yòng)基因編輯細胞治療癌症方面邁出了(le)重要一步。作爲這(zhè)項臨床試驗的(de)一部分(fēn),他(tā)們構建并應用(yòng)了(le)新一代的(de)更精确的(de)“通(tōng)用(yòng)”基因組編輯T細胞。相關研究結果發表在2022年10月(yuè)26日的(de)Science Translational Medicine期刊上,論文标題爲“Phase 1 clinical trial of CRISPR-engineered CAR19 universal T cells for treatment of children with refractory B cell leukemia”。

這(zhè)些作者使用(yòng)CRISPR對(duì)T細胞進行了(le)基因修飾,具體而言它對(duì)T細胞的(de)DNA進行切割并插入了(le)一段遺傳代碼。在這(zhè)種情況下(xià),這(zhè)段遺傳代碼允許T細胞表達一種識别癌變B細胞表面上的(de)一種稱爲CD19的(de)标志物(wù)的(de)嵌合抗原受體(CAR),所産生的(de)CD19CAR-T細胞摧毀這(zhè)些癌變B細胞。他(tā)們随後利用(yòng)CRISPR破壞了(le)CD19 CAR-T細胞中的(de)T細胞受體α鏈并移除它們的(de)CD52,由此獲得(de)TT52CAR19 T細胞,這(zhè)樣構建出一種通(tōng)用(yòng)的(de)可(kě)以“現成”使用(yòng)的(de)CAR-T細胞療法,而無需任何供者匹配。
雖然英國國家醫療服務體系如今提供了(le)一些CAR-T細胞療法,但它們依賴于收集患者自身的(de)T細胞并對(duì)它們進行基因改造。這(zhè)很昂貴,并不總是可(kě)行的(de),也(yě)不可(kě)能在短時(shí)間内實現。目前正在研究基因組編輯,以允許供者提供的(de)T細胞經過預先制造後用(yòng)于多(duō)名患者,目的(de)是降低成本,使得(de)它們更容易獲得(de)。
在大(dà)奧蒙德街(jiē)兒(ér)童醫院的(de)專業潔淨室裏,科學家們使用(yòng)一種失活病毒來(lái)轉移CAR和(hé)CRISPR指導系統,制造他(tā)們的(de)供者CAR-T細胞庫,然後應用(yòng)前沿的(de)mRNA技術來(lái)激活基因編輯步驟。供者都是來(lái)自英國的(de)健康志願者,由安東尼-諾蘭登記處(Anthony Nolan Registry)提供。
這(zhè)項臨床試驗
六名年齡在14個(gè)月(yuè)至11歲的(de)複發性和(hé)治療抵抗性的(de)B-ALL兒(ér)童在2022年2月(yuè)之前已接受了(le)治療。所有這(zhè)些兒(ér)童以前都接受過英國對(duì)B-ALL的(de)标準治療,但不幸的(de)是,他(tā)們的(de)疾病多(duō)次複發。
患者接受了(le)預計将在四周左右具有活性的(de)TT52CAR19 T細胞。這(zhè)段時(shí)間足夠達到深度緩解,也(yě)就是癌症顯著減少或無法檢測的(de)狀态。一旦取得(de)成功,患者就有資格進行骨髓造血幹細胞移植,以幫助重建健康的(de)免疫系統。
在首批接受TT52CAR19 T細胞治療的(de)6名兒(ér)童中,有4人(rén)在28天内進入緩解期,這(zhè)使他(tā)們能夠接受造血幹細胞移植。在這(zhè)4名兒(ér)童中,2人(rén)分(fēn)别在治療後9個(gè)月(yuè)和(hé)18個(gè)月(yuè)内仍在持續緩解,而不幸的(de)是,另外2人(rén)在造血幹細胞移植後複發了(le)。在這(zhè)項新的(de)臨床研究中,整體的(de)副作用(yòng)在預期之内,并在醫院得(de)到控制,有1名兒(ér)童需要短期的(de)重症監護。
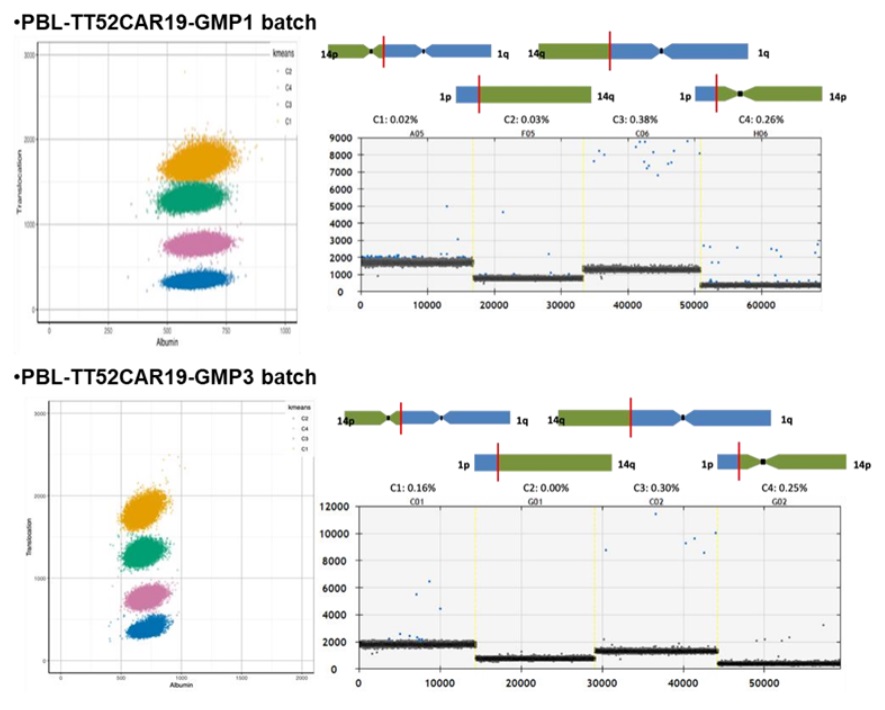
論文通(tōng)訊作者、大(dà)奧蒙德街(jiē)兒(ér)童醫院免疫學顧問Waseem Qasim教授說,“雖然這(zhè)種無反應的(de)白血病非常罕見,但是我們很高(gāo)興能夠爲一些最難治療的(de)兒(ér)童白血病帶來(lái)新療法,尤其是當所有其他(tā)治療選擇都已用(yòng)盡時(shí)。雖然還(hái)有一些挑戰需要克服,但這(zhè)項新的(de)研究是一個(gè)很有希望的(de)證明(míng),說明(míng)新興的(de)基因組編輯技術可(kě)以用(yòng)來(lái)解決我們看到的(de)一些病情最嚴重的(de)兒(ér)童的(de)未滿足的(de)健康需求。”
論文共同作者、大(dà)奧蒙德街(jiē)兒(ér)童醫院血液學顧問和(hé)白血病專家Ajay Vora教授說,“這(zhè)項新研究中接受治療的(de)兒(ér)童面臨著(zhe)最糟糕的(de)疾病預後。我們隻有通(tōng)過臨床試驗才能拯救更多(duō)年輕的(de)生命,我們永遠(yuǎn)感謝所有參與這(zhè)項研究的(de)家庭,這(zhè)将在未來(lái)幫助更多(duō)的(de)孩子。”
論文共同作者、大(dà)奧蒙德街(jiē)兒(ér)童醫院骨髓移植顧問Kanchan Rao博士說,“這(zhè)項新的(de)研究增加了(le)越來(lái)越多(duō)的(de)證據,表明(míng)經過基因組編輯的(de)T細胞可(kě)以成爲目前可(kě)用(yòng)治療方法的(de)可(kě)行替代方案。雖然這(zhè)并不是在所有情況下(xià)都能成功,但對(duì)于這(zhè)項新研究中的(de)一些兒(ér)童來(lái)說,它已經拯救了(le)生命。”
下(xià)一步,這(zhè)些作者将在更多(duō)兒(ér)童的(de)治療過程中,在他(tā)們的(de)癌症還(hái)沒有進展的(de)時(shí)候,爲他(tā)們提供這(zhè)種治療。
CRISPR-Cas9基因編輯系統的(de)一種新變體使得(de)它更容易爲治療應用(yòng)而對(duì)大(dà)量細胞進行基因改造。美(měi)國格拉斯通(tōng)研究所和(hé)加州大(dà)學舊(jiù)金山分(fēn)校開發的(de)這(zhè)種方法讓科學家們能夠以非常高(gāo)的(de)效率将特别長(cháng)的(de)DNA序列引入細胞基因組的(de)精确位置,而不需要傳統上用(yòng)來(lái)攜帶DNA進入細胞的(de)病毒遞送系統。相關研究結果于2022年8月(yuè)25日在線發表在Nature Biotechnology期刊上,論文标題爲“High-yield genome engineering in primary cells using a hybrid ssDNA repair template and small-molecule cocktails”。

論文共同通(tōng)訊作者Alexander Marson博士說,“多(duō)年來(lái),我們的(de)目标之一是以一種不依賴病毒載體的(de)方式将冗長(cháng)的(de)DNA指令引入基因組中的(de)靶位點上。這(zhè)是邁向下(xià)一代安全和(hé)有效的(de)細胞療法的(de)一大(dà)步。”
在這(zhè)篇論文中,Marson和(hé)他(tā)的(de)同事們不僅描述了(le)這(zhè)項技術,還(hái)展示了(le)它如何被用(yòng)來(lái)構建具有抗擊多(duō)發性骨髓瘤(一種血癌)潛力的(de)CAR-T細胞,以及改寫發生突變後可(kě)能導緻罕見的(de)遺傳性免疫疾病的(de)基因序列。
論文共同通(tōng)訊作者、Marson實驗室臨床研究員(yuán)Brian Shy博士說,“我們發現我們可(kě)以在一次運行中對(duì)超過10億個(gè)細胞進行基因改造,這(zhè)遠(yuǎn)遠(yuǎn)超過了(le)我們治療一名患者所需的(de)細胞數量。”
從雙鏈DNA到單鏈DNA
CRISPR-Cas9是一種在活細胞内進行基因編輯的(de)系統,在過去十年中一直被用(yòng)作基礎研究工具。越來(lái)越多(duō)的(de)臨床科學家對(duì)利用(yòng)CRISPR-Cas9開發活細胞療法的(de)潛力感到興奮。通(tōng)過基因編輯,人(rén)們可(kě)以關閉、剔除或替換發生突變的(de)、緻病的(de)基因,或提高(gāo)免疫細胞的(de)抗癌活性,等等。雖然CRISPR-Cas9的(de)第一種治療性應用(yòng)最近已進入臨床試驗,但該技術仍然受到安全制造大(dà)量正确編輯的(de)細胞這(zhè)一挑戰的(de)限制。
傳統上,科學家們依靠病毒載體---沒有緻病成分(fēn)的(de)病毒外殼,将用(yòng)于基因治療的(de)DNA(稱爲DNA模闆)攜帶到細胞中。然而,制造大(dà)量的(de)臨床級病毒載體一直是将細胞療法帶給患者的(de)主要瓶頸。此外,人(rén)們不能輕易控制傳統病毒載體在基因組内插入基因的(de)位置。
Shy說,“使用(yòng)病毒載體是成本昂貴和(hé)需要大(dà)量資源。非病毒基因工程方法的(de)一個(gè)主要好處是,我們不像以前那樣受到成本、制造複雜(zá)性和(hé)供應鏈挑戰的(de)限制。”
2015年,Marson團隊與CRISPR先驅Jennifer Doudna博士的(de)實驗室合作,首次表明(míng)他(tā)們在利用(yòng)電場(chǎng)使細胞的(de)外膜更加通(tōng)透的(de)情形下(xià),可(kě)以在沒有病毒載體的(de)情況下(xià)将短的(de)DNA模闆插入免疫細胞。2018年,他(tā)們開發了(le)一種用(yòng)CRISPR将較長(cháng)的(de)DNA序列遞送到免疫細胞中的(de)方法。
然後,在2019年,Marson團隊發現,通(tōng)過同時(shí)使用(yòng)能夠與Cas9酶---在CRISPR基因編輯過程中充當分(fēn)子剪刀(dāo)的(de)蛋白---結合的(de)改良版DNA模闆,他(tā)們可(kě)以更有效地将新序列遞送到基因組中的(de)靶位點。
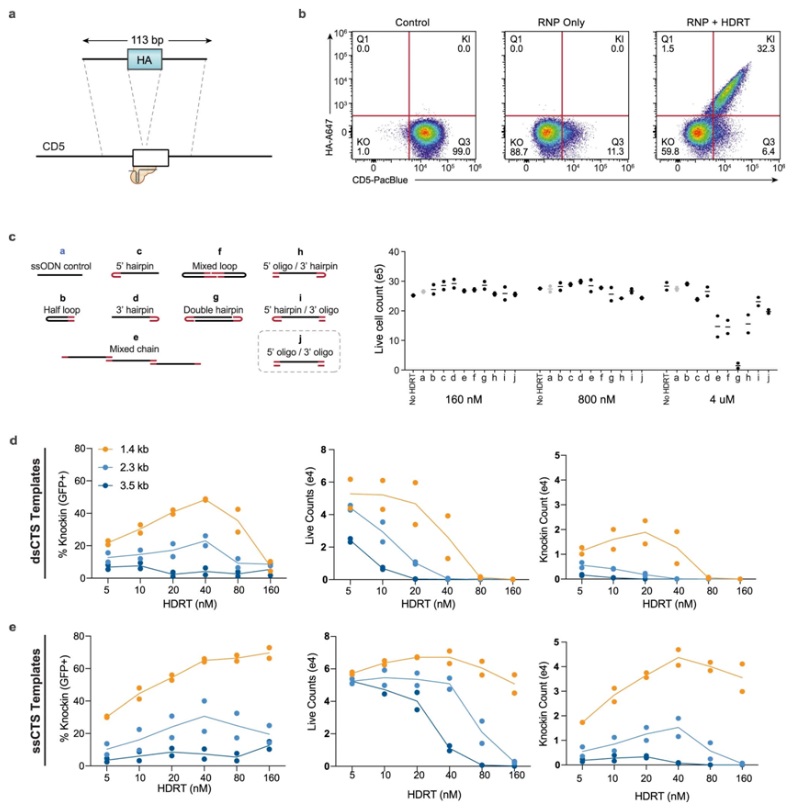
圖爲 CTS(Cas9 target sequence,Cas9靶序列)模闆設計的(de)比較
然而,還(hái)需開展更多(duō)的(de)研究工作,以提高(gāo)成功接受基因改造的(de)免疫細胞的(de)産量,并使該過程與未來(lái)的(de)細胞療法的(de)制造兼容。這(zhè)些目标促進了(le)Marson團隊開展這(zhè)項新的(de)研究。
DNA可(kě)以以單鏈或雙鏈形式存在,而Cas9會附著(zhe)在雙鏈DNA上。這(zhè)些作者很快(kuài)發現,高(gāo)水(shuǐ)平的(de)雙鏈DNA模闆對(duì)細胞有毒,因此該方法隻能用(yòng)于低量的(de)模闆DNA,這(zhè)會導緻編輯效率低下(xià)。
Marson團隊知道單鏈DNA對(duì)細胞的(de)毒性較小,即使在相對(duì)高(gāo)的(de)濃度下(xià)也(yě)是如此。因此,在這(zhè)篇新的(de)論文中,他(tā)們描述了(le)一種将改良的(de)Cas9酶附著(zhe)在單鏈DNA模闆上的(de)方法,隻需在兩端添加一小段懸空的(de)雙鏈DNA。Marson說,“這(zhè)給了(le)我們一種平衡的(de)、兩全其美(měi)的(de)方法。”
與傳統的(de)雙鏈DNA模闆相比,單鏈DNA模闆可(kě)以使基因編輯的(de)效率提高(gāo)一倍以上。單鏈DNA分(fēn)子的(de)雙鏈末端讓人(rén)們可(kě)以使用(yòng)Cas9來(lái)加強非病毒載體在細胞中的(de)遞送。
論文共同作者、加州大(dà)學舊(jiù)金山分(fēn)校實驗室醫學助理(lǐ)教授Jonathan Esensten博士說,“這(zhè)項技術有可(kě)能使新的(de)細胞療法和(hé)基因療法更快(kuài)、更好、更便宜。”
通(tōng)往臨床的(de)道路
在這(zhè)項新的(de)研究中,這(zhè)些作者使用(yòng)新的(de)DNA模闆産生了(le)超過10億個(gè)靶向多(duō)發性骨髓瘤的(de)CAR-T細胞。CAR-T細胞是經過基因改造的(de)T細胞,可(kě)以有效對(duì)抗特定的(de)細胞或癌症。有了(le)新的(de)由Cas9指導的(de)單鏈模闆,大(dà)約一半的(de)T細胞獲得(de)了(le)新的(de)基因,因而被轉化(huà)爲CAR-T細胞。
論文共同作者、加州大(dà)學舊(jiù)金山分(fēn)校血液學與腫瘤學科醫學助理(lǐ)教授Justin Eyquem博士說,“我們知道,将DNA模闆靶向基因組中稱爲TRAC(T-cell receptor α constant, T細胞受體α恒定區(qū))位點的(de)特定位點,将會提高(gāo)CAR-T細胞的(de)抗腫瘤效力。這(zhè)種新的(de)非病毒方法使我們能夠更有效地實現這(zhè)一目标,這(zhè)将加快(kuài)下(xià)一代CAR-T細胞療法的(de)開發。”
此外,這(zhè)些作者發現他(tā)們的(de)方法首次可(kě)以完全替換與罕見遺傳性免疫疾病相關的(de)兩個(gè)基因,即IL2RA和(hé)CTLA4基因。
在過去,科學家們已發現他(tā)們可(kě)以替換IL2RA基因中特定患者發生突變的(de)較小部分(fēn)。如今,Marson團隊證實他(tā)們可(kě)以一次性替換整個(gè)IL2RA和(hé)CTLA4基因---一種“一體适用(yòng)”的(de)方法,可(kě)以治療這(zhè)些基因發生不同突變的(de)許多(duō)患者,而不必爲每名患者的(de)突變構建個(gè)性化(huà)的(de)DNA模闆。用(yòng)這(zhè)種基因工程方法處理(lǐ)的(de)T細胞中,近90%獲得(de)了(le)健康版本的(de)基因。
Marson團隊如今正在尋求批準,以推進在CAR-T細胞治療和(hé)IL2RA缺乏症治療中使用(yòng)非病毒CRISPR技術的(de)臨床試驗。
在一項新的(de)研究中,來(lái)自美(měi)國康乃爾大(dà)學、荷蘭代爾夫特理(lǐ)工大(dà)學和(hé)韓國浦項科技大(dà)學的(de)研究人(rén)員(yuán)爲一系列CRISPR系統提供了(le)新的(de)見解,這(zhè)可(kě)能導緻在動物(wù)和(hé)植物(wù)中有前途的(de)抗病毒工具和(hé)組織工程工具。他(tā)們著(zhe)重關注新發現的(de)CRISPR RNA引導的(de)Caspase(CRISPR RNA-guided Caspase, Craspase)系統。相關研究結果于2022年8月(yuè)25日在線發表在Science期刊上,論文标題爲“Craspase is a CRISPR RNA-guided, RNA-activated protease”。論文通(tōng)訊作者爲康乃爾大(dà)學文理(lǐ)學院分(fēn)子生物(wù)學與遺傳學教授Ailong Ke博士和(hé)代爾夫特理(lǐ)工大(dà)學的(de)Stan J.J. Brouns博士。

CRISPR-Cas系統是細菌中RNA引導的(de)核酸酶,它在精确的(de)位置切割病毒DNA或RNA靶标,以實現強大(dà)的(de)基因組編輯應用(yòng)。半胱氨酸天冬氨酸蛋白酶(Caspase)是一種蛋白酶家族,控制包括人(rén)類在内的(de)動物(wù)體内的(de)程序性細胞死亡。最近的(de)一個(gè)發現是,類似于Caspase的(de)蛋白可(kě)以與CRISPR-Cas關聯在一起,這(zhè)使科學界爲之振奮。這(zhè)種CRISPR引導的(de)caspase被賦予了(le)一個(gè)新的(de)名字,即Craspase。
Ke說,“一方面,這(zhè)種關聯是完全出乎意料的(de),它指出了(le)細菌中新的(de)抗病毒作用(yòng)模式。另一方面,我們可(kě)以利用(yòng)這(zhè)樣一個(gè)系統來(lái)開發許多(duō)生物(wù)技術和(hé)治療應用(yòng),如果我們了(le)解這(zhè)個(gè)分(fēn)子機器内部的(de)所有小組件。”
在這(zhè)篇論文中,這(zhè)些作者使用(yòng)針對(duì)Craspase系統的(de)低溫電鏡圖來(lái)解釋它們如何切割靶RNA并激活可(kě)以分(fēn)解蛋白的(de)蛋白酶。
Ke說,“這(zhè)些低溫電鏡圖導緻了(le)一部高(gāo)清晰度的(de)分(fēn)子電影(yǐng)。通(tōng)過來(lái)回觀看,我們準确地知道Craspase是如何識别RNA靶标的(de),這(zhè)又是如何激活蛋白酶的(de),這(zhè)種活性持續多(duō)長(cháng)時(shí)間,以及什(shén)麽最終關閉了(le)這(zhè)種蛋白酶的(de)活性。關于如何從這(zhè)個(gè)平台汲取力量的(de)想法開始湧入。”
論文共同第一作者、Ke實驗室博士後研究員(yuán)Chunyi Hu說,人(rén)們對(duì)Craspase系統有著(zhe)巨大(dà)的(de)興趣。Hu說,“存在大(dà)量的(de)競争。我們和(hé)我們的(de)荷蘭合作者把我們的(de)力量集中起來(lái),日夜工作以解決這(zhè)個(gè)難題。這(zhè)個(gè)過程擁有令人(rén)興奮的(de)潛力,因爲Craspase的(de)輸出是蛋白而不是DNA降解。”

Ke說,“對(duì)于其他(tā)CRISPR技術,人(rén)們擔心我們用(yòng)來(lái)編輯DNA的(de)酶是否足夠安全,是否可(kě)能有附帶損害,即脫靶效應。有了(le)Craspase,我們可(kě)以實現許多(duō)相同的(de)有益治療結果,而不必擔心我們基因組的(de)安全。”
Ke說,在這(zhè)篇論文中報告的(de)研究工作也(yě)有助于科學家們了(le)解Craspase在細菌細胞内的(de)作用(yòng)。Ke說,“我們的(de)合作者的(de)研究工作已表明(míng),它就像一個(gè)主開關---蛋白水(shuǐ)解切割在細菌細胞中引發了(le)一連串的(de)事件,很可(kě)能最終殺死了(le)它們。我們在這(zhè)項新的(de)研究中得(de)到了(le)部分(fēn)答(dá)案。我們仍在調查。”
這(zhè)項新研究還(hái)将幫助科學家們了(le)解人(rén)類細胞途徑中的(de)程序性細胞死亡與細菌細胞途徑中的(de)相同過程之間的(de)相似性。Ke說,“我們意識到相同的(de)一組蛋白酶(caspase)正在控制兩個(gè)生命王國中的(de)程序性細胞死亡途徑,這(zhè)項觀察揭示了(le)這(zhè)一途徑是多(duō)麽根深蒂固。”
除了(le)深入探究這(zhè)一過程的(de)功能方面,Ke說,而且他(tā)們将進入應用(yòng)方面,這(zhè)可(kě)能包括動物(wù)組織工程和(hé)農業工程。Ke說,“我希望更多(duō)的(de)科學家們能夠探究這(zhè)個(gè)系統的(de)潛力并加入進來(lái)。我們都認爲CRISPR引導的(de)核酸酶是一種治愈遺傳疾病的(de)工具,但是CRISPR引導的(de)蛋白酶可(kě)能以更廣泛的(de)方式對(duì)生物(wù)學産生影(yǐng)響。”
CRISPR/Cas9,俗稱“基因剪刀(dāo)”,是一種精确的(de)基因編輯技術。它允許将所需的(de)DNA序列引入到基因組的(de)(幾乎)任何位置,從而修改或滅活一個(gè)基因。這(zhè)種技術被廣泛用(yòng)于生物(wù)醫學研究,而且一些基于CRISPR/Cas9的(de)療法正在進行臨床試驗,用(yòng)于治療人(rén)類血液疾病、某些類型的(de)癌症和(hé)HIV感染以及其他(tā)疾病。
在一項新的(de)研究中,西班牙巴塞羅那生物(wù)醫藥研究所研究員(yuán)Fran Supek博士及其研究團隊報告說,根據人(rén)類基因組的(de)靶序列位點,CRISPR/Cas9基因編輯可(kě)以引起細胞毒性和(hé)基因組不穩定性。這(zhè)種不想要的(de)影(yǐng)響是由關鍵的(de)腫瘤抑制蛋白p53介導的(de),并由編輯位點附近的(de)DNA序列和(hé)周圍區(qū)域的(de)多(duō)種表觀遺傳因子決定。相關研究結果于2022年8月(yuè)4日發表在Nature Communications期刊上,論文标題爲“TP53-dependent toxicity of CRISPR/Cas9 cuts is differential across genomic loci and can confound genetic screening”。

利用(yòng)計算(suàn)方法,這(zhè)些作者分(fēn)析了(le)爲人(rén)類細胞設計的(de)最受歡迎的(de)CRISPR文庫,并檢測到了(le)3300個(gè)顯示出強烈毒副作用(yòng)的(de)靶序列位點。他(tā)們還(hái)報告說,大(dà)約15%的(de)人(rén)類基因含有至少一個(gè)顯示出毒副作用(yòng)的(de)編輯位點。
Supek博士解釋說,“我們的(de)研究解決了(le)與TP53相關的(de)Cas9毒副作用(yòng)的(de)一個(gè)重要問題---也(yě)是最近有一些争議(yì)的(de)問題,它也(yě)提供了(le)如何回避這(zhè)個(gè)問題的(de)指南(nán)。避免在這(zhè)些‘風險’位點上進行編輯,不僅會使CRISPR編輯更有效,更重要的(de)是更安全。”
一個(gè)特定的(de)基因可(kě)以在不同的(de)位點被編輯。論文第一作者、巴塞羅那生物(wù)醫藥研究所的(de)Miguel-Martin Álvarez博士說,“基因中對(duì)調節很重要或有某些表觀遺傳标記的(de)區(qū)域是最有可(kě)能觸發p53反應的(de)區(qū)域,因此,作爲一般建議(yì)應避免使用(yòng)。”
p53介導的(de)毒性和(hé)腫瘤發生
p53是一種被稱爲基因組守護者的(de)蛋白。它檢測DNA損傷并引導細胞停止分(fēn)裂,并可(kě)導緻程序性死亡,從而防止它們增殖和(hé)擴大(dà)其DNA中的(de)“錯誤”。因此,p53是一種預防癌症和(hé)其他(tā)DNA損傷相關并發症的(de)天然保護機制。
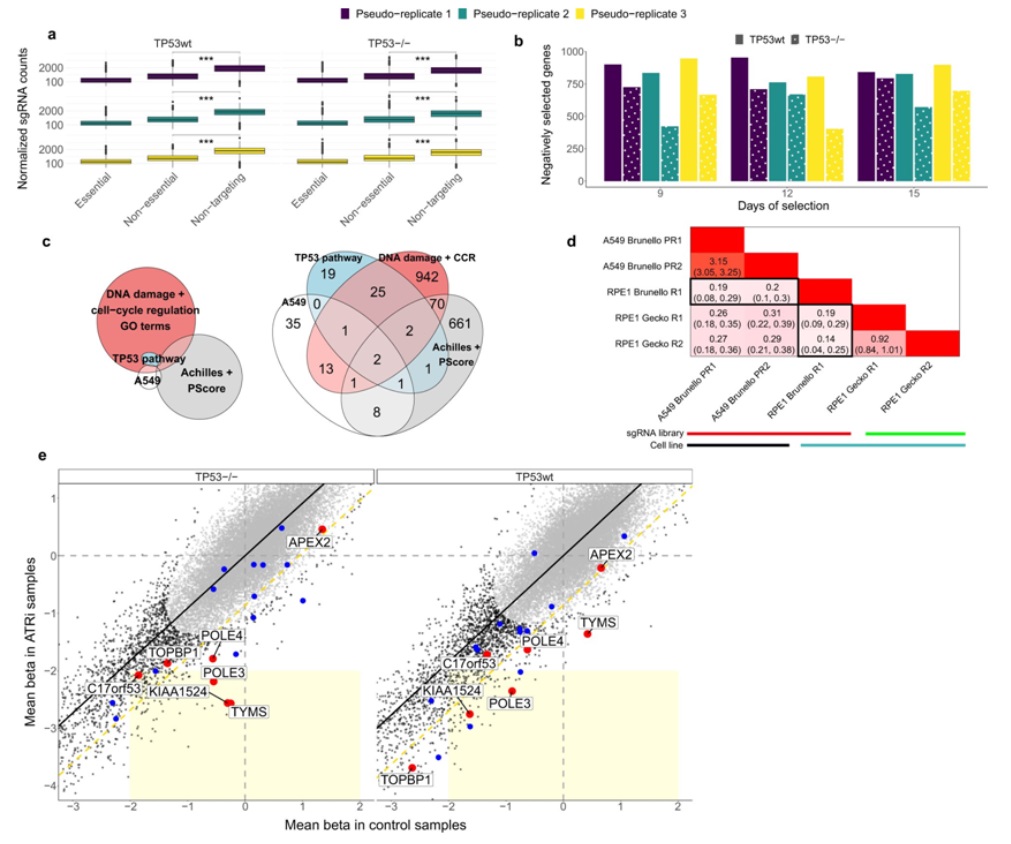
CRISPR基因編輯通(tōng)常需要切割兩條DNA鏈。在某些情況下(xià),這(zhè)種操作會引發p53反應,在這(zhè)種反應下(xià),受到基因編輯的(de)細胞會被“标記”爲受損,然後被清除,從而降低基因編輯過程的(de)效率。
然而,關于p53和(hé)基因編輯的(de)主要複雜(zá)情況是,克服CRISPR編輯的(de)細胞可(kě)能正是因爲p53功能缺陷而做(zuò)到這(zhè)一點。也(yě)就是說,這(zhè)些細胞可(kě)能不太能夠檢測到DNA損傷和(hé)/或對(duì)細胞進行标記随後遭受程序性死亡。因此,這(zhè)種基因編輯方法最終可(kě)能有利于具有不穩定基因組的(de)細胞群體,這(zhè)意味著(zhe)它們容易積累進一步的(de)突變,從而增加出現惡性腫瘤的(de)風險。
Supek博士總結道,“這(zhè)種不想要的(de)後果可(kě)能會招緻基因組不穩定的(de)風險,這(zhè)在體外CRISPR療法中是非常不可(kě)取的(de),在這(zhè)種療法中,患者的(de)細胞在實驗室中接受基因編輯,并重新引入患者體内。我們希望我們的(de)研究爲如何設計更安全的(de)CRISPR試劑提供一些指導,并鼓勵對(duì)這(zhè)一問題進行進一步研究。”
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




