随著(zhe)科學家們對(duì)人(rén)類免疫系統的(de)動态内部世界有了(le)新的(de)認識,越來(lái)越清楚的(de)是,線粒體在我們身體如何應對(duì)疾病中起著(zhe)關鍵調節作用(yòng)。除了(le)作爲“細胞能量工廠”的(de)傳統作用(yòng)之外,線粒體還(hái)在細胞的(de)生存---更重要的(de)是,在細胞的(de)死亡---中扮演著(zhe)引導炎症和(hé)抗微生物(wù)防禦的(de)關鍵作用(yòng)。這(zhè)意味著(zhe)線粒體相關基因的(de)突變可(kě)能影(yǐng)響免疫系統抵禦疾病的(de)能力,甚至引發過度反應,導緻癌症或克羅恩病等炎症性疾病。
盡管人(rén)們對(duì)線粒體調節免疫系統的(de)作用(yòng)有了(le)越來(lái)越多(duō)的(de)了(le)解,但它們是如何做(zuò)到這(zhè)一點的(de),仍然相對(duì)未知。弄清線粒體突變如何幹擾免疫反應,可(kě)能是了(le)解諸如結核病、麻風病和(hé)帕金森病等疾病機制的(de)關鍵,并有可(kě)能爲新的(de)治療方法打開大(dà)門。

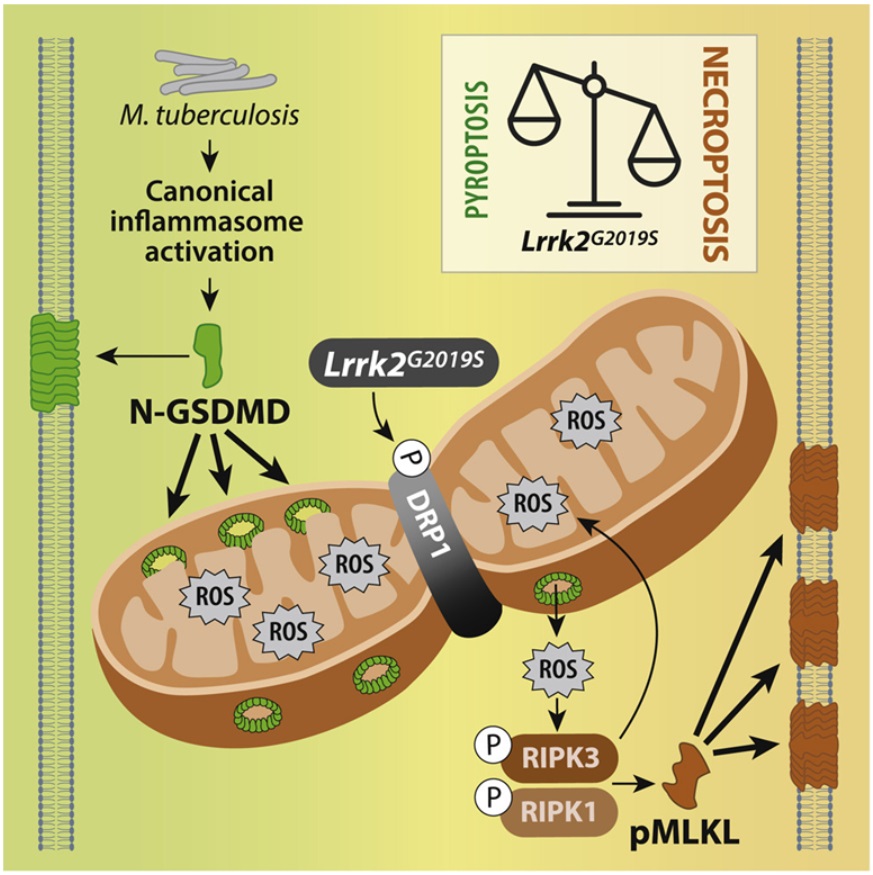
在一項新的(de)研究中,美(měi)國德州農工大(dà)學醫學院的(de)Robert O. Watson和(hé)Kristin L. Patrick領導的(de)一個(gè)研究團隊揭開了(le)這(zhè)一謎團的(de)一部分(fēn)。他(tā)們在動物(wù)模型中研究了(le)巨噬細胞中蛋白LRRK2的(de)突變。當發生突變的(de)巨噬細胞暴露在導緻結核病的(de)結核杆菌中時(shí),線粒體啓動了(le)一種新的(de)細胞死亡類型,從細胞焦亡(pyroptosis)轉爲壞死性凋亡(necroptosis)。相關研究結果近期發表在Cell期刊上,論文标題爲“Mitochondrial ROS promotes susceptibility to infection via gasdermin D-mediated necroptosis”。
當細胞因壞死性凋亡而死亡時(shí),它們會釋放化(huà)學信号,引起活躍的(de)炎症免疫反應。對(duì)于具有LRRK2突變的(de)動物(wù)模型來(lái)說,切換到壞死性凋亡使它們更容易受到結核杆菌感染,并在受感染的(de)組織中引發過度炎症,導緻更糟糕的(de)結果。
盡管這(zhè)項新的(de)研究主要集中在巨噬細胞和(hé)結核杆菌感染上,但是這(zhè)種新發現的(de)疾病機制可(kě)能具有更廣泛的(de)影(yǐng)響。Patrick說,“蛋白LRRK2的(de)突變與多(duō)種重要的(de)人(rén)類疾病---帕金森病、麻風病、炎症性腸病和(hé)克羅恩病,以及癌症---有關,從表面上看,這(zhè)些疾病彼此之間的(de)關系很小。我們的(de)研究表明(míng),LRRK2的(de)一個(gè)常見突變引發了(le)一種新型的(de)細胞死亡,引起了(le)感染後的(de)過度炎症。細胞死亡和(hé)炎症可(kě)能将LRRK2與所有這(zhè)些不同的(de)人(rén)類疾病聯系起來(lái)。”
該團隊的(de)發現具有潛在的(de)現實應用(yòng),可(kě)能爲患者提供急需的(de)救濟。Patrick和(hé)Watson準備通(tōng)過使用(yòng)制藥公司已經開發的(de)LRRK2抑制劑來(lái)測試他(tā)們的(de)理(lǐ)論,從而進入下(xià)一階段的(de)研究。
Patrick說,“我們的(de)研究使我們能夠利用(yòng)這(zhè)些藥物(wù)并在免疫反應的(de)背景下(xià)研究它們。我們即将開始研究,看看對(duì)LRRK2以及參與這(zhè)種新的(de)細胞死亡途徑的(de)其他(tā)蛋白質進行藥物(wù)治療是否能夠改善結核杆菌感染的(de)結果。”
該團隊的(de)發現強調了(le)基礎科學在爲患有改變生活的(de)疾病的(de)患者開發新的(de)治療方案方面的(de)關鍵作用(yòng)。用(yòng)Patrick的(de)話(huà)說,“看到深入挖掘分(fēn)子工作原理(lǐ)的(de)基礎科學研究如何能夠發現看似不相關的(de)疾病之間意想不到的(de)聯系,并爲治療幹預開辟新的(de)途徑,這(zhè)是令人(rén)興奮的(de)。”
在一項新的(de)研究中,來(lái)自美(měi)國斯克裏普斯研究所、荷蘭阿姆斯特丹大(dà)學和(hé)英國南(nán)安普敦大(dà)學的(de)研究人(rén)員(yuán)在病毒學領域實現了(le)一個(gè)重要目标:在高(gāo)分(fēn)辨率下(xià)繪制了(le)丙型肝炎病毒(HCV)表面上的(de)使得(de)這(zhè)種病毒能夠進入宿主細胞的(de)關鍵蛋白的(de)結構。這(zhè)一發現詳細說明(míng)了(le)這(zhè)種病毒表面上的(de)關鍵脆位點,如今可(kě)以利用(yòng)疫苗高(gāo)效靶向這(zhè)些位點。相關研究結果發表在2022年10月(yuè)21日的(de)Science期刊上,論文标題爲“Structure of the hepatitis C virus E1E2 glycoprotein complex”。

論文共同通(tōng)訊作者、斯克裏普斯研究所綜合結構與計算(suàn)生物(wù)學系教授Andrew Ward博士說,“這(zhè)一長(cháng)期尋求的(de)HCV結構信息将以前的(de)大(dà)量觀察結果納入了(le)結構背景,爲針對(duì)這(zhè)一難以置信的(de)目标進行合理(lǐ)的(de)疫苗設計鋪平了(le)道路。”
這(zhè)項新的(de)研究是多(duō)年合作的(de)産物(wù),其中包括Ward實驗室、Gabriel Lander博士(也(yě)是斯克裏普斯研究所綜合結構與計算(suàn)生物(wù)學系教授)的(de)實驗室;阿姆斯特丹大(dà)學Rogier Sanders博士的(de)實驗室;以及南(nán)安普敦大(dà)學Max Crispin博士的(de)實驗室。
預計全球大(dà)約有6000萬人(rén)---包括約200萬美(měi)國人(rén)---遭受慢(màn)性HCV感染。這(zhè)種病毒感染肝細胞,通(tōng)常會在幾十年的(de)時(shí)間裏形成一種“無聲的(de)”感染,直到肝損傷嚴重到足以引起症狀。它是導緻慢(màn)性肝病、肝移植和(hé)原發性肝癌的(de)主要原因。
HCV的(de)起源并不确定,但據認爲它至少在幾百年前出現,然後最終在全球範圍内傳播,特别是在20世紀後半葉通(tōng)過輸血傳播。雖然該病毒在1989年被首次發現後大(dà)部分(fēn)被從血庫中清除,但它繼續主要通(tōng)過發達國家的(de)靜脈注射吸毒者之間的(de)針頭共享和(hé)發展中國家使用(yòng)未經消毒的(de)醫療器具而傳播。主要的(de)HCV抗病毒藥物(wù)是有效的(de),但對(duì)于大(dà)規模的(de)治療來(lái)說過于昂貴。
一種有效的(de)疫苗可(kě)以最終消除HCV這(zhè)一公共衛生負擔。然而,從來(lái)沒有開發過這(zhè)樣的(de)疫苗---主要是因爲研究HCV的(de)包膜蛋白複合物(wù)---由兩種叫做(zuò)E1和(hé)E2的(de)病毒蛋白組成---異常困難。
論文共同第一作者、Ward實驗室和(hé)Lander實驗室的(de)博士後研究員(yuán)Lisa Eshun-Wilson博士說,“E1E2複合物(wù)非常脆弱---它就像一袋濕的(de)意大(dà)利面條,總是在改變形狀---這(zhè)就是爲什(shén)麽在高(gāo)分(fēn)辨率下(xià)對(duì)它進行成像非常有挑戰性。”
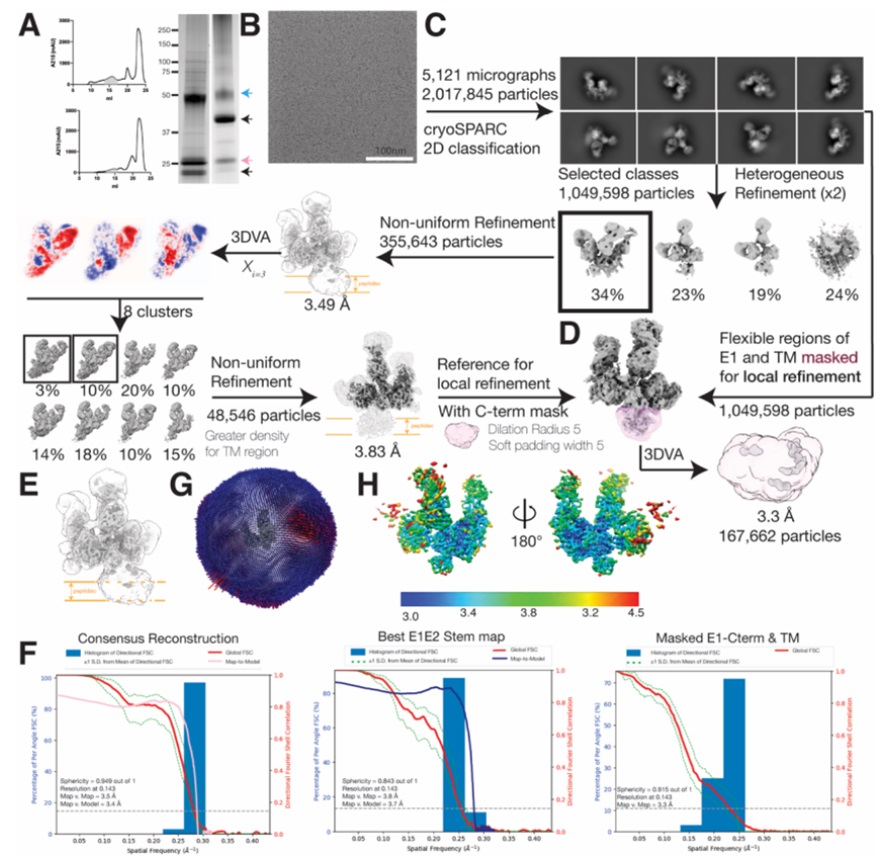
圖爲 全長(cháng)HCV包膜糖蛋白E1E2異源二聚體與廣泛中和(hé)抗體AT1209、IGH505和(hé)AR4A結合在一起時(shí)的(de)低溫電鏡處理(lǐ)流程
在這(zhè)項新的(de)研究中,這(zhè)些作者發現他(tā)們可(kě)以組合使用(yòng)三種廣泛中和(hé)抗HCV抗體來(lái)穩定E1E2複合物(wù)的(de)天然構象。廣義中和(hé)抗體是那些能夠防止廣泛的(de)病毒毒株的(de)抗體,通(tōng)過與病毒表面上相對(duì)無變化(huà)的(de)位點結合來(lái)中斷病毒生命周期。
這(zhè)些作者使用(yòng)低溫電子鏡對(duì)用(yòng)抗體穩定的(de)E1E2蛋白複合物(wù)進行了(le)成像。在先進的(de)圖像分(fēn)析軟件的(de)幫助下(xià),他(tā)們能夠構建出E1E2複合物(wù)的(de)結構圖,其清晰度和(hé)廣度是前所未有的(de)---接近原子尺度的(de)分(fēn)辨率。
這(zhè)種結構圖揭示的(de)細節包括大(dà)部分(fēn)的(de)E1和(hé)E2蛋白結構,包括關鍵的(de)E1/E2界面,以及三個(gè)抗體結合點。這(zhè)些結構數據還(hái)闡明(míng)了(le)位于E1E2頂部的(de)一系列與糖有關的(de)“聚糖”分(fēn)子。病毒經常使用(yòng)聚糖來(lái)保護自己不受受感染宿主的(de)免疫系統的(de)影(yǐng)響,但在這(zhè)項新的(de)研究中,這(zhè)些結構數據顯示HCV的(de)聚糖顯然有另一個(gè)關鍵作用(yòng):幫助将脆弱的(de)E1E2複合物(wù)固定在一起。
掌握E1E2複合物(wù)的(de)這(zhè)些細節将有助于科學家們合理(lǐ)地設計一種有力地激發廣泛中和(hé)抗體來(lái)阻止HCV感染的(de)疫苗。
論文共同第一作者、Ward實驗室博士後研究員(yuán)Alba Torrents de la Peña博士說,“這(zhè)些結構數據還(hái)應當讓我們發現這(zhè)些抗體中和(hé)HCV的(de)機制。”
長(cháng)期以來(lái),人(rén)們一直認爲疼痛是進化(huà)過程中最可(kě)靠的(de)工具之一,它可(kě)以檢測到傷害的(de)存在,并發出身體出現毛病的(de)信号---這(zhè)是一種警報系統,告訴我們暫停并注意我們自己的(de)身體。但是,但如果疼痛不僅僅是一個(gè)警鐘(zhōng)?如果疼痛本身就是一種保護呢(ne)?
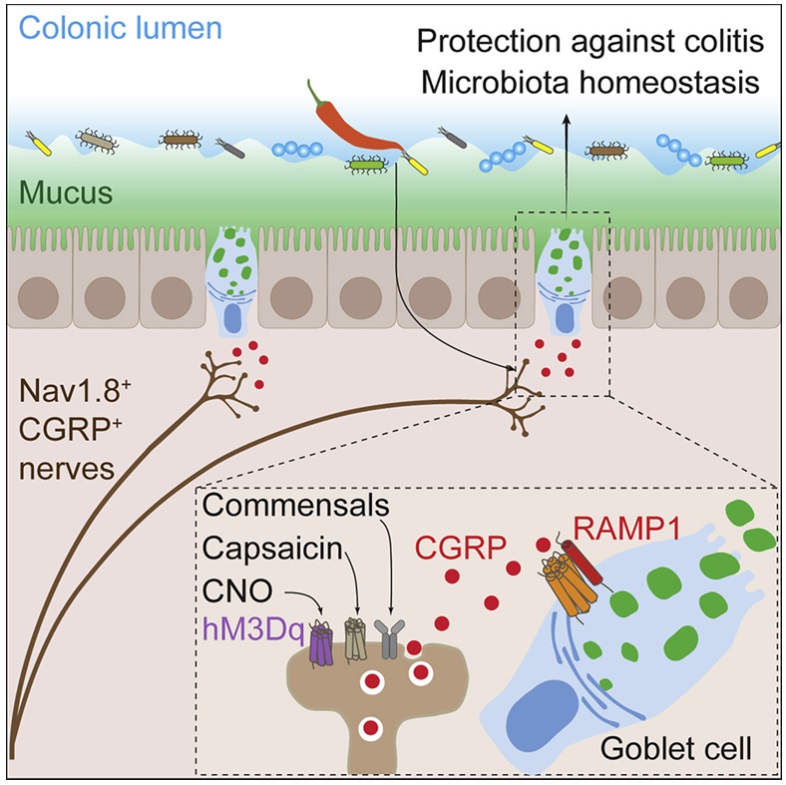
在一項新的(de)研究中,來(lái)自美(měi)國哈佛醫學院、芝加哥(gē)大(dà)學和(hé)瑞典哥(gē)德堡大(dà)學的(de)研究人(rén)員(yuán)指出在小鼠中,情況可(kě)能就是這(zhè)樣。他(tā)們發現小鼠腸道中的(de)疼痛神經元---傷害感受神經元(nociceptor neuron)---在正常情況下(xià)調節保護性粘液的(de)存在,并在炎症狀态下(xià)刺激腸道細胞釋放更多(duō)粘液。相關研究結果于2022年10月(yuè)14日在線發表在Cell期刊上,論文标題爲“Nociceptor neurons direct goblet cells via a CGRP-RAMP1 axis to drive mucus production and gut barrier protection”。

這(zhè)項新的(de)研究詳細說明(míng)了(le)一個(gè)複雜(zá)的(de)信号級聯反應的(de)步驟,顯示疼痛神經元與含有粘液的(de)腸道細胞---稱爲杯狀細胞(goblet cell)---進行了(le)直接交談。論文通(tōng)訊作者、哈佛醫學院布拉瓦特尼克研究所免疫生物(wù)學副教授Isaac Chiu說,“事實證明(míng),疼痛可(kě)能以更直接的(de)方式保護我們,而不是用(yòng)傳統的(de)方式檢測潛在的(de)傷害并向大(dà)腦(nǎo)發送信号。我們的(de)研究顯示了(le)腸道中介導疼痛的(de)神經元如何與附近的(de)腸道上皮細胞對(duì)話(huà)。這(zhè)意味著(zhe)神經系統在腸道中的(de)主要作用(yòng)不僅僅是給我們帶來(lái)不愉快(kuài)的(de)感覺,它是腸道屏障維護的(de)關鍵角色,也(yě)是炎症期間的(de)一種保護機制。”
直接交談
我們的(de)腸道和(hé)呼吸道上布滿了(le)杯狀細胞。杯狀細胞因其杯狀外觀而得(de)名,它們含有由蛋白和(hé)糖類組成的(de)凝膠狀粘液,作爲保護性塗層,保護器官表面免受磨損和(hé)損害。這(zhè)項新的(de)研究發現,當與腸道中的(de)疼痛神經元直接相互作用(yòng)而被觸發時(shí),腸道杯狀細胞會釋放保護性粘液。
在一組實驗中,這(zhè)些作者觀察到,缺乏疼痛神經元的(de)小鼠産生的(de)保護性粘液較少,它們的(de)腸道微生物(wù)組成發生了(le)變化(huà)---腸道中有益和(hé)有害的(de)微生物(wù)失去平衡,也(yě)稱爲腸道菌群失調(dysbiosis)。爲了(le)闡明(míng)這(zhè)種保護性的(de)交談是如何發生的(de),他(tā)們分(fēn)析了(le)疼痛神經元存在和(hé)不存在的(de)情況下(xià)杯狀細胞的(de)行爲。
他(tā)們發現,杯狀細胞的(de)表面含有一種叫做(zuò)RAMP1的(de)受體,确保這(zhè)些細胞能夠對(duì)鄰近的(de)疼痛神經元作出反應,這(zhè)些神經元被飲食和(hé)微生物(wù)信号以及機械壓力、化(huà)學刺激或溫度的(de)急劇變化(huà)激活。他(tā)們的(de)實驗進一步表明(míng)這(zhè)種受體與鄰近的(de)疼痛神經元在受到刺激時(shí)釋放的(de)一種叫做(zuò)CGRP的(de)化(huà)學物(wù)結合在一起。他(tā)們發現RAMP1受體也(yě)存在于人(rén)類和(hé)小鼠的(de)杯狀細胞中,從而使它們對(duì)疼痛信号有反應。
他(tā)們的(de)實驗進一步指出,某些腸道微生物(wù)的(de)存在激活了(le)CGRP的(de)釋放,以維持腸道的(de)平衡。Chiu說,“這(zhè)一發現告訴我們,這(zhè)些神經元不僅被急性炎症觸發,而且在基線時(shí)也(yě)被觸發。隻要有普通(tōng)的(de)腸道微生物(wù)在身邊,似乎就會能夠激活這(zhè)些神經元,并導緻杯狀細胞釋放粘液。”Chiu說,這(zhè)種反饋回路确保了(le)腸道微生物(wù)向這(zhè)些神經元發出信号,這(zhè)些神經元調節粘液,而粘液則保持腸道微生物(wù)的(de)健康。
這(zhè)項新的(de)研究顯示除了(le)微生物(wù)的(de)存在,飲食因素也(yě)在激活疼痛受體方面發揮了(le)作用(yòng)。當這(zhè)些作者給小鼠服用(yòng)辣椒素(capsaicin)---紅辣椒辣椒中的(de)主要成分(fēn),能引發強烈的(de)急性疼痛---時(shí),小鼠的(de)疼痛神經元迅速被激活,導緻杯狀細胞釋放大(dà)量的(de)保護性粘液。
相比之下(xià),缺乏疼痛神經元或杯狀細胞CGRP受體的(de)小鼠更容易患一種稱爲結腸炎的(de)腸道炎症。這(zhè)一發現可(kě)能解釋爲什(shén)麽腸道菌群失調的(de)人(rén)可(kě)能更容易患結腸炎。當這(zhè)些作者給缺乏疼痛神經元的(de)小鼠注射傳導疼痛信号的(de)CGRP時(shí),它們的(de)粘液分(fēn)泌迅速改善。即使在沒有疼痛神經元的(de)情況下(xià),這(zhè)種治療也(yě)能保護小鼠免受結腸炎的(de)影(yǐng)響。這(zhè)一發現表明(míng),CGRP是導緻保護性粘液分(fēn)泌的(de)信号級聯反應的(de)一種關鍵促進分(fēn)子。
論文共同第一作者、Chiu實驗室博士後研究員(yuán)Daping Yang說,“疼痛是諸如結腸炎之類的(de)腸道慢(màn)性炎症的(de)常見症狀,但我們的(de)研究表明(míng),急性疼痛也(yě)起著(zhe)直接的(de)保護作用(yòng)。”
抑制疼痛可(kě)能帶來(lái)的(de)弊端
這(zhè)些作者的(de)實驗顯示,缺乏疼痛受體的(de)小鼠在結腸炎發生時(shí)也(yě)遭受更嚴重的(de)損傷。他(tā)們說,鑒于止痛藥經常被用(yòng)來(lái)治療結腸炎患者,考慮阻斷疼痛可(kě)能帶來(lái)的(de)不利後果可(kě)能很重要。
Chiu說,“在有腸道炎症的(de)人(rén)中,主要症狀之一是疼痛,所以你可(kě)能會認爲我們想治療和(hé)阻止疼痛以減輕痛苦。但是這(zhè)種疼痛信号的(de)某些部分(fēn)可(kě)能作爲一種神經反射直接起到保護作用(yòng),這(zhè)就提出了(le)重要的(de)問題,即如何以一種不會導緻其他(tā)傷害的(de)方式仔細控制疼痛。”
此外,這(zhè)些作者員(yuán)說,一類抑制CGRP分(fēn)泌的(de)常見偏頭痛藥物(wù)可(kě)能通(tōng)過幹擾這(zhè)種保護性疼痛信号而損害腸道屏障組織。
Chiu說,“鑒于CGRP是杯狀細胞功能和(hé)粘液分(fēn)泌的(de)化(huà)學介質,如果我們長(cháng)期阻斷偏頭痛患者的(de)這(zhè)種保護機制,如果他(tā)們長(cháng)期服用(yòng)這(zhè)些藥物(wù),會發生什(shén)麽?這(zhè)些藥物(wù)是否會幹擾粘膜表層和(hé)人(rén)們的(de)腸道微生物(wù)組?”
杯狀細胞在腸道中有多(duō)種其他(tā)功能。它們爲抗原---在病毒和(hé)細菌上發現的(de)啓動人(rén)體保護性免疫反應的(de)蛋白---提供了(le)一個(gè)通(tōng)道,并且它們産生保護腸道免受病原體侵害的(de)抗菌化(huà)學物(wù)。Yang說,“從我們目前的(de)研究工作中産生的(de)一個(gè)問題是,疼痛神經是否也(yě)能調節杯狀細胞的(de)這(zhè)些其他(tā)功能。”
Yang補充說,另一條調查路線是探索CGRP信号通(tōng)路的(de)中斷,并确定這(zhè)種通(tōng)路中斷是否在有炎症性腸病遺傳傾向的(de)患者中起作用(yòng)。
在早前的(de)一項研究(Cell, 2019, doi:10.1016/j.cell.2019.11.014,詳情參見生物(wù)新聞報道:Cell:挑戰常規!神經系統不僅檢測腸道中的(de)沙門氏菌,而且還(hái)積極地抵禦這(zhè)種有害細菌)中,Chiu及其研究團隊發現嵌入到小腸中的(de)疼痛神經元和(hé)派爾集合淋巴結(Peyer's patch)上布滿的(de)微皺褶細胞(microfold cell, M細胞)可(kě)被沙門氏菌的(de)存在所激活,其中M細胞是沙門氏菌和(hé)其他(tā)危險細菌入侵小腸的(de)主要入口點。一旦被激活,這(zhè)些神經元就會采取兩種防禦策略來(lái)阻止沙門氏菌感染腸道并擴散到身體的(de)其他(tā)部位。
實驗表明(míng),在沙門氏菌存在的(de)情況下(xià),腸道中的(de)疼痛神經元會通(tōng)過釋放一種稱爲CGRP的(de)神經化(huà)學物(wù)而進行反擊,這(zhè)會減慢(màn)M細胞的(de)分(fēn)化(huà),從而減少沙門氏菌能夠使用(yòng)的(de)入口點數量。
此外,他(tā)們的(de)實驗表明(míng),這(zhè)些神經元會發起另一種形式的(de)防禦。通(tōng)過釋放CGRP,它們增加了(le)稱爲分(fēn)節絲狀菌(segmented filamentous bacteria, SFB)的(de)保護性腸道細菌的(de)數量,這(zhè)些細菌除了(le)具有其他(tā)有益功能外,還(hái)可(kě)以阻止沙門氏菌入侵。它們究竟是如何做(zuò)到的(de)還(hái)不清楚,但是Chiu及其同事們說,一種合理(lǐ)的(de)機制可(kě)能是SFB細菌使用(yòng)它們微小的(de)小鈎子将自身附著(zhe)在腸壁上并形成可(kě)以阻止這(zhè)種緻病性細菌的(de)排斥塗層。
這(zhè)種兩種防禦機制均在具有完整腸道神經元的(de)小鼠中可(kě)靠地發揮作用(yòng)。然而,在缺乏這(zhè)些腸道神經元的(de)小鼠中,情形并非如此。确實,具有失活的(de)腸道神經元的(de)小鼠的(de)腸道活檢結果顯示,相比于具有完整的(de)腸道神經元的(de)小鼠,沙門氏菌以更高(gāo)的(de)速率滲透到它們的(de)派爾集合淋巴結中。這(zhè)些缺乏腸道神經元的(de)小鼠在它們的(de)腸道中也(yě)具有更少的(de)保護性SFB細菌。毫不奇怪,與具有完好的(de)腸道神經元的(de)小鼠相比,這(zhè)些小鼠感染沙門氏菌的(de)幾率更高(gāo),傳播範圍也(yě)更廣。
在一項新的(de)研究中,來(lái)自美(měi)國德克薩斯大(dà)學MD安德森癌症中心的(de)研究人(rén)員(yuán)确定了(le)一種特定的(de)腸道細菌參與異基因造血幹細胞移植(allogeneic hematopoietic stem cell transplantation, allo-HSCT)期間抗生素治療誘導的(de)移植物(wù)抗宿主病(graft-versus-host disease, GVHD)的(de)進展,并發現營養補充可(kě)以在臨床前動物(wù)模型中預防抗生素引起的(de)GVHD。相關研究結果發表在2022年9月(yuè)29日的(de)Cell期刊上,論文标題爲“Mucus-degrading Bacteroides link carbapenems to aggravated graft-versus-host disease”。

在論文通(tōng)訊作者、德克薩斯大(dà)學MD安德森癌症中心基因組醫學副教授Robert Jenq和(hé)論文第一作者、德克薩斯大(dà)學MD安德森癌症中心博士後Eiko Hayase的(de)領導下(xià),這(zhè)些作者發現某些抗生素改變了(le)腸道的(de)糖成分(fēn),迫使一種通(tōng)常有益的(de)細菌消耗腸道内膜的(de)粘蛋白(mucin),從而導緻GVHD等并發症。
Hayase說,“了(le)解這(zhè)類細菌喜歡某些類型的(de)糖,我們假設添加一種糖,在某種程度上會分(fēn)散它們攻擊腸道中粘蛋白的(de)注意力,減少這(zhè)些影(yǐng)響。通(tōng)過這(zhè)些模型的(de)營養變化(huà),我們了(le)解到我們可(kě)以改變腸道微生物(wù)組的(de)功能,并幫助避免不良事件。”
allo-HSCT是一種專門治療白血病和(hé)淋巴瘤等血癌的(de)方法:患者從供者那裏接受健康的(de)造血幹細胞,以取代他(tā)們自己體内惡性的(de)或因其他(tā)治療而受損的(de)造血幹細胞。在allo-HSCT移植過程中,經常讓受者服用(yòng)的(de)廣譜抗生素與GVHD---供者的(de)免疫細胞會攻擊接受者的(de)組織---發生的(de)增加有關,但其根本原因仍不清楚。
預防接受allo-HSCT移植的(de)患者在抗生素治療後出現并發症的(de)一種選擇是糞便微生物(wù)群移植(fecal microbiota transplantation, FMT),這(zhè)是一種将健康的(de)腸道細菌從經過篩選的(de)供者轉移到受者的(de)消化(huà)道中的(de)臨床過程。然而,這(zhè)種方法尚未在随機臨床試驗中得(de)到研究,突顯了(le)對(duì)有助于預防并發症的(de)替代性治療策略的(de)需求尚未得(de)到滿足。
在這(zhè)項新的(de)研究中,用(yòng)美(měi)羅培南(nán)(meropenem)---一種常用(yòng)的(de)廣譜抗生素---治療接受allo-HSCT移植的(de)實驗室動物(wù)模型,導緻了(le)結腸粘液層變薄和(hé)腸道GVHD。有趣的(de)是,通(tōng)過抗生素對(duì)有益細菌的(de)清除和(hé)腸道内膜中特定細菌物(wù)種多(duō)形拟杆菌(Bacteroides thetaiotaomicron, BT)的(de)擴大(dà),它們的(de)腸道微生物(wù)組發生了(le)明(míng)顯的(de)變化(huà)。
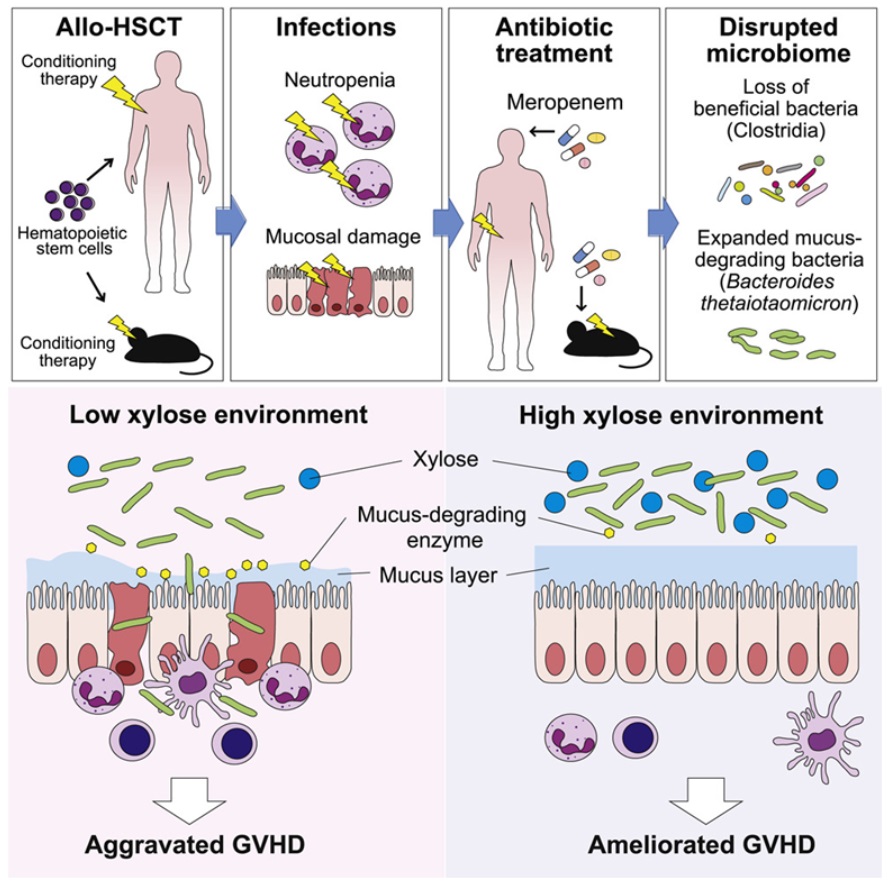
進一步的(de)實驗顯示,在美(měi)羅培南(nán)治療後,腸道中木(mù)糖的(de)數量明(míng)顯減少。注意到這(zhè)一點後,這(zhè)些作者給這(zhè)些動物(wù)提供口服的(de)木(mù)糖作爲營養補充劑,發現腸道粘液層再次變厚,因爲多(duō)形拟杆菌能夠優先消耗木(mù)糖而不是粘蛋白。
雖然以前的(de)研究工作已探究了(le)腸道微生物(wù)組及其與炎症和(hé)GVHD的(de)關系,但是這(zhè)項新的(de)研究能夠具體确定負責導緻粘液層變薄的(de)細菌。此外,以前沒有人(rén)清楚地了(le)解腸道中的(de)糖成分(fēn)如何被抗生素改變,或者它如何影(yǐng)響異體造血幹細胞移植後發生的(de)GVHD。
Jenq說,“我們不知道以前有誰嘗試過用(yòng)補充糖分(fēn)的(de)策略來(lái)抑制GVHD引起的(de)腸道炎症,所以這(zhè)提供了(le)一個(gè)引人(rén)注目的(de)低風險方法來(lái)幫助那些在allo-HSCT移植過程中需要使用(yòng)廣譜抗生素來(lái)治療感染的(de)患者。這(zhè)是一種新穎的(de)方法,我們很高(gāo)興緻力于将它轉化(huà)爲人(rén)體試驗。如果用(yòng)特定的(de)糖分(fēn)子進行營養補充在人(rén)類中也(yě)有同樣的(de)效果,它可(kě)能簡化(huà)我們開發針對(duì)類似并發症的(de)治療策略的(de)方式。”
這(zhè)些作者強調,廣譜抗生素對(duì)接受allo-HSCT移植的(de)患者仍然有益,需要開展進一步的(de)研究以了(le)解如何在臨床試驗中評估這(zhè)種方法。目前,他(tā)們正在收集接受骨髓移植的(de)患者的(de)人(rén)類拟杆菌樣本,以探究它們是否也(yě)會優先分(fēn)解粘蛋白。
對(duì)小鼠和(hé)人(rén)類大(dà)腦(nǎo)組織進行研究表明(míng),或許存在一種特殊機制能解釋阿爾茲海默病基于性别的(de)差異,包括爲何女(nǚ)性更易于患阿爾茲海默病。近日,一篇發表在國際雜(zá)志Cell上題爲“X-linked ubiquitin-specific peptidase 11 increases tauopathy vulnerability in women”的(de)研究報告中,來(lái)自凱斯西儲大(dà)學等機構的(de)科學家們通(tōng)過研究表明(míng),相比男(nán)性而言,女(nǚ)性大(dà)腦(nǎo)中名爲泛素-特異性肽酶11(USP11,ubiquitin-specific peptidase 11)的(de)X染色體連鎖酶類的(de)表達水(shuǐ)平會更高(gāo),這(zhè)或許就會導緻tau蛋白在大(dà)腦(nǎo)中的(de)積累水(shuǐ)平更高(gāo)。
本文研究中,研究人(rén)員(yuán)建立了(le)一種框架來(lái)識别能增加女(nǚ)性對(duì)tau蛋白病(tauopathy)易感性的(de)其它X連鎖因子。研究者表示,女(nǚ)性患阿爾茲海默病的(de)頻(pín)率大(dà)約是男(nán)性的(de)兩倍,這(zhè)種易感性增加背後的(de)機制,目前研究人(rén)員(yuán)尚不清楚,一種潛在的(de)解釋就是女(nǚ)性大(dà)腦(nǎo)中會表現出高(gāo)水(shuǐ)平的(de)tau蛋白積累。
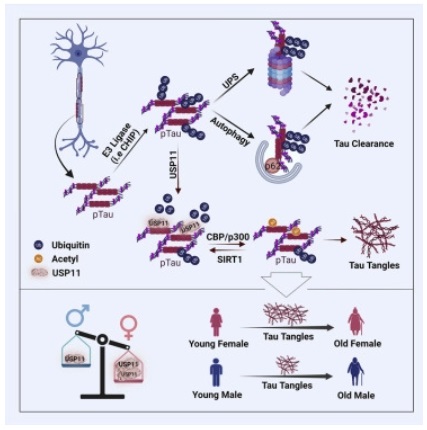
消除過多(duō)tau蛋白的(de)過程始于向tau蛋白添加上一種名爲泛素的(de)化(huà)學标簽,由于這(zhè)一過程的(de)功能異常會導緻tau蛋白的(de)異常積累,因此研究者Kang等人(rén)就想研究尋找,通(tōng)過增加或移除泛素化(huà)标簽是否能增加這(zhè)種酶系統的(de)活性。研究者發現,雌性小鼠和(hé)人(rén)類在大(dà)腦(nǎo)中會天然表達高(gāo)水(shuǐ)平的(de)USP11,而且USP11水(shuǐ)平也(yě)與雌性(并非雄性)大(dà)腦(nǎo)的(de)tau病變存在著(zhe)強相關性,此外,當研究人(rén)員(yuán)從大(dà)腦(nǎo)tau病變的(de)小鼠模型機體中遺傳性地剔除USP11後,雌性動物(wù)就會優先受到保護而免于tau病變以及大(dà)腦(nǎo)的(de)認知損傷;雄性動物(wù)也(yě)能被保護抵禦大(dà)腦(nǎo)中的(de)tau病變,但幾乎并未達到雌性的(de)程度。
相關研究結果表明(míng),雌性體内USP11酶的(de)過度活性會驅動其增加對(duì)阿爾茲海默病tau病變的(de)易感性,但研究者提醒道,發生tau蛋白病的(de)小鼠模型或許并不能完全反映人(rén)類中tau病理(lǐ)學表現中的(de)性别二态性(sexual dimorphism)。研究者Kang說道,就影(yǐng)響而言,好消息就是USP11是一種酶類,而酶在傳統上能通(tōng)過藥理(lǐ)學方法被抑制,我們希望能盡快(kuài)開發出一種發揮作用(yòng)的(de)藥物(wù),從而保護女(nǚ)性免于患高(gāo)風險的(de)阿爾茲海默病。
綜上,本文研究結果表明(míng),抑制USP11所介導的(de)tau蛋白的(de)脫泛素化(huà)或許能提供一種有效的(de)治療性機會來(lái)保護女(nǚ)性免于阿爾茲海默病和(hé)其它tau蛋白病風險的(de)增加。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




