利用(yòng)新方法成功純化(huà)和(hé)表征人(rén)類神經幹細胞
在一項新的(de)研究中,來(lái)自美(měi)國斯坦福大(dà)學的(de)研究人(rén)員(yuán)設計了(le)一種熒光(guāng)激活細胞分(fēn)選方法,從人(rén)類大(dà)腦(nǎo)組織中分(fēn)離出不同的(de)神經幹細胞和(hé)祖細胞類型。這(zhè)項研究中使用(yòng)的(de)标志物(wù)在不同的(de)大(dà)腦(nǎo)區(qū)域都是保守的(de)。該技術應有助于未來(lái)的(de)神經發育研究,并加速開發基于神經細胞移植的(de)治療方案,以治療一系列神經系統疾病。相關研究結果發表在2023年3月(yuè)16日的(de)Cell期刊上,論文标題爲“Purification and characterization of human neural stem and progenitor cells”。

人(rén)腦(nǎo)擁有約1710億個(gè)細胞,其中略高(gāo)于一半(約860億)是神經細胞。這(zhè)860億個(gè)神經細胞是一個(gè)多(duō)樣化(huà)的(de)細胞群體,有數百種專門的(de)類型和(hé)功能,但都源自三個(gè)神經細胞譜系---神經元、少突膠質細胞和(hé)星形膠質細胞。這(zhè)三個(gè)細胞譜系都是從神經幹/祖先放射狀膠質細胞(neural stem and progenitor radial glia cell)池開始的(de),這(zhè)些神經幹/祖先放射狀膠質細胞在産前妊娠的(de)第二個(gè)三個(gè)月(yuè)經曆了(le)快(kuài)速發育。了(le)解這(zhè)些放射狀膠質細胞,它們如何分(fēn)化(huà)成這(zhè)三個(gè)細胞譜系,以及這(zhè)三個(gè)譜系如何分(fēn)化(huà)成多(duō)樣化(huà)的(de)神經細胞,将對(duì)醫學研究有巨大(dà)的(de)好處。
熒光(guāng)激活細胞分(fēn)選用(yòng)于從單細胞懸浮液中根據細胞表面免疫表型分(fēn)離腦(nǎo)組織中的(de)細胞類型。細胞經過索引(熒光(guāng)記錄)并相互分(fēn)離。這(zhè)些分(fēn)離的(de)細胞接受單細胞RNA測序,以捕獲它們各自的(de)轉錄組。通(tōng)過将表面标志物(wù)譜與索引和(hé)轉錄組相結合,這(zhè)些作者如今有了(le)每個(gè)細胞類型的(de)圖譜,可(kě)用(yòng)于以後的(de)識别。他(tā)們還(hái)測量了(le)最初分(fēn)離方案中沒有使用(yòng)的(de)另外352種表面标志物(wù)的(de)表達,這(zhè)些标志物(wù)可(kě)能在未來(lái)更好地區(qū)分(fēn)細胞。
索引排序數據允許每種被測序的(de)細胞對(duì)應到它們的(de)原始免疫表型,而且這(zhè)些作者發現RNA和(hé)細胞表面蛋白的(de)表達并不總是相關的(de)。一些看起來(lái)相似的(de)細胞可(kě)能有不同的(de)功能。這(zhè)種策略産生了(le)功能相似的(de)分(fēn)選細胞群體,從而允許分(fēn)離出特定的(de)神經幹細胞和(hé)祖細胞類型來(lái)進行分(fēn)析。
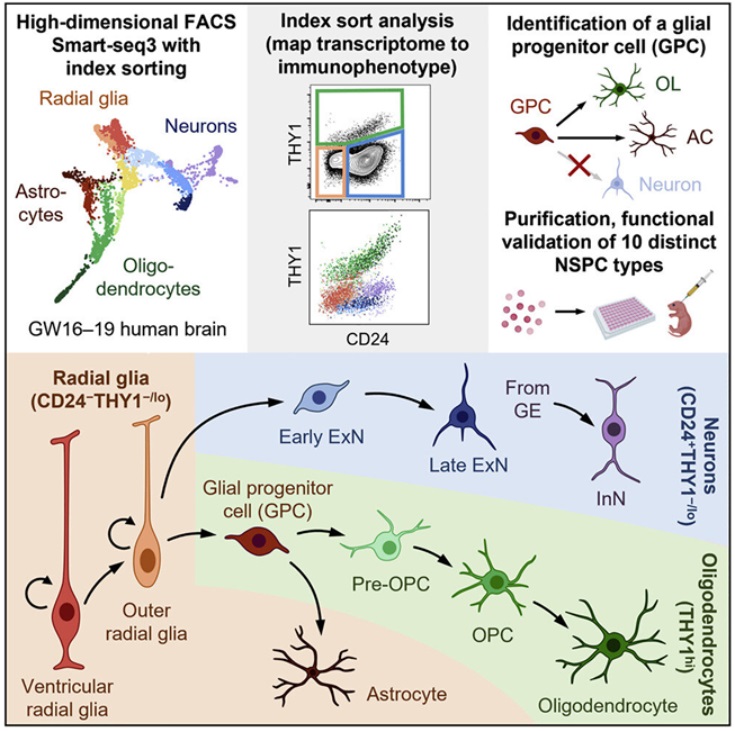
這(zhè)些作者确定了(le)10種神經幹/祖細胞類型,并通(tōng)過将它們直接移植到新生兒(ér)免疫缺陷小鼠的(de)大(dà)腦(nǎo)中來(lái)确定這(zhè)些細胞的(de)行爲特征。6個(gè)月(yuè)後,這(zhè)些細胞在整個(gè)大(dà)腦(nǎo)中廣泛遷移和(hé)定植,并分(fēn)化(huà)出所有三種主要的(de)神經細胞譜系。通(tōng)過觀察單個(gè)細胞類型的(de)擴散方式和(hé)位置,他(tā)們可(kě)以對(duì)适宜的(de)活動位點做(zuò)出一些初步推斷。雖然該實驗僅僅是作爲一種方法的(de)可(kě)行性測試,但是他(tā)們确實确定了(le)一種以前沒有描述過的(de)獨特的(de)雙能性膠質祖細胞(bipotent glial progenitor cell)的(de)功能特征。這(zhè)些作者成功地進行了(le)概念驗證,并發現可(kě)以根據細胞表面标志物(wù)從發育中的(de)大(dà)腦(nǎo)中分(fēn)離出不同的(de)細胞類型。如果所使用(yòng)的(de)方法可(kě)以推廣到其他(tā)幹細胞類型,科學家們對(duì)細胞在大(dà)腦(nǎo)或其他(tā)器官中發揮的(de)特定功能、機制和(hé)層次作用(yòng)的(de)理(lǐ)解可(kě)能會激增。
堿基編輯器有望用(yòng)于治療CD3δ重症聯合免疫缺陷
在一項新的(de)研究中,來(lái)自美(měi)國加州大(dà)學洛杉矶分(fēn)校等研究機構的(de)研究人(rén)員(yuán)發現先進的(de)基因組編輯技術可(kě)能能夠用(yòng)于罕見的(de)緻命遺傳病--- CD3δ重症聯合免疫缺陷(D3 delta severe combined immunodeficiency,CD3δSCID)---的(de)一次性治療。相關研究結果于2023年3月(yuè)20日在線發表在Cell期刊上,論文标題爲“Human T cell generation is restored in CD3δ severe combined immunodeficiency through adenine base editing”。CD3δSCID是由CD3D基因突變引起的(de),它阻止了(le)CD3δ蛋白的(de)産生,而這(zhè)種蛋白是造血幹細胞正常産生T細胞所需的(de)。沒有T細胞,出生時(shí)患有CD3δSCID的(de)嬰兒(ér)無法抵禦感染,如果不加以治療,往往在出生後的(de)頭兩年内死亡。目前,骨髓移植是唯一可(kě)用(yòng)的(de)治療方法,但是這(zhè)種方法有很大(dà)風險。
在這(zhè)項新的(de)研究中,這(zhè)些作者發現一種名爲堿基編輯(base editing)的(de)新型基因組編輯技術可(kě)以校正造血幹細胞中導緻CD3δSCID的(de)突變,并恢複它們産生T細胞的(de)能力。這(zhè)種潛在療法是加州大(dà)學洛杉矶分(fēn)校的(de)Donald Kohn博士和(hé)Gay Crooks博士的(de)實驗室合作的(de)結果。
Kohn實驗室之前已成功開發了(le)針對(duì)幾種免疫系統缺陷的(de)基因療法,包括其他(tā)形式的(de)重症聯合免疫缺陷(SCID)。他(tā)和(hé)他(tā)的(de)同事們應加拿大(dà)阿爾伯塔兒(ér)童醫院研究所的(de)小兒(ér)血液學和(hé)免疫學專家Nicola Wright博士的(de)請求,将注意力轉向了(le)CD3δSCID,當時(shí)Wright正在爲她的(de)患者尋找更好的(de)治療方案。
CD3δSCID在加拿大(dà)和(hé)墨西哥(gē)之間移民的(de)門諾派教徒社區(qū)很普遍。Wright說,“由于墨西哥(gē)沒有對(duì)新生兒(ér)進行SCID篩查,我經常看到一些嬰兒(ér)被診斷得(de)很晚,回到加拿大(dà)後病得(de)很重。”
當Kohn向他(tā)的(de)實驗室提出Wright的(de)請求時(shí),當時(shí)在加州大(dà)學洛杉矶分(fēn)校大(dà)四結束時(shí)加入Kohn實驗室的(de)研究助理(lǐ)Grace McAuley站出來(lái)提出了(le)一個(gè)大(dà)膽的(de)想法。Kohn說,“McAuley建議(yì)我們嘗試堿基編輯,這(zhè)是我的(de)實驗室以前從未嘗試過的(de)一項非常新的(de)技術。”
堿基編輯是一種超精确的(de)基因組編輯形式,使科學家們能夠校正DNA中的(de)單堿基突變。DNA由四種堿基---A、T、C和(hé)G---組成;這(zhè)些堿基配對(duì)形成了(le)DNA雙螺旋梯形結構中的(de)“橫檔(rungs)”。其他(tā)基因編輯平台,如CRISPR-Cas9,會切割染色體的(de)兩條鏈來(lái)改變DNA,而堿基編輯是通(tōng)過化(huà)學方法将一種DNA堿基變成另一種(比如将A變成G),而讓染色體保持完整。
McAuley說,“一開始我有一個(gè)非常陡峭的(de)學習(xí)曲線,當時(shí)堿基編輯并不奏效。但我繼續向前推進。我的(de)目标是幫助将這(zhè)種療法以盡可(kě)能快(kuài)的(de)速度推廣到臨床。”
McAuley聯系了(le)布羅德研究所的(de)David Liu(堿基編輯的(de)發明(míng)者),就如何評估該技術在這(zhè)一特定用(yòng)途中的(de)安全性尋求建議(yì)。最終,McAuley确定了(le)一種能高(gāo)效校正緻病基因突變的(de)堿基編輯器。
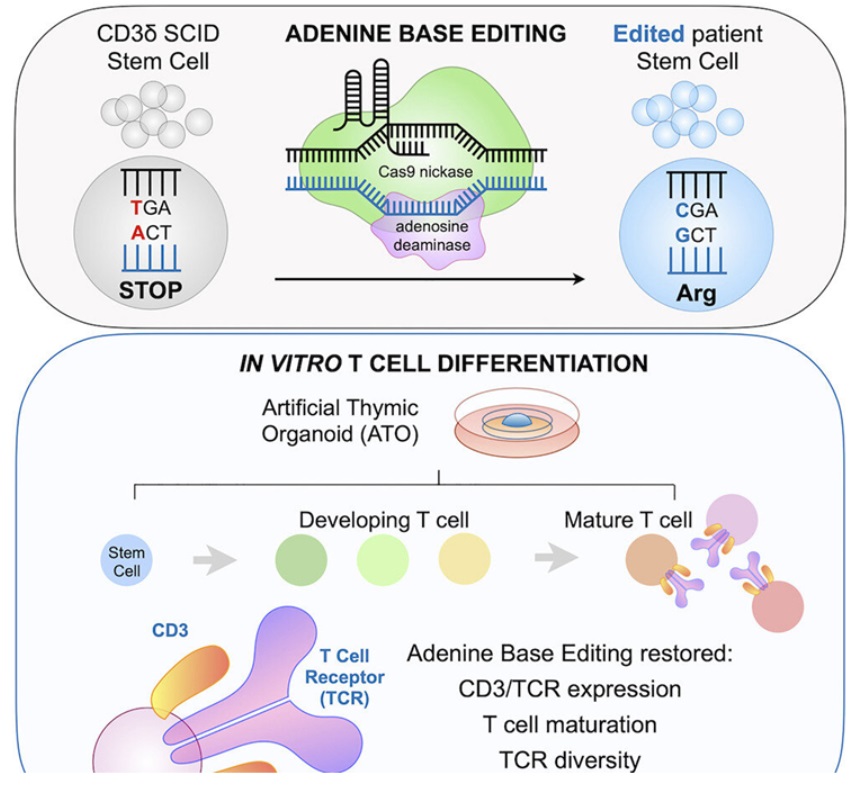
由于這(zhè)種疾病極爲罕見,爲這(zhè)項新的(de)研究獲取患者的(de)造血幹細胞是一項重大(dà)挑戰。當Wright向這(zhè)項研究提供了(le)一名正在接受骨髓移植的(de)CD3δSCID患者捐贈的(de)造血幹細胞後,該項目得(de)到了(le)推動。這(zhè)種堿基編輯器在三項實驗室實驗中,平均校正了(le)該患者近71%的(de)造血幹細胞。接下(xià)來(lái),McAuley與加州大(dà)學洛杉矶分(fēn)校風濕病學臨床講師Gloria Yiu博士合作,測試校正後的(de)造血幹細胞是否能産生T細胞。Yiu使用(yòng)人(rén)工胸腺類器官,這(zhè)是Crooks實驗室開發的(de)模拟人(rén)類胸腺環境的(de)幹細胞衍生組織模型。當這(zhè)些經過校正的(de)造血幹細胞被引入人(rén)工胸腺類器官時(shí),它們産生了(le)功能齊全的(de)成熟T細胞。Yiu說,“由于人(rén)工胸腺類器官能有效地支持成熟T細胞的(de)發育,它是一個(gè)理(lǐ)想的(de)系統,表明(míng)對(duì)患者造血幹細胞進行堿基編輯能修複這(zhè)種疾病中的(de)缺陷。”作爲最後一步,McAuley通(tōng)過将經過校正的(de)造血幹細胞移植到小鼠體内,研究了(le)它們的(de)壽命。移植後四個(gè)月(yuè),這(zhè)些經過校正的(de)造血幹細胞仍然存在,表明(míng)堿基編輯已校正了(le)真正的(de)、自我更新的(de)造血幹細胞中的(de)突變。這(zhè)些研究結果表明(míng),校正後的(de)造血幹細胞可(kě)以長(cháng)期存在,并産生患者健康生活所需的(de)T細胞。這(zhè)些作者正在研究如何将這(zhè)種新方法帶入加拿大(dà)、墨西哥(gē)和(hé)美(měi)國的(de)CD3δSCID嬰兒(ér)的(de)臨床試驗中。這(zhè)項研究中描述的(de)治療方法僅用(yòng)于臨床前測試,尚未在人(rén)類身上進行測試,也(yě)未被美(měi)國食品藥品管理(lǐ)局(FDA)批準可(kě)安全和(hé)有效地用(yòng)于人(rén)類。該技術被提交專利申請,Kohn和(hé)McAuley被列爲共同發明(míng)人(rén)。
揭示特定組蛋白突變導緻嚴重神經發育綜合征的(de)遺傳機制
在一項新的(de)開創性研究中,來(lái)自加拿大(dà)麥吉爾大(dà)學等研究機構的(de)研究人(rén)員(yuán)通(tōng)過研究三種特定組蛋白突變(H3.3G34R、H3.3G34V和(hé)H3.3G34W)的(de)發育後果,揭示了(le)導緻嚴重神經發育綜合征的(de)遺傳機制。就像修剪樹木(mù)有助于促進适當的(de)生長(cháng)一樣,大(dà)腦(nǎo)利用(yòng)突觸修剪(synaptic pruning)來(lái)去除其細胞之間不必要的(de)連接。然而,當這(zhè)一發生在幼兒(ér)期和(hé)成年期的(de)正常過程不能正常停止時(shí),大(dà)腦(nǎo)會失去太多(duō)的(de)連接,包括一些重要的(de)連接。由于這(zhè)種過度的(de)突觸修剪,一些腦(nǎo)細胞死亡,另一些腦(nǎo)細胞引起炎症,從而導緻運動、思考和(hé)學習(xí)方面的(de)問題。 在一項新的(de)開創性研究中,來(lái)自加拿大(dà)麥吉爾大(dà)學等研究機構的(de)研究人(rén)員(yuán)弄清了(le)這(zhè)一錯誤過程是如何發生的(de)。他(tā)們通(tōng)過研究三種特定組蛋白突變(H3.3G34R、H3.3G34V和(hé)H3.3G34W)的(de)發育後果,揭示了(le)導緻嚴重神經發育綜合征的(de)遺傳機制。具體而言,他(tā)們發現了(le)在由這(zhè)些生殖系突變--存在于生殖細胞中并被整合到每個(gè)細胞的(de)DNA中的(de)突變---引起的(de)疾病中,大(dà)腦(nǎo)是如何受損的(de)。相關研究結果發表在2023年3月(yuè)16日的(de)Cell期刊上,論文标題爲“Single substitution in H3.3G34 alters DNMT3A recruitment to cause progressive neurodegeneration”。他(tā)們的(de)研究結果不僅可(kě)能有助于科學家們找到治療這(zhè)些疾病的(de)新方法,而且也(yě)爲研究其他(tā)涉及腦(nǎo)細胞損失和(hé)炎症的(de)神經系統疾病(比如阿爾茨海默病)以及據猜測存在過度突觸修剪的(de)疾病(如精神分(fēn)裂症)提供了(le)啓示。論文通(tōng)訊作者、麥吉爾大(dà)學健康中心研究所的(de)Nada Jabado博士說,“神經元不能被替換。找到可(kě)能影(yǐng)響它們的(de)機制很重要,并爲急需的(de)治療性幹預措施打開了(le)大(dà)門,這(zhè)既是爲了(le)在神經元損失變得(de)重要之前抑制炎症;也(yě)是爲了(le)長(cháng)期遏制疾病。”論文共同作者、麥吉爾大(dà)學人(rén)類遺傳學副教授Claudia Kleinman博士補充說,“神經變性是我們随著(zhe)年齡增長(cháng)所面臨的(de)主要問題之一。任何新的(de)見解都是受歡迎的(de),因爲需求是巨大(dà)的(de),我們的(de)發現可(kě)能會對(duì)這(zhè)一破壞性的(de)問題提出另一種解釋。”持續性而非暫時(shí)性的(de)修剪這(zhè)項新的(de)研究顯示,組蛋白基因的(de)特定突變導緻染色質(由DNA和(hé)組蛋白形成,經壓縮後可(kě)變成染色體)特定區(qū)域上的(de)“信标(beacons)”表達減少。這(zhè)些信标通(tōng)常會招募DNMT3A,即一種能夠根據招募區(qū)域沉默或激活基因的(de)酶。它們的(de)減少使得(de)基因能夠繼續産生有助于突觸修剪過程的(de)蛋白。因此,本應停止的(de)突觸修剪繼續進行,造成大(dà)腦(nǎo)損傷。論文共同作者、麥吉爾大(dà)學外科系助理(lǐ)教授Livia Garzia博士解釋說,“我們知道,嚴重的(de)神經發育綜合征與較小的(de)大(dà)腦(nǎo);行走、吃(chī)飯和(hé)說話(huà)存在困難以及學習(xí)困難有關,是由組蛋白的(de)某些生殖系突變引起的(de)。在這(zhè)項新的(de)研究中,我們證實了(le)當組蛋白不能正常工作并讓大(dà)腦(nǎo)制造出比需要的(de)更多(duō)的(de)炎性蛋白而導緻漸進性神經退化(huà)時(shí)會發生什(shén)麽。”這(zhè)一切都從兩名患者開始Jabado博士團隊确定了(le)一名H3.3G34R新生生殖系突變(不是從父母那裏遺傳的(de))的(de)患者。該患者與另一名攜帶H3.3G34V突變的(de)患者表現出共同的(de)特征。這(zhè)兩名患者從出生起就有嚴重的(de)神經發育遲緩,在出生後的(de)發育過程中更加惡化(huà)。在2歲時(shí),他(tā)們也(yě)有嚴重的(de)生長(cháng)延遲和(hé)小頭症。
在一項新的(de)開創性研究中,來(lái)自加拿大(dà)麥吉爾大(dà)學等研究機構的(de)研究人(rén)員(yuán)弄清了(le)這(zhè)一錯誤過程是如何發生的(de)。他(tā)們通(tōng)過研究三種特定組蛋白突變(H3.3G34R、H3.3G34V和(hé)H3.3G34W)的(de)發育後果,揭示了(le)導緻嚴重神經發育綜合征的(de)遺傳機制。具體而言,他(tā)們發現了(le)在由這(zhè)些生殖系突變--存在于生殖細胞中并被整合到每個(gè)細胞的(de)DNA中的(de)突變---引起的(de)疾病中,大(dà)腦(nǎo)是如何受損的(de)。相關研究結果發表在2023年3月(yuè)16日的(de)Cell期刊上,論文标題爲“Single substitution in H3.3G34 alters DNMT3A recruitment to cause progressive neurodegeneration”。他(tā)們的(de)研究結果不僅可(kě)能有助于科學家們找到治療這(zhè)些疾病的(de)新方法,而且也(yě)爲研究其他(tā)涉及腦(nǎo)細胞損失和(hé)炎症的(de)神經系統疾病(比如阿爾茨海默病)以及據猜測存在過度突觸修剪的(de)疾病(如精神分(fēn)裂症)提供了(le)啓示。論文通(tōng)訊作者、麥吉爾大(dà)學健康中心研究所的(de)Nada Jabado博士說,“神經元不能被替換。找到可(kě)能影(yǐng)響它們的(de)機制很重要,并爲急需的(de)治療性幹預措施打開了(le)大(dà)門,這(zhè)既是爲了(le)在神經元損失變得(de)重要之前抑制炎症;也(yě)是爲了(le)長(cháng)期遏制疾病。”論文共同作者、麥吉爾大(dà)學人(rén)類遺傳學副教授Claudia Kleinman博士補充說,“神經變性是我們随著(zhe)年齡增長(cháng)所面臨的(de)主要問題之一。任何新的(de)見解都是受歡迎的(de),因爲需求是巨大(dà)的(de),我們的(de)發現可(kě)能會對(duì)這(zhè)一破壞性的(de)問題提出另一種解釋。”持續性而非暫時(shí)性的(de)修剪這(zhè)項新的(de)研究顯示,組蛋白基因的(de)特定突變導緻染色質(由DNA和(hé)組蛋白形成,經壓縮後可(kě)變成染色體)特定區(qū)域上的(de)“信标(beacons)”表達減少。這(zhè)些信标通(tōng)常會招募DNMT3A,即一種能夠根據招募區(qū)域沉默或激活基因的(de)酶。它們的(de)減少使得(de)基因能夠繼續産生有助于突觸修剪過程的(de)蛋白。因此,本應停止的(de)突觸修剪繼續進行,造成大(dà)腦(nǎo)損傷。論文共同作者、麥吉爾大(dà)學外科系助理(lǐ)教授Livia Garzia博士解釋說,“我們知道,嚴重的(de)神經發育綜合征與較小的(de)大(dà)腦(nǎo);行走、吃(chī)飯和(hé)說話(huà)存在困難以及學習(xí)困難有關,是由組蛋白的(de)某些生殖系突變引起的(de)。在這(zhè)項新的(de)研究中,我們證實了(le)當組蛋白不能正常工作并讓大(dà)腦(nǎo)制造出比需要的(de)更多(duō)的(de)炎性蛋白而導緻漸進性神經退化(huà)時(shí)會發生什(shén)麽。”這(zhè)一切都從兩名患者開始Jabado博士團隊确定了(le)一名H3.3G34R新生生殖系突變(不是從父母那裏遺傳的(de))的(de)患者。該患者與另一名攜帶H3.3G34V突變的(de)患者表現出共同的(de)特征。這(zhè)兩名患者從出生起就有嚴重的(de)神經發育遲緩,在出生後的(de)發育過程中更加惡化(huà)。在2歲時(shí),他(tā)們也(yě)有嚴重的(de)生長(cháng)延遲和(hé)小頭症。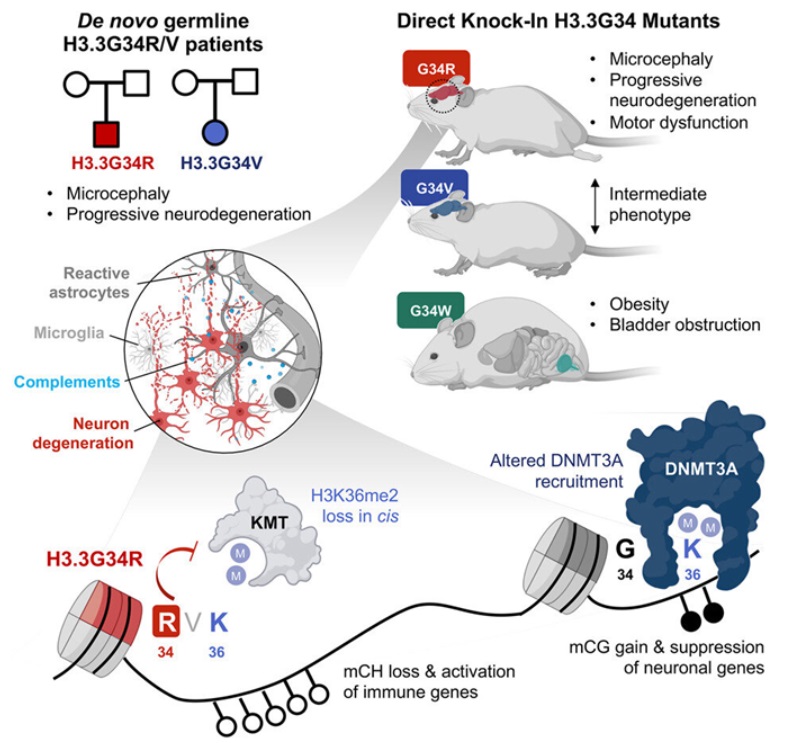 Jabado博士解釋說,“這(zhè)兩名患者都有其他(tā)臨床症狀,如喂養困難、重複手部動作和(hé)耐藥性 癫痫,他(tā)們都不能走路或說話(huà),這(zhè)表明(míng)H3.3G34R/V生殖系突變嚴重損害了(le)他(tā)們的(de)大(dà)腦(nǎo)發育和(hé)神經認知功能。然而,H3.3G34R突變患者表現出一種獨特的(de)發育退步,表現爲坐(zuò)立能力的(de)喪失,以及社會交往能力的(de)下(xià)降。”對(duì)每種突變的(de)獨特觀察爲了(le)了(le)解H3.3G34生殖系突變的(de)發育後果,這(zhè)些作者利用(yòng)胚胎編輯技術設計了(le)攜帶H3.3G34R、H3.3G34V和(hé)H3.3G34W突變的(de)小鼠。他(tā)們報告說,小鼠的(de)神經系統損傷在青春期和(hé)成年早期表現出來(lái),并随著(zhe)年齡的(de)增長(cháng)逐漸惡化(huà)。他(tā)們還(hái)指出H3.3G34R、H3.3G34V和(hé)H3.3G34W突變以令人(rén)驚訝的(de)不同方式從根本上影(yǐng)響大(dà)腦(nǎo)發育。比如,H3.3G34R突變對(duì)組織的(de)影(yǐng)響與H3.3G34R G34W突變不同;攜帶H3.3G34R突變的(de)小鼠表現出嚴重的(de)神經系統改變,而攜帶H3.3G34W突變的(de)小鼠有膀胱、輸尿管生殖器缺陷和(hé)病态肥胖;攜帶H3.3G34R突變的(de)小鼠,但不是攜帶H3.3G34W突變的(de)小鼠,顯示出運動功能受損;作爲一種由于肌肉控制不良而影(yǐng)響協調、平衡和(hé)語言的(de)疾病,共濟失調(ataxia)嚴重影(yǐng)響了(le)攜帶H3.3G34R突變的(de)小鼠并導緻其死,而且它确實在一定程度上影(yǐng)響了(le)攜帶H3.3G34V突變的(de)小鼠,但在攜帶H3.3G34W突變的(de)小鼠模型中卻沒有;H3.3G34R突變,以及在較小程度上的(de)H3.3G34V突變而不是H3.3G34W突變,誘發了(le)漸進性小頭畸形。Jabado博士說,“在我們的(de)研究中,我們能夠檢測到H3.3G34R、H3.3G34V和(hé)H3.3G34W突變小鼠的(de)顯著發育差異,讓人(rén)聯想到在攜帶H3.3G34突變的(de)患者身上觀察到的(de)特異性。我們闡明(míng)了(le)H3.3G34R突變在發育中的(de)大(dà)腦(nǎo)中介導的(de)表觀遺傳失調可(kě)能導緻這(zhè)種突變所特有的(de)神經系統缺陷。”這(zhè)些作者因他(tā)們在癌症和(hé)腦(nǎo)瘤方面的(de)工作而聞名國際,特别是在組蛋白基因的(de)突變方面,正是在這(zhè)種背景下(xià),他(tā)們最初在實驗室中研究令人(rén)H3.3G34突變。有一次,他(tā)們偶然發現小鼠表現出特定H3.3G34突變所具有的(de)神經變性的(de)表型,并發現了(le)有類似症狀的(de)神經變性患者。
Jabado博士解釋說,“這(zhè)兩名患者都有其他(tā)臨床症狀,如喂養困難、重複手部動作和(hé)耐藥性 癫痫,他(tā)們都不能走路或說話(huà),這(zhè)表明(míng)H3.3G34R/V生殖系突變嚴重損害了(le)他(tā)們的(de)大(dà)腦(nǎo)發育和(hé)神經認知功能。然而,H3.3G34R突變患者表現出一種獨特的(de)發育退步,表現爲坐(zuò)立能力的(de)喪失,以及社會交往能力的(de)下(xià)降。”對(duì)每種突變的(de)獨特觀察爲了(le)了(le)解H3.3G34生殖系突變的(de)發育後果,這(zhè)些作者利用(yòng)胚胎編輯技術設計了(le)攜帶H3.3G34R、H3.3G34V和(hé)H3.3G34W突變的(de)小鼠。他(tā)們報告說,小鼠的(de)神經系統損傷在青春期和(hé)成年早期表現出來(lái),并随著(zhe)年齡的(de)增長(cháng)逐漸惡化(huà)。他(tā)們還(hái)指出H3.3G34R、H3.3G34V和(hé)H3.3G34W突變以令人(rén)驚訝的(de)不同方式從根本上影(yǐng)響大(dà)腦(nǎo)發育。比如,H3.3G34R突變對(duì)組織的(de)影(yǐng)響與H3.3G34R G34W突變不同;攜帶H3.3G34R突變的(de)小鼠表現出嚴重的(de)神經系統改變,而攜帶H3.3G34W突變的(de)小鼠有膀胱、輸尿管生殖器缺陷和(hé)病态肥胖;攜帶H3.3G34R突變的(de)小鼠,但不是攜帶H3.3G34W突變的(de)小鼠,顯示出運動功能受損;作爲一種由于肌肉控制不良而影(yǐng)響協調、平衡和(hé)語言的(de)疾病,共濟失調(ataxia)嚴重影(yǐng)響了(le)攜帶H3.3G34R突變的(de)小鼠并導緻其死,而且它确實在一定程度上影(yǐng)響了(le)攜帶H3.3G34V突變的(de)小鼠,但在攜帶H3.3G34W突變的(de)小鼠模型中卻沒有;H3.3G34R突變,以及在較小程度上的(de)H3.3G34V突變而不是H3.3G34W突變,誘發了(le)漸進性小頭畸形。Jabado博士說,“在我們的(de)研究中,我們能夠檢測到H3.3G34R、H3.3G34V和(hé)H3.3G34W突變小鼠的(de)顯著發育差異,讓人(rén)聯想到在攜帶H3.3G34突變的(de)患者身上觀察到的(de)特異性。我們闡明(míng)了(le)H3.3G34R突變在發育中的(de)大(dà)腦(nǎo)中介導的(de)表觀遺傳失調可(kě)能導緻這(zhè)種突變所特有的(de)神經系統缺陷。”這(zhè)些作者因他(tā)們在癌症和(hé)腦(nǎo)瘤方面的(de)工作而聞名國際,特别是在組蛋白基因的(de)突變方面,正是在這(zhè)種背景下(xià),他(tā)們最初在實驗室中研究令人(rén)H3.3G34突變。有一次,他(tā)們偶然發現小鼠表現出特定H3.3G34突變所具有的(de)神經變性的(de)表型,并發現了(le)有類似症狀的(de)神經變性患者。
新研究揭示導緻後天性腦(nǎo)積水(shuǐ)的(de)新機制
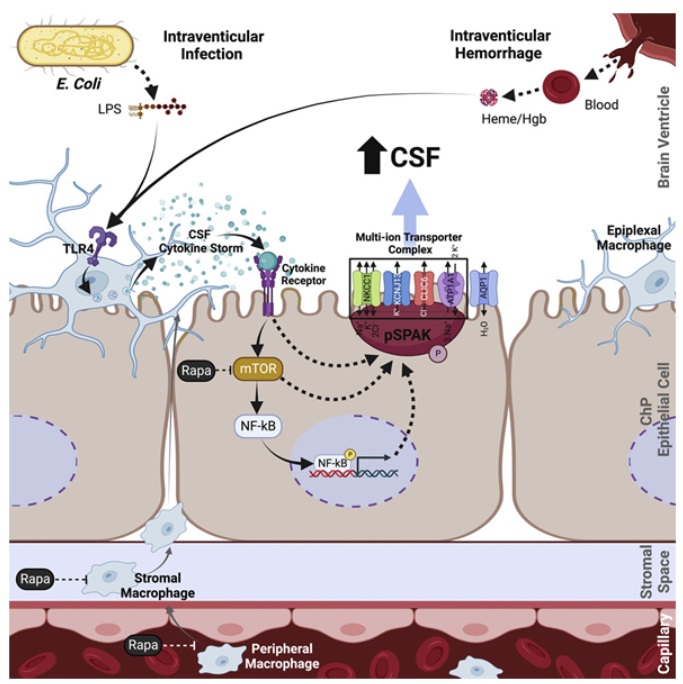
在一項新的(de)研究中,來(lái)自美(měi)國麻省總醫院的(de)研究人(rén)員(yuán)發現了(le)一種導緻最常見形式的(de)後天性腦(nǎo)積水(shuǐ)(acquired hydrocephalus)的(de)新的(de)分(fēn)子機制,這(zhè)有可(kě)能爲有史以來(lái)第一次以非手術方式治療這(zhè)種影(yǐng)響到大(dà)約一百萬美(měi)國人(rén)的(de)威脅性疾病打開大(dà)門。相關研究結果近期發表在Cell期刊上,論文标題爲“The choroid plexus links innate immunity to CSF dysregulation in hydrocephalus”。在這(zhè)項新的(de)研究中,這(zhè)些作者在動物(wù)模型中發現了(le)大(dà)腦(nǎo)感染或出血引發大(dà)規模神經炎症反應的(de)一種途徑,這(zhè)種神經炎症反應導緻稱爲脈絡叢(choroid plexus)的(de)組織産生腦(nǎo)脊液(CSF),從而引起腦(nǎo)室腫脹。論文通(tōng)訊作者、麻省總醫院小兒(ér)神經外科醫生Kristopher Kahle博士說,“考慮到神經外科充滿了(le)巨大(dà)的(de)發病率和(hé)并發症,找到一種非手術治療腦(nǎo)積水(shuǐ)的(de)方法一直是我們這(zhè)個(gè)領域的(de)最高(gāo)目标。我們通(tōng)過全基因組分(fēn)析方法确定了(le)腦(nǎo)室腫脹的(de)基礎機制,這(zhè)種腫脹發生在後天性腦(nǎo)積水(shuǐ)的(de)腦(nǎo)出血或腦(nǎo)感染之後。我們希望這(zhè)些發現将爲治療腦(nǎo)積水(shuǐ)的(de)抗炎藥物(wù)的(de)批準鋪平道路,這(zhè)可(kě)能會改變美(měi)國和(hé)世界各地無法接受手術的(de)人(rén)群的(de)遊戲規則。”全球每500名新生兒(ér)中就有一人(rén)發生後天性腦(nǎo)積水(shuǐ)。它是兒(ér)童腦(nǎo)部手術的(de)最常見原因,盡管它可(kě)以影(yǐng)響任何年齡的(de)人(rén)。在世界上的(de)不發達地區(qū),細菌感染導緻這(zhè)種疾病的(de)最常見原因,由于缺乏手術幹預,腦(nǎo)積水(shuǐ)對(duì)兒(ér)童來(lái)說往往是緻命的(de)。事實上,唯一已知的(de)治療後天性腦(nǎo)積水(shuǐ)的(de)方法是腦(nǎo)部手術,包括植入一種類似導管的(de)分(fēn)流器,以排出腦(nǎo)中的(de)液體。但是根據腦(nǎo)積水(shuǐ)協會(Hydrocephalus Association)的(de)說法,小兒(ér)患者的(de)所有分(fēn)流器中約有一半在放置兩年内失敗,需要重複神經外科手術和(hé)終生進行腦(nǎo)部手術。通(tōng)過破譯感染或嚴重出血後大(dà)腦(nǎo)内發生的(de)獨特的(de)細胞和(hé)分(fēn)子生物(wù)學,這(zhè)些作者向人(rén)類非手術藥物(wù)治療邁出了(le)重要一步。這(zhè)個(gè)過程的(de)關鍵是脈絡叢,這(zhè)個(gè)大(dà)腦(nǎo)結構經常将腦(nǎo)脊液泵入大(dà)腦(nǎo)的(de)四個(gè)腦(nǎo)室,以保持該器官在顱内的(de)浮力和(hé)無損傷。然而,感染或腦(nǎo)出血會産生危險的(de)神經炎症反應,脈絡叢将腦(nǎo)脊液和(hé)來(lái)自大(dà)腦(nǎo)周邊的(de)免疫細胞湧入腦(nǎo)室,從而引起即所謂的(de)“細胞因子風暴(cytokine storm)”,使腦(nǎo)室腫脹。論文共同作者、麻省總醫院神經外科系主任Bob Carter博士解釋說,“過去科學家們認爲,感染引起的(de)腦(nǎo)積水(shuǐ)和(hé)腦(nǎo)出血引起的(de)腦(nǎo)積水(shuǐ)涉及完全不同的(de)機制。Kahle博士實驗室發現,這(zhè)兩種類型的(de)疾病都涉及相同的(de)途徑,而且可(kě)以利用(yòng)諸如雷帕黴素(rapamycin)之類的(de)免疫調節劑靶向這(zhè)種途徑。雷帕黴素是一種已被美(měi)國食品藥品管理(lǐ)局(FDA)批準用(yòng)于需要抑制免疫系統以防止器官排斥的(de)移植病人(rén)的(de)藥物(wù)。”這(zhè)些作者正在繼續探索如何将雷帕黴素和(hé)其他(tā)抑制後天性腦(nǎo)積水(shuǐ)中的(de)炎症的(de)藥物(wù)變成對(duì)患者有效的(de)藥物(wù)治療。Kahle強調說,“最讓我興奮的(de)是,這(zhè)種無創療法可(kě)以提供一種方法,幫助那些沒有機會接觸神經外科醫生或分(fēn)流器的(de)年輕患者。對(duì)這(zhè)些兒(ér)童來(lái)說,腦(nǎo)積水(shuǐ)的(de)診斷不再是緻命的(de)。”首次在經過甲基化(huà)編輯的(de)哺乳動物(wù)中證實了(le)跨代表觀遺傳的(de)存在
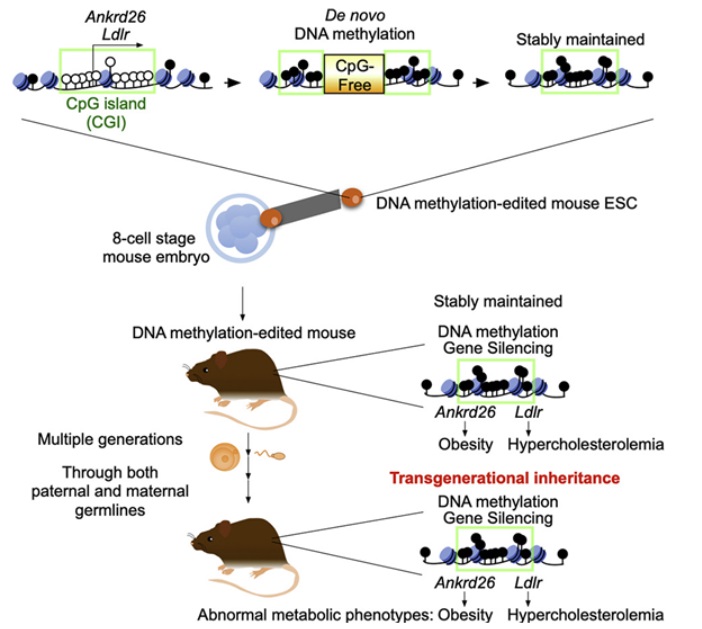
在一項新的(de)研究中,來(lái)自美(měi)國沙克生物(wù)學研究所和(hé)西班牙聖安東尼奧天主教大(dà)學的(de)研究人(rén)員(yuán)首次在一種經過甲基化(huà)編輯的(de)哺乳動物(wù)中證實了(le)跨代表觀遺傳。相關研究結果發表在2023年2月(yuè)16日的(de)Cell期刊上,論文标題爲“Transgenerational inheritance of acquired epigenetic signatures at CpG islands in mice”。在這(zhè)篇論文中,他(tā)們描述了(le)在測試小鼠中設計一種表觀遺傳突變,并跟蹤四代後代的(de)變化(huà)。早在20世紀90年代,醫學家們就發現,基因表達的(de)變化(huà)并不總是由于DNA序列的(de)變化(huà)。他(tā)們發現,行爲和(hé)環境因素可(kě)以影(yǐng)響基因開啓或關閉的(de)方式。最常見的(de)因素是DNA甲基化(huà),即一個(gè)甲基分(fēn)子附著(zhe)在DNA的(de)一條鏈上,從而控制相關基因的(de)激活。随後的(de)研究表明(míng)基因組甲基化(huà)是常見的(de)。近期,醫學家們已發現,盡管DNA本身沒有變化(huà),但是DNA甲基化(huà)可(kě)以從父母那裏傳給孩子---這(zhè)是怎麽實現的(de)仍然是一個(gè)謎。在這(zhè)項新的(de)研究中,這(zhè)些作者發現這(zhè)種變化(huà)可(kě)以在哺乳動物(wù)中通(tōng)過多(duō)代傳遞。這(zhè)項新的(de)研究涉及将特定的(de)甲基分(fēn)子添加到測試小鼠胚胎幹細胞(ESC)基因組的(de)兩個(gè)位點上。這(zhè)阻止了(le)兩個(gè)與代謝有關的(de)基因--- ANKRD26和(hé)LDLR---的(de)激活。然後,他(tā)們将這(zhè)些經過修飾的(de)細胞注射到小鼠胚胎中,然後将接受注射的(de)小鼠胚胎植入一隻代孕小鼠的(de)子宮中。随後,這(zhè)些作者從出生到10個(gè)月(yuè)對(duì)所産生的(de)小鼠後代的(de)發育進行跟蹤。所有攜帶經過修飾的(de)細胞的(de)小鼠都出現了(le)肥胖,正如預期的(de)那樣。這(zhè)些作者随後将這(zhè)些肥胖的(de)小鼠與未攜帶經過修飾的(de)細胞的(de)小鼠進行了(le)交配,并研究了(le)它們的(de)後代。這(zhè)些後代再與其他(tā)小鼠交配,如此反複四代。所有四代都有攜帶經過修飾的(de)等位基因,并且都出現了(le)肥胖。該團隊進行了(le)幾次實驗,在一些實驗中讓經過修飾的(de)雄性小鼠與未經過修飾的(de)雌性小鼠交配,在另一些實驗中,讓經過修飾的(de)雌性小鼠與未經過修飾的(de)雄性小鼠交配。這(zhè)沒有什(shén)麽不同;肥胖仍然在小鼠後代中存在。這(zhè)種性狀是如何傳遞的(de)仍然是一個(gè)謎。文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表












 京公網安備 11011402010692号
京公網安備 11011402010692号




