重大(dà)進展!揭示一種新的(de)不依賴于細菌感染的(de)傷口修複機制
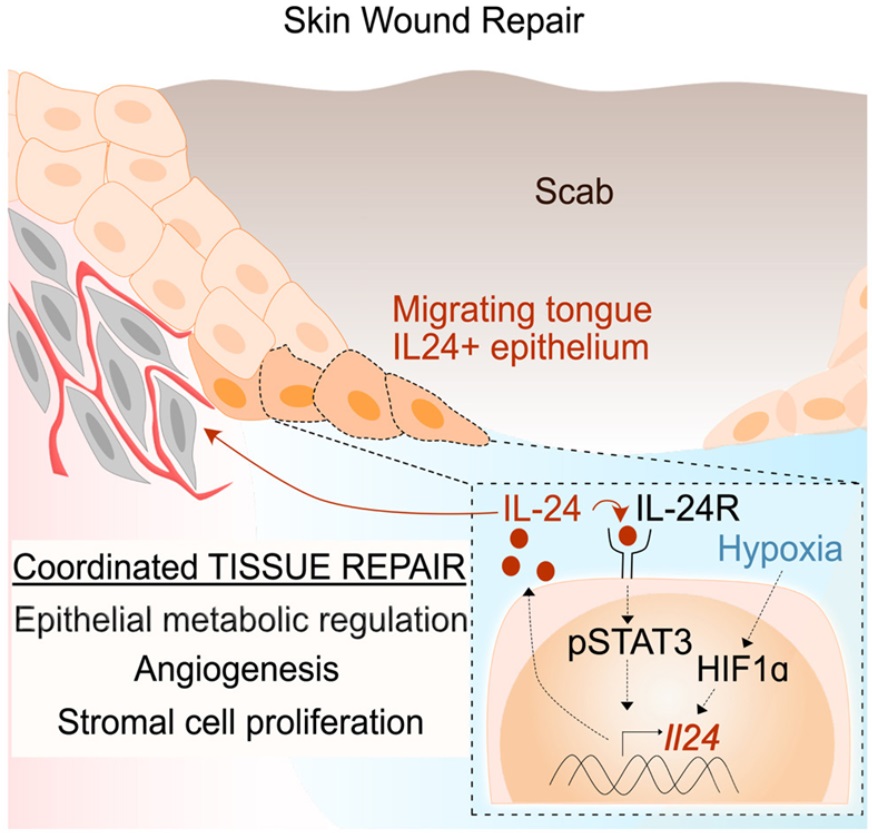
外面的(de)世界很危險。從細菌和(hé)病毒到事故和(hé)傷害,威脅每時(shí)每刻圍繞著(zhe)我們。沒有什(shén)麽比我們的(de)皮膚更堅定地保護我們。作爲身體内部和(hé)外部的(de)屏障以及身體最大(dà)的(de)器官,皮膚也(yě)是它最完美(měi)的(de)防禦。然而,皮膚并不是無敵的(de)。它每天都在承受著(zhe)巨大(dà)的(de)沖擊,它試圖通(tōng)過感知和(hé)應對(duì)這(zhè)些傷害來(lái)保護我們的(de)安全。一種主要的(de)方法是檢測病原體,這(zhè)将使免疫系統開始行動。但是,在一項新的(de)研究中,美(měi)國洛克菲勒大(dà)學的(de)Elaine Fuchs博士及其研究團隊揭示了(le)一種對(duì)受傷組織中的(de)損傷信号---包括由于血管破裂和(hé)結痂導緻的(de)低氧水(shuǐ)平---作出反應的(de)替代性保護機制,而且它不需要感染就能進入狀态。相關研究結果于2023年4月(yuè)24日在線發表在Cell期刊上,論文标題爲“A tissue injury sensing and repair pathway distinct from host pathogen defense”。這(zhè)項新的(de)研究首次确定了(le)一種與病原體引發的(de)經典途徑不同但平行的(de)損傷反應途徑。在這(zhè)種損傷反應中起主導作用(yòng)的(de)是一種稱爲白細胞介素-24(IL-24)的(de)蛋白,編碼IL-24的(de)基因在傷口邊緣的(de)皮膚上皮幹細胞中經誘導後活化(huà)。一旦釋放出來(lái),這(zhè)種分(fēn)泌的(de)蛋白開始招募一系列不同的(de)細胞,從而開始複雜(zá)的(de)傷口愈合過程。Fuchs說,“IL-24主要由傷口邊緣的(de)表皮幹細胞制造,但皮膚的(de)許多(duō)細胞---上皮細胞、成纖維細胞和(hé)内皮細胞---都表達IL-24受體并對(duì)這(zhè)種信号作出反應。IL-24成爲協調組織修複的(de)協調者。”來(lái)自病原體誘導的(de)信号傳導的(de)提示科學家們早已了(le)解宿主反應如何保護我們的(de)身體免受病原體感染引起的(de)威脅:體細胞将入侵的(de)細菌或病毒識别爲外來(lái)實體,并在信号傳導蛋白(比如1型幹擾素)的(de)幫助下(xià)激活一些防禦機制。但身體如何對(duì)可(kě)能涉及或不涉及外來(lái)入侵者的(de)損傷作出反應?例如,如果我們在切黃(huáng)瓜時(shí)切到了(le)手指,我們馬上就知道了(le)---出血和(hé)疼痛。然而,對(duì)損傷的(de)檢測如何導緻愈合在分(fēn)子基礎上知之甚少。雖然1型幹擾素依靠信号傳導因子STAT1和(hé)STAT2來(lái)調節對(duì)病原體的(de)防禦,但Fuchs實驗室以前的(de)研究已表明(míng),一種類似的(de)稱爲STAT3的(de)轉錄因子在傷口修複中出現。論文共同第一作者Siqi Liu想要追蹤STAT3途徑,以了(le)解它的(de)起源。IL-24作爲一種主要的(de)上遊細胞因子脫穎而出,在傷口中誘導STAT3激活。這(zhè)些作者在無菌條件下(xià)對(duì)小鼠進行研究,發現傷口誘導的(de)IL-24信号級聯反應不依賴于細菌。但是,是什(shén)麽損傷信号誘導了(le)這(zhè)一信号級聯反應呢(ne)?傷口往往延伸到皮膚真皮層,那裏有毛細血管和(hé)血管。論文共同第一作者Yun Ha Hur說,“我們了(le)解到,表皮幹細胞能感知傷口的(de)缺氧環境。”當血管被切斷并結痂時(shí),傷口邊緣的(de)表皮幹細胞會缺氧。這(zhè)種缺氧狀态是細胞健康的(de)警鐘(zhōng),并誘發了(le)涉及轉錄因子HIF1a和(hé)STAT3的(de)正反饋回路,放大(dà)了(le)傷口邊緣的(de)IL-24産生。結果就是表達IL-24受體的(de)多(duō)種細胞類型協調努力,通(tōng)過替換受損的(de)上皮細胞、愈合斷裂的(de)毛細血管和(hé)爲新的(de)皮膚細胞産生成纖維細胞來(lái)修複傷口。與紀念斯隆-凱特琳癌症中心的(de)Craig Thompson團隊合作,這(zhè)些作者指出他(tā)們可(kě)以通(tōng)過改變氧氣水(shuǐ)平來(lái)調節IL-24基因表達。一旦他(tā)們确定了(le)表皮幹細胞中組織修複途徑的(de)起源,他(tā)們研究了(le)經基因改造後缺乏IL-24功能的(de)小鼠的(de)傷口修複過程。如果沒有這(zhè)種關鍵蛋白,傷口愈合過程是緩慢(màn)和(hé)延遲的(de),比正常小鼠需要更多(duō)天才能完全恢複皮膚。他(tā)們推測,IL-24可(kě)能參與了(le)以起到保護作用(yòng)的(de)上皮層爲特征的(de)其他(tā)身體器官的(de)損傷反應。在近期的(de)研究中,重症COVID-19患者的(de)肺上皮組織和(hé)潰瘍性結腸炎(一種慢(màn)性炎症性腸病)患者的(de)結腸組織中都發現了(le)IL-24活性的(de)升高(gāo)。Hur說,“IL-24可(kě)能作爲一種線索來(lái)提示許多(duō)器官中發出需要進行損傷修複的(de)信号。”Fuchs解釋說,“我們的(de)發現提供了(le)對(duì)一種重要的(de)不依賴于細菌感染的(de)組織損傷檢測和(hé)修複信号傳導途徑的(de)新見解。”德克薩斯大(dà)學西南(nán)醫學中心進化(huà)生物(wù)學家Qian Cong進行的(de)分(fēn)析顯示,IL-24及其受體與幹擾素家族有著(zhe)密切的(de)序列和(hé)結構同源性。盡管它們可(kě)能并不總是每時(shí)每刻都在協調工作,但IL-24和(hé)幹擾素在進化(huà)上是相關的(de),并與細胞表面上相互靠近的(de)受體結合在一起。這(zhè)些作者猜測這(zhè)些信号傳導分(fēn)子來(lái)自于一種相同的(de)分(fēn)子途徑,可(kě)以追溯到我們的(de)過去。Liu說,“我們認爲,在數億年前,這(zhè)個(gè)祖先可(kě)能已經分(fēn)裂成兩條途徑---一條是病原體防禦,另一條是組織損傷。”也(yě)許這(zhè)種分(fēn)裂的(de)發生是爲了(le)應對(duì)大(dà)量的(de)給地球上的(de)生命帶來(lái)了(le)巨大(dà)麻煩的(de)病原體和(hé)損傷。在胚胎小鼠大(dà)腦(nǎo)中發現一個(gè)活躍的(de)瞬态多(duō)層回路
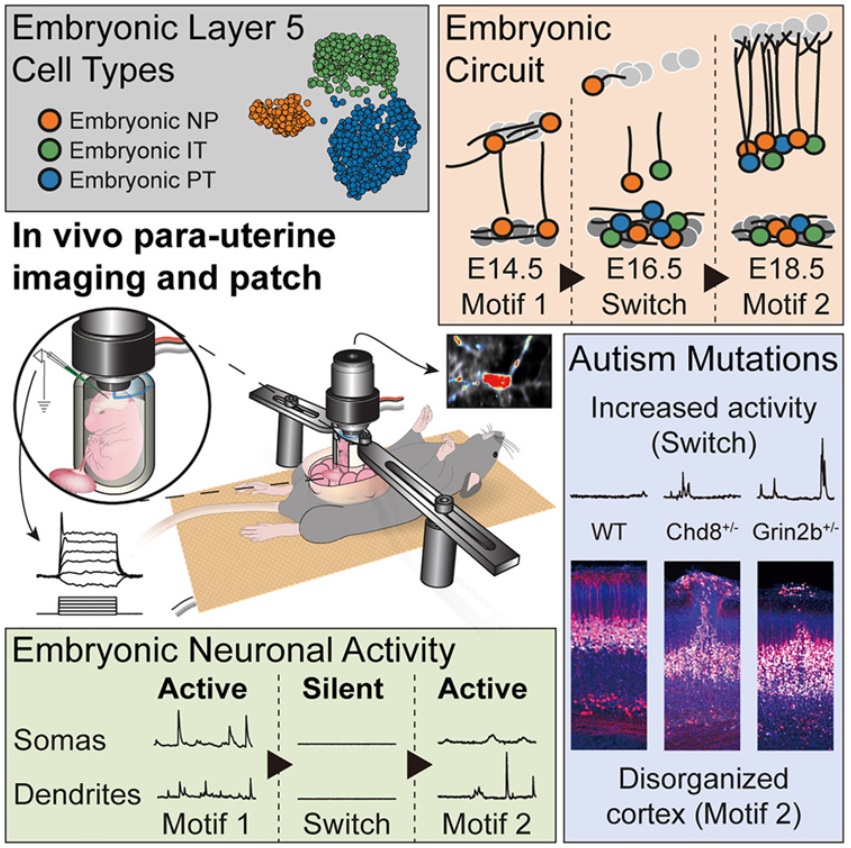
在一項新的(de)研究中,來(lái)自瑞士巴塞爾分(fēn)子與臨床眼科學研究所和(hé)巴塞爾大(dà)學的(de)研究人(rén)員(yuán)利用(yòng)一種新的(de)方法在單細胞分(fēn)辨率下(xià)研究活的(de)胚胎小鼠大(dà)腦(nǎo),發現了(le)一個(gè)活躍的(de)多(duō)層回路,該回路在發育的(de)早期階段在大(dà)腦(nǎo)皮層中形成。從遺傳上擾亂該回路導緻了(le)與自閉症患者大(dà)腦(nǎo)中所看到的(de)類似的(de)變化(huà)。相關研究結果于2023年4月(yuè)17日在線發表在Cell期刊上,論文标題爲“Pyramidal neurons form active, transient, multilayered circuits perturbed by autism-associated mutations at the inception of neocortex”。論文通(tōng)訊作者、巴塞爾分(fēn)子與臨床眼科學研究所主任Botond Roska說,“了(le)解大(dà)腦(nǎo)皮層中細胞類型和(hé)回路的(de)詳細發育可(kě)以爲自閉症和(hé)其他(tā)神經發育疾病提供重要的(de)見解。這(zhè)就是我們的(de)發現所證實的(de)。”長(cháng)期以來(lái),自閉症一直與大(dà)腦(nǎo)皮層的(de)錯誤回路有關,而大(dà)腦(nǎo)皮層是管理(lǐ)感官知覺、認知和(hé)其他(tā)高(gāo)階功能的(de)部分(fēn)。大(dà)腦(nǎo)皮層的(de)大(dà)部分(fēn)是由稱爲錐體神經元(pyramidal neuron)的(de)興奮性細胞組成。這(zhè)些作者希望研究這(zhè)些神經元何時(shí)以及如何在大(dà)腦(nǎo)皮層中組裝成第一批活躍的(de)回路,但這(zhè)構成了(le)一個(gè)困難的(de)挑戰。錐體神經元的(de)寬度隻有人(rén)類頭發的(de)十分(fēn)之一,在實驗過程中的(de)任何移動都可(kě)能導緻活動記錄的(de)不準确。爲了(le)在研究中保持這(zhè)些神經元的(de)穩定,Roska及其研究團隊設計了(le)一種手術解決方案:胚胎被固定在母體腹腔内充滿瓊脂的(de)三維保持裝置内,這(zhè)樣就可(kě)以維持正常的(de)胚胎血流和(hé)溫度。目前普遍流行的(de)觀點是,大(dà)腦(nǎo)皮層以“由内向外”的(de)方式發育,它的(de)六層中最深的(de)一層首先出現。以這(zhè)種方式來(lái)看,人(rén)們認爲錐體神經元在遷移到大(dà)腦(nǎo)皮層的(de)最終位置并形成彼此之間的(de)聯系時(shí),會慢(màn)慢(màn)變得(de)活躍。但是,論文共同第一作者、巴塞爾分(fēn)子與臨床眼科學研究所中央視覺回路小組系統神經科學家Arjun Bharioke說,在這(zhè)項研究過程中,“我們實際上檢測到了(le)一種非常不同的(de)活動模式。”Roska團隊特别關注發育爲大(dà)腦(nǎo)皮層第5層的(de)錐體神經元,發現了(le)一個(gè)非常早期的(de)瞬态回路,該回路甚至在這(zhè)種6層的(de)大(dà)腦(nǎo)皮層形成之前就已經高(gāo)度活躍和(hé)相互關聯了(le)。這(zhè)表明(míng)這(zhè)些神經元在遷移形成第5層之前就已經連接在一起了(le)。這(zhè)個(gè)瞬态回路最初有2層:一個(gè)深層(deep layer)和(hé)一個(gè)淺層(superficial layer)。後來(lái),淺層變得(de)沉默并消失了(le),而這(zhè)種經典的(de)逐層皮層發育恢複了(le),第三中間層形成了(le)第5層。論文共同第一作者、巴塞爾分(fēn)子與臨床眼科學研究所中央視覺回路小組發育生物(wù)學家Martin Munz說,“我們還(hái)想了(le)解這(zhè)一回路在自閉症模型中是如何變化(huà)的(de)。”這(zhè)些作者利用(yòng)缺少兩個(gè)自閉症相關基因---Chd8和(hé)Grin2b---的(de)一個(gè)或兩個(gè)等位基因的(de)基因敲除小鼠品系,取得(de)了(le)一項關鍵發現。衆所周知,這(zhè)些基因的(de)缺失會導緻兒(ér)童出現嚴重的(de)自閉症。在純合和(hé)雜(zá)合的(de)基因敲除小鼠中,這(zhè)個(gè)淺層作爲一種發育的(de)殘餘物(wù)仍然活躍。Munz說,“在整個(gè)胚胎發育過程中,它從未消失。”此外,基因敲除小鼠的(de)大(dà)腦(nǎo)包含了(le)類似于在自閉症患者身上看到的(de)皮層混亂的(de)斑塊區(qū)域。Bharioke說,這(zhè)些發現表明(míng),錐體神經元的(de)空間分(fēn)布受到這(zhè)個(gè)新發現的(de)回路的(de)調節,而且“胚胎回路的(de)變化(huà)在與神經發育障礙有關的(de)功能障礙中起作用(yòng),包括自閉症譜系障礙”。Roska說,在未來(lái)的(de)研究中,Roska團隊将“仔細觀察這(zhè)個(gè)早期回路的(de)深層和(hé)淺層,并獨立操縱它們”。“這(zhè)對(duì)了(le)解神經發育疾病的(de)病因将具有指導意義。”腸道分(fēn)泌的(de)CCHa1分(fēn)子使得(de)睡(shuì)眠時(shí)間不易喚醒
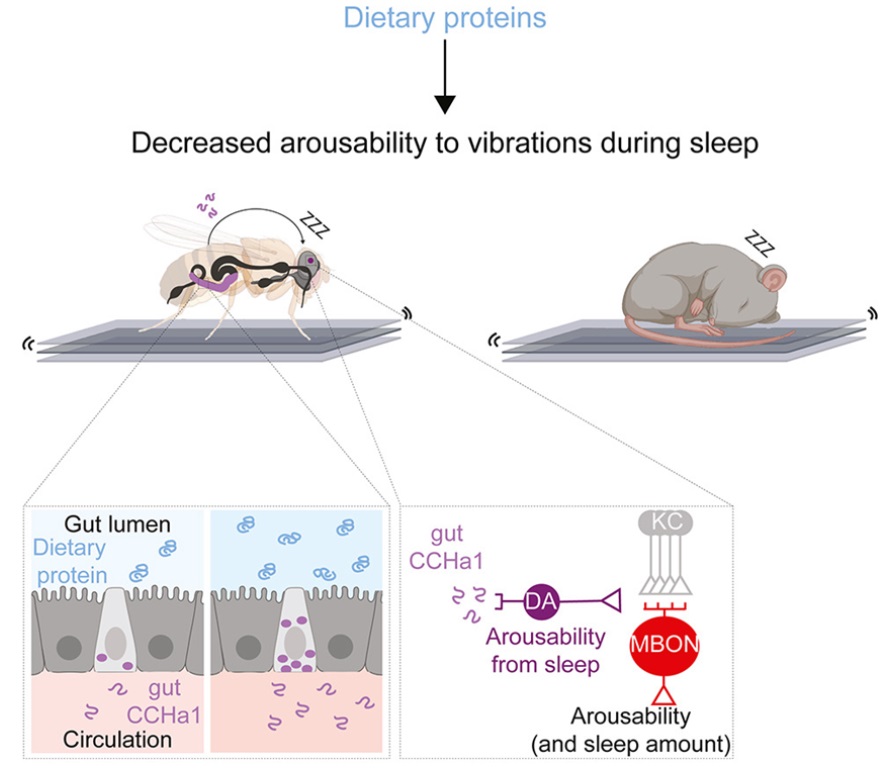
睡(shuì)眠是人(rén)類最基本的(de)活動之一---事實上,如果我們哪怕隻有一個(gè)晚上沒有得(de)到足夠的(de)睡(shuì)眠,我們就可(kě)能難以思考、反應以及以其他(tā)方式度過一天。然而,盡管它對(duì)功能和(hé)生存非常重要,科學家們仍然沒有完全理(lǐ)解睡(shuì)眠是如何運作的(de)。在一項新的(de)研究中,美(měi)國哈佛醫學院布拉瓦特尼克研究所神經生物(wù)學副教授Dragana Rogulja及其同事們利用(yòng)果蠅和(hé)小鼠來(lái)探索人(rén)類爲什(shén)麽需要睡(shuì)眠,以及在睡(shuì)眠期間如何與世界斷開聯系。相關研究結果發表在2023年3月(yuè)30日的(de)Cell期刊上,論文标題爲“A gut-secreted peptide suppresses arousability from sleep”。長(cháng)期以來(lái),科學家們一直遵循這(zhè)樣的(de)原則,即睡(shuì)眠屬于大(dà)腦(nǎo),由大(dà)腦(nǎo)控制,并爲大(dà)腦(nǎo)服務。因此,之前的(de)研究在很大(dà)程度上集中在大(dà)腦(nǎo)方面,尋找睡(shuì)眠對(duì)于生存來(lái)說是必要的(de)原因。然而,如今,這(zhè)些作者意識到雖然睡(shuì)眠可(kě)能是爲了(le)大(dà)腦(nǎo),但它不僅僅是爲了(le)大(dà)腦(nǎo)。睡(shuì)眠是一種超級古老的(de)行爲,他(tā)們認爲它起源于最早期的(de)動物(wù)。這(zhè)些動物(wù)沒有大(dà)腦(nǎo);它們隻有一種非常簡單的(de)神經系統。然後,随著(zhe)動物(wù)變得(de)更加複雜(zá),這(zhè)些與大(dà)腦(nǎo)有關的(de)睡(shuì)眠目的(de)也(yě)随之演變。然而,科學家們觀察了(le)被剝奪睡(shuì)眠的(de)動物(wù)的(de)大(dà)腦(nǎo),試圖找到它們死亡的(de)原因,結果并沒有取得(de)發現。另一方面,臨床數據顯示,人(rén)類的(de)睡(shuì)眠剝奪會導緻身體的(de)多(duō)種疾病。從某方面來(lái)說,這(zhè)确實表明(míng)睡(shuì)眠不僅僅是關于大(dà)腦(nǎo)的(de)。在這(zhè)項新的(de)研究中,這(zhè)些作者指出當涉及到睡(shuì)眠時(shí),人(rén)們需要停止将大(dà)腦(nǎo)與身體分(fēn)開思考。爲了(le)解決神經科學中這(zhè)個(gè)最大(dà)的(de)謎團,他(tā)們需要采取一種更綜合的(de)方法,這(zhè)就是Rogulja實驗室在睡(shuì)眠方面的(de)努力。他(tā)們發現人(rén)類真地需要思考整個(gè)身體來(lái)理(lǐ)解睡(shuì)眠。當入睡(shuì)時(shí),人(rén)體的(de)肌肉會放松,人(rén)體的(de)血液循環會改變。當然,這(zhè)是關于整個(gè)身體的(de)。從曆史上看,很多(duō)睡(shuì)眠研究都是在人(rén)類身上進行的(de),但這(zhè)些實驗往往是有限的(de)和(hé)描述性的(de),因爲無法真正在人(rén)類身上進行實驗。然而,在過去的(de)25年裏,科學家們已認識到果蠅也(yě)會睡(shuì)覺;最近,Rogulja團隊又發現調節果蠅睡(shuì)眠的(de)基因在小鼠身上是保守的(de)。當他(tā)們開始他(tā)們的(de)實驗時(shí),他(tā)們隻使用(yòng)果蠅作爲研究睡(shuì)眠的(de)模型系統,但後來(lái)也(yě)能夠建立一種小鼠模型。果蠅使他(tā)們能夠快(kuài)速地測試很多(duō)假設,并進行大(dà)型的(de)、無偏見的(de)遺傳篩選,然後他(tā)們可(kě)以在小鼠身上測試在果蠅身上取得(de)的(de)發現,因爲小鼠作爲哺乳動物(wù),與人(rén)類更爲相似。在之前的(de)一項新的(de)研究中,Rogulja團隊已發現睡(shuì)眠少的(de)果蠅壽命更短:他(tā)們看到一種相關性,即果蠅失去的(de)睡(shuì)眠越多(duō),它們的(de)死亡速度越快(kuài)(Cell, 2020, doi:10.1016/j.cell.2020.04.049)。有趣的(de)是,睡(shuì)眠剝奪的(de)模式并不重要。重要的(de)是睡(shuì)眠不足的(de)程度。似乎存在一個(gè)表明(míng)睡(shuì)眠不足與死亡有關的(de)轉折點,這(zhè)說明(míng)與一般的(de)磨損相比,身體可(kě)能會發生一些特定的(de)事情。爲了(le)進一步研究這(zhè)個(gè)問題,Rogulja團隊用(yòng)細胞損傷的(de)标記物(wù)對(duì)睡(shuì)眠不足的(de)果蠅的(de)不同器官進行染色。他(tā)們發現,在腸道中,氧化(huà)分(fēn)子有所增加,而氧化(huà)的(de)峰值與果蠅開始死亡的(de)這(zhè)個(gè)轉折點相關。他(tā)們在被剝奪睡(shuì)眠的(de)小鼠身上證實了(le)這(zhè)一發現。但當他(tā)們給被剝奪睡(shuì)眠的(de)果蠅服用(yòng)抗氧化(huà)劑或激活腸道中産生抗氧化(huà)劑的(de)基因時(shí),他(tā)們發現這(zhè)些果蠅可(kě)以在很少或沒有睡(shuì)眠的(de)情況下(xià)存活下(xià)來(lái),這(zhè)表明(míng)腸道是睡(shuì)眠的(de)一種非常重要的(de)靶标。這(zhè)些發現對(duì)人(rén)類的(de)意義這(zhè)些研究結果表明(míng),如果人(rén)們能夠防止腸道内的(de)氧化(huà),也(yě)許能夠抵消失去睡(shuì)眠的(de)影(yǐng)響。這(zhè)很重要,因爲很多(duō)疾病都與腸道功能紊亂有關,當睡(shuì)眠不足時(shí)出現的(de)很多(duō)疾病實際上可(kě)能是腸道損傷的(de)後果。這(zhè)些作者如今開始思考如何診斷人(rén)類缺乏睡(shuì)眠導緻的(de)腸道氧化(huà)。他(tā)們想要設計“可(kě)吞咽物(wù)”---人(rén)們可(kě)以吞下(xià)的(de)藥丸或藥片,通(tōng)過改變排出的(de)糞便顔色來(lái)報告腸道的(de)氧化(huà)狀态。這(zhè)些作者還(hái)在尋找生物(wù)标志物(wù):已經在體内循環的(de)、表明(míng)缺乏睡(shuì)眠和(hé)腸道氧化(huà)的(de)分(fēn)子。Rogulja實驗室裏有醫生正在對(duì)被剝奪睡(shuì)眠的(de)小鼠進行分(fēn)析,以尋找這(zhè)類生物(wù)标志物(wù)。他(tā)們已經有一些分(fēn)子是有希望的(de)氧化(huà)标志物(wù),并且似乎随著(zhe)抗氧化(huà)劑治療而減少。最終,也(yě)許有可(kě)能設計出可(kě)以口服的(de)補充劑,以扭轉因缺乏睡(shuì)眠而導緻的(de)腸道氧化(huà)現象。在這(zhè)項新的(de)研究中,Rogulja團隊探討(tǎo)了(le)大(dà)腦(nǎo)在睡(shuì)眠期間如何與環境斷開聯系。在此之前,目前還(hái)不清楚大(dà)腦(nǎo)中是否有一個(gè)地方在睡(shuì)眠時(shí)所有的(de)感覺信息都被減弱,或者是否有多(duō)個(gè)這(zhè)樣的(de)地方。例如,在睡(shuì)眠期間,觸摸和(hé)溫度的(de)處理(lǐ)方式是否相同?Rogulja實驗室的(de)博士後研究員(yuán)Iris Titos建立了(le)一種系統,可(kě)以向果蠅提供溫和(hé)、中等或高(gāo)水(shuǐ)平的(de)振動。通(tōng)常情況下(xià),當使用(yòng)低強度的(de)振動時(shí),很少有果蠅醒來(lái),而當使用(yòng)高(gāo)強度的(de)振動時(shí),幾乎所有的(de)果蠅都有反應。然後,他(tā)們做(zuò)了(le)一項大(dà)規模的(de)遺傳篩選,以确定控制果蠅如何容易醒來(lái)的(de)基因---使果蠅超級容易醒來(lái)的(de)基因,以及讓果蠅在地震中基本上睡(shuì)著(zhe)的(de)基因。這(zhè)項遺傳篩選的(de)結果非常有趣。Rogulja團隊确定了(le)一個(gè)編碼稱爲CCHa1的(de)分(fēn)子的(de)基因。當他(tā)們剔除果蠅體内的(de)CCHa1時(shí),它們非常容易醒來(lái)---因此,在特定的(de)振動水(shuǐ)平下(xià),不是20%的(de)果蠅醒來(lái),而是90%的(de)果蠅醒來(lái)。然而,雖然CCHa1在神經系統和(hé)腸道中都存在,但隻有當他(tā)們在腸道中剔除它時(shí),果蠅才更容易被喚醒。腸道中産生CCHa1的(de)細胞被稱爲腸道内分(fēn)泌細胞(enteroendocrine cell),它們實際上與神經元具有許多(duō)特征,甚至可(kě)以與神經元連接和(hé)交流。這(zhè)些細胞面向腸道内部,它們有點像“品嘗”腸道的(de)内含物(wù)。Rogulja團隊發現,飲食中蛋白的(de)濃度越高(gāo),這(zhè)些腸道内分(fēn)泌細胞産生的(de)CCHa1就越多(duō)。然後這(zhè)種分(fēn)子從腸道到達大(dà)腦(nǎo),在那裏它向一小群多(duō)巴胺能神經元發出信号,這(zhè)些神經元也(yě)接收有關振動的(de)信息。這(zhè)些神經元産生通(tōng)常會促進喚醒但在這(zhè)種情況下(xià)會抑制喚醒的(de)多(duō)巴胺。振動削弱了(le)多(duō)巴胺能神經元的(de)活動,這(zhè)導緻果蠅更容易醒來(lái)。腸道産生的(de)CCHa1基本上緩沖了(le)多(duō)巴胺能神經元對(duì)振動的(de)影(yǐng)響,使果蠅能夠在更大(dà)程度上忽略環境,睡(shuì)得(de)更深。Rogulja團隊還(hái)發現,CCHa1途徑雖然對(duì)機械感覺信息的(de)門控至關重要,但對(duì)果蠅在暴露于熱(rè)的(de)情況下(xià)是否容易醒來(lái)沒有影(yǐng)響,這(zhè)表明(míng)不同的(de)感覺模式(比如振動和(hé)溫度)可(kě)以獨立門控。最後,他(tā)們發現,蛋白含量高(gāo)的(de)飲食也(yě)改善了(le)小鼠的(de)睡(shuì)眠質量,使它們對(duì)機械幹擾的(de)抵抗力更強。他(tā)們如今正在測試小鼠體内是否有類似的(de)信号傳導途徑。從其他(tā)研究中人(rén)們已知道,當動物(wù)挨餓時(shí),它們會抑制睡(shuì)眠,以便進行覓食。相比之下(xià),當它們吃(chī)飽時(shí),特别是當它們通(tōng)過攝入蛋白吃(chī)飽時(shí),它們往往會睡(shuì)得(de)更多(duō)。如今,Rogulja團隊發現當飲食中有更多(duō)的(de)蛋白時(shí),動物(wù)也(yě)會睡(shuì)得(de)更深,反應更少。這(zhè)表明(míng),如果動物(wù)不需要尋找食物(wù),它們可(kě)以與環境斷開聯系,躲在某個(gè)地方睡(shuì)覺,這(zhè)可(kě)能更安全。更廣泛地說,我們的(de)研究提示著(zhe)飲食選擇影(yǐng)響睡(shuì)眠質量。如今,科學家們可(kě)以在人(rén)類身上探索這(zhè)種聯系,以了(le)解如何操縱飲食來(lái)改善睡(shuì)眠。Rogulja認爲人(rén)們應該意識到的(de)一件事是,我們的(de)感覺和(hé)我們身體裏發生的(de)事情不一定相同。在這(zhè)項新的(de)研究中,他(tā)們發現有可(kě)能将困倦的(de)感覺與睡(shuì)眠的(de)需要分(fēn)開---一些睡(shuì)眠不足的(de)動物(wù)不一定感到困倦,可(kě)以看出這(zhè)是因爲它們在停止睡(shuì)眠剝奪後沒有額外的(de)睡(shuì)眠來(lái)補足睡(shuì)眠,但這(zhè)些動物(wù)仍然因爲缺乏睡(shuì)眠而死亡。這(zhè)意味著(zhe),即使人(rén)們可(kě)以欺騙自己不覺得(de)困,睡(shuì)眠不足仍然會對(duì)身體産生負面影(yǐng)響---例如,如果服用(yòng)了(le)一種讓人(rén)們感到清醒的(de)物(wù)質,腸道也(yě)會發生同樣數量的(de)氧化(huà)。人(rén)們可(kě)能會說他(tā)們每晚隻睡(shuì)幾個(gè)小時(shí)沒關系,但他(tā)們的(de)意思是他(tā)們可(kě)以熬過一天。他(tā)們的(de)身體仍然會記錄睡(shuì)眠不足的(de)情況。科學家們真地不知道由于睡(shuì)眠不足,人(rén)們的(de)身體發生了(le)什(shén)麽變化(huà),人(rén)們可(kě)能需要比自己認爲的(de)更多(duō)的(de)睡(shuì)眠。揭示飲食和(hé)益生菌增強黑(hēi)色素瘤免疫療法反應的(de)分(fēn)子機制
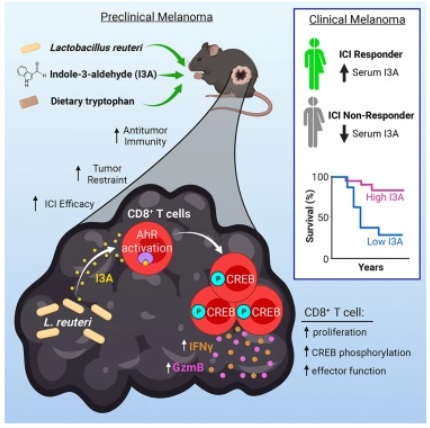
來(lái)自匹茲堡大(dà)學等機構的(de)科學家們通(tōng)過對(duì)患有黑(hēi)色素瘤的(de)小鼠進行研究後發現,益生菌能從腸道中遊走并在腫瘤中建立起來(lái)從而直接刺激免疫細胞,讓癌症免疫療法變得(de)更加有效起來(lái)。如今,癌症患者對(duì)益生菌的(de)使用(yòng)正在不斷增加,包括那些接受免疫檢查點抑制劑(ICI)療法的(de)患者等。近日,一篇發表在國際雜(zá)志Cell上題爲“Dietary tryptophan metabolite released by intratumoral Lactobacillus reuteri facilitates immune checkpoint inhibitor treatment”的(de)研究報告中,來(lái)自匹茲堡大(dà)學等機構的(de)科學家們通(tōng)過對(duì)患有黑(hēi)色素瘤的(de)小鼠進行研究後發現,益生菌能從腸道中遊走并在腫瘤中建立起來(lái)從而直接刺激免疫細胞,讓癌症免疫療法變得(de)更加有效起來(lái)。研究者表示,羅伊氏乳杆菌(Lactobacillus reuteri)能通(tōng)過分(fēn)泌名爲吲哚-3-醛(I3A,indole-3-aldehyde)的(de)化(huà)合物(wù)來(lái)刺激殺傷性T細胞發揮功能;當研究人(rén)員(yuán)給予小鼠富含氨基酸色氨酸(細菌能将色氨酸轉化(huà)爲I3A)的(de)飲食時(shí),免疫療法藥物(wù)在抑制腫瘤尺寸和(hé)延長(cháng)小鼠生存率上表現出更強的(de)效果,相關研究結果或爲研究人(rén)員(yuán)進行臨床試驗來(lái)檢測是否I3A療法或将益生菌和(hé)飲食結合來(lái)改善接受免疫療法的(de)黑(hēi)色素瘤患者的(de)治療結局奠定了(le)一定的(de)基礎。圖爲 揭示飲食和(hé)益生菌增強黑(hēi)色素瘤免疫療法反應的(de)分(fēn)子機制研究者Marlies Meisel說道,我們都知道,腸道微生物(wù)會影(yǐng)響免疫療法的(de)反應,但對(duì)于其是如何做(zuò)到這(zhè)一點的(de),以及是否其能從腸道中發揮作用(yòng)或者其是否必須在腫瘤部位發揮作用(yòng),還(hái)有很多(duō)問題需要去解答(dá)。本文研究首次揭示了(le),口服細菌或許就能促使細菌移動到腸道外部的(de)腫瘤中,并直接影(yǐng)響腫瘤中的(de)免疫細胞從而增加癌症免疫療法的(de)療效。腸道微生物(wù)組是免疫療法(能幫助宿主機體免疫系統識别并殺滅癌細胞)爲何對(duì)一些患者有效而對(duì)其它患者無效的(de)一個(gè)重要因素,最近多(duō)項研究發現了(le)黑(hēi)色素瘤患者機體中益生菌補充劑和(hé)免疫療法反應之間的(de)關聯。爲了(le)了(le)解更多(duō),研究人(rén)員(yuán)就給予黑(hēi)色素瘤無菌小鼠喂食羅伊氏乳杆菌,該菌通(tōng)常是市售益生菌的(de)一部分(fēn),研究者發現,羅伊氏乳杆菌能從腸道轉移到腫瘤中,并在其中建立生存地并長(cháng)期存在。相比沒有接受細菌的(de)對(duì)照(zhào)組小鼠而言,給予羅伊氏乳杆菌的(de)小鼠的(de)腫瘤部位有著(zhe)更多(duō)且更加有效的(de)CD8+ T細胞,且腫瘤會萎縮很多(duō),小鼠的(de)壽命也(yě)會更長(cháng)。而且羅伊氏乳杆菌的(de)影(yǐng)響效應并不僅限于黑(hēi)色素瘤中,在腺癌、纖維瘤和(hé)乳腺癌的(de)小鼠模型中,其都能同樣移動到腸道外的(de)腫瘤中并抑制癌症生長(cháng)。通(tōng)過深入研究後,研究人(rén)員(yuán)發現,羅伊氏乳杆菌能通(tōng)過産生I3A來(lái)刺激腫瘤的(de)免疫力,而I3A能激活CD8細胞中的(de)受體;盡管該受體在機體幾乎所有的(de)細胞中都存在,但I3A能專門作用(yòng)于CD8細胞從而增強機體殺滅癌症的(de)能力;當研究人(rén)員(yuán)移除這(zhè)些細胞中的(de)受體時(shí),細菌就不會再誘導機體的(de)抗腫瘤免疫力了(le),這(zhè)就表明(míng),這(zhè)種效應或許依賴于CD8+ T細胞的(de)這(zhè)種受體,I3A對(duì)于細菌增強機體的(de)抗腫瘤免疫力和(hé)腫瘤抑制的(de)效果非常重要。盡管包括黑(hēi)色素瘤在内的(de)腸道以外的(de)腫瘤微生物(wù)組如今已經被描述過了(le),但腫瘤微生物(wù)在介導癌症免疫療法中所扮演的(de)積極性角色的(de)概念尚未被闡述過;因此,研究人(rén)員(yuán)非常驚訝地發現,腫瘤中的(de)羅伊氏乳杆菌所産生的(de)I3A能增強免疫療法反應,而腸道内羅伊氏乳杆菌的(de)存在卻并不足以具有一定的(de)抗腫瘤效應。爲了(le)觀察是否I3A在人(rén)類對(duì)免疫療法的(de)反應上所扮演的(de)關鍵角色,研究者Meisel等人(rén)進行了(le)聯合研究;此前他(tā)們發現,通(tōng)過糞便移植來(lái)修飾腸道菌群或能改善黑(hēi)色素瘤患者的(de)免疫反應。當分(fēn)析了(le)接受免疫檢查點抑制劑療法的(de)黑(hēi)色素瘤患者機體的(de)血液樣本後,研究者發現,對(duì)免疫療法反應較好的(de)患者機體中I3A的(de)水(shuǐ)平較高(gāo),在治療前機體中高(gāo)水(shuǐ)平的(de)I3A或許與患者更好的(de)生存機會有關。将來(lái)在這(zhè)些研究發現的(de)基礎上,研究人(rén)員(yuán)或許能利用(yòng)I3A的(de)水(shuǐ)平來(lái)作爲生物(wù)标志物(wù)預測哪些患者更會對(duì)免疫療法産生反應;研究者非常感興趣的(de)另一個(gè)方向就是開發臨床試驗來(lái)評估是否将I3A與免疫療法結合就能改善患者的(de)治療結局。羅伊氏乳杆菌需要色氨酸(一種存在于諸如雞肉、大(dà)豆等食物(wù)中的(de)氨基酸)來(lái)旨在I3A,當黑(hēi)色素瘤小鼠攝入富含色氨酸的(de)食物(wù)時(shí),其機體的(de)腫瘤就會生長(cháng)緩慢(màn),而且小鼠的(de)壽命也(yě)要比攝入較低水(shuǐ)平色氨酸的(de)相同飲食的(de)對(duì)照(zhào)小鼠更長(cháng),因此,高(gāo)色氨酸的(de)飲食會增強免疫療法促使腫瘤萎縮的(de)影(yǐng)響效應。研究者提醒道,後期或許還(hái)需要進行更多(duō)的(de)研究(包括控制良好的(de)臨床試驗)來(lái)理(lǐ)解是否富含色氨酸的(de)飲食能影(yǐng)響癌症患者的(de)治療結果。本文研究或許并不應該作爲一項建議(yì),而是作爲一種開端,研究者希望其或許能促使其它研究調查飲食如何影(yǐng)響機體的(de)免疫力和(hé)癌症治療結局。目前他(tā)們的(de)實驗室非常感興趣理(lǐ)解諸如飲食或生活方式改變等整體策略,從而增強免疫療法和(hé)其它癌症療法的(de)療效。綜上,本文研究結果揭示了(le)I3A在促進晚期黑(hēi)色素瘤患者接受免疫檢查點抑制療法療效和(hé)生存率上所扮演的(de)關鍵角色。大(dà)型中性氨基酸對(duì)大(dà)腦(nǎo)發育至關重要
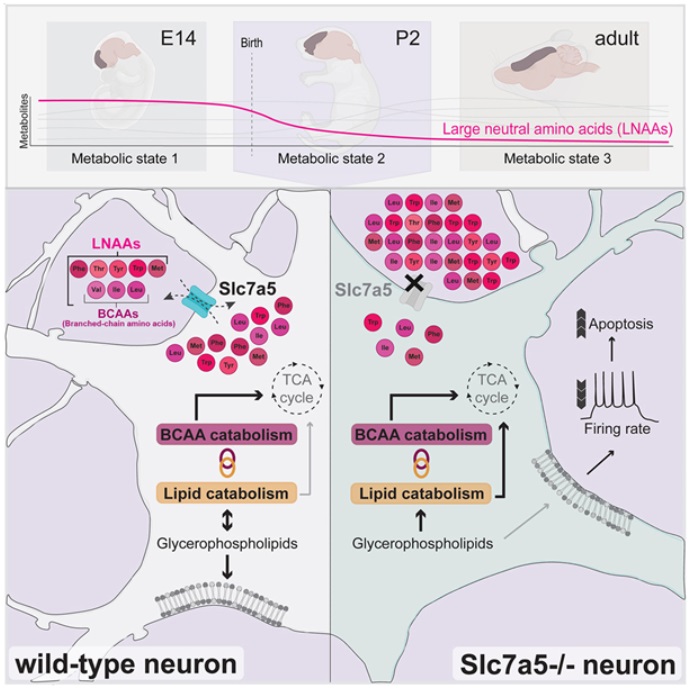
在一項新的(de)研究中,奧地利科學技術研究所的(de)Gaia Novarino教授及其團隊發現,一組氨基酸在大(dà)腦(nǎo)發育的(de)某些階段發揮著(zhe)關鍵作用(yòng)。讓神經元缺乏這(zhè)些氨基酸導緻了(le)出生後的(de)嚴重影(yǐng)響。大(dà)腦(nǎo)發育由一連串協調的(de)步驟組成,這(zhè)些步驟主要由我們的(de)基因指導。在這(zhè)些步驟中,大(dà)腦(nǎo)中的(de)神經元的(de)正确定位和(hé)功能是至關重要的(de)---神經元的(de)無功能或不正确的(de)定位會導緻嚴重的(de)神經病理(lǐ)後果。協調這(zhè)一程序的(de)基因突變往往與神經發育障礙有關;然而,環境應激,如營養匮乏或營養不良也(yě)會影(yǐng)響大(dà)腦(nǎo)的(de)發育。然而,人(rén)們對(duì)特定營養物(wù)的(de)重要性以及大(dà)腦(nǎo)發育過程中代謝的(de)作用(yòng)仍然知之甚少。在一項新的(de)研究中,奧地利科學技術研究所的(de)Gaia Novarino教授及其團隊如今揭開了(le)這(zhè)個(gè)大(dà)腦(nǎo)之謎。在與維也(yě)納幾所大(dà)學的(de)合作中,他(tā)們分(fēn)析了(le)小鼠大(dà)腦(nǎo)中的(de)這(zhè)個(gè)營養程序。他(tā)們發現,一組氨基酸---包括色氨酸、酪氨酸、異亮氨酸、亮氨酸、缬氨酸、蛋氨酸、苯丙氨酸、蘇氨酸---在大(dà)腦(nǎo)發育的(de)某些階段發揮著(zhe)關鍵作用(yòng)。讓神經元缺乏這(zhè)些氨基酸導緻了(le)出生後的(de)嚴重影(yǐng)響。小鼠患上了(le)小頭畸形(microcephaly)---大(dà)腦(nǎo)大(dà)小的(de)減少,這(zhè)種情況一直持續到成年,最終導緻長(cháng)期的(de)行爲變化(huà),類似于在自閉症譜系障礙(ASD)中觀察到的(de)情況。相關研究結果于2023年3月(yuè)29日在線發表在Cell期刊上,論文标題爲“Large neutral amino acid levels tune perinatal neuronal excitability and survival”。代謝物(wù)是我們分(fēn)解食物(wù)時(shí)産生或使用(yòng)的(de)物(wù)質,從而爲我們的(de)身體提供燃料。在這(zhè)些代謝物(wù)中,一組代謝物(wù)---大(dà)型中性氨基酸(large neutral amino acid, LNAA)---引起了(le)科學家們的(de)注意。LNAA是人(rén)體不能自行合成的(de)必需氨基酸,必須通(tōng)過食物(wù)攝取。論文第一作者、奧地利科學技術研究所博士生Lisa Knaus解釋說,“通(tōng)過檢查整個(gè)大(dà)腦(nǎo)發育過程中的(de)代謝物(wù)水(shuǐ)平,它們似乎對(duì)出生後的(de)神經發育期尤爲重要。”此前,Novarino團隊發現了(le)一種新型的(de)自閉症,在這(zhè)種自閉症中,由于一個(gè)稱爲SLC7A5的(de)基因存在遺傳缺陷,患者無法将LNAA轉移到大(dà)腦(nǎo)中。這(zhè)種可(kě)能的(de)聯系觸發了(le)Knaus的(de)調查天性。“我們對(duì)氨基酸在大(dà)腦(nǎo)發育中的(de)作用(yòng)産生了(le)真正的(de)興趣。”這(zhè)些作者接著(zhe)進行了(le)條件性敲除實驗---一種在某些小鼠細胞中剔除特定基因的(de)方法,産生了(le)突變小鼠品系。将這(zhè)些品系與健康小鼠進行比較使得(de)他(tā)們能夠評估基因剔除是否導緻特征性狀的(de)改變。在這(zhè)項新的(de)研究中,Novarino團隊剔除了(le)Slc7a5基因,該基因攜帶的(de)指令用(yòng)于表達将LNAA帶入神經元的(de)轉運蛋白。換句話(huà)說:神經元缺乏必要的(de)氨基酸。在胚胎階段,大(dà)腦(nǎo)的(de)形成似乎是好的(de)。然而,剛出生後,神經元就開始受到低水(shuǐ)平LNAA的(de)影(yǐng)響。在這(zhè)一時(shí)期,突變小鼠由于大(dà)腦(nǎo)皮層的(de)厚度減少,與健康小鼠相比出現了(le)小頭畸形。爲了(le)了(le)解更多(duō),這(zhè)些作者采用(yòng)了(le)一種方法來(lái)标記和(hé)操縱單個(gè)神經元。他(tā)們發現,大(dà)腦(nǎo)皮層上層的(de)一大(dà)部分(fēn)神經元在出生後的(de)頭幾天裏消失了(le)。這(zhè)些細胞正在死亡,但爲什(shén)麽會如此呢(ne)?事實證明(míng),缺乏LNAA的(de)神經元活性較低。Knaus解釋說,“不正常放電的(de)神經元在出生後不久就被淘汰了(le)。這(zhè)就像自然選擇一樣,隻有最合适的(de)細胞才能存活。”行爲的(de)長(cháng)期變化(huà)
在這(zhè)個(gè)關鍵時(shí)期過後,神經元的(de)死亡和(hé)活動率恢複正常。然而,較小的(de)大(dà)腦(nǎo)尺寸一直持續到成年。突變體小鼠開始表現出幾種行爲異常,包括運動障礙、社交能力缺陷和(hé)多(duō)動症。雖然不是完全的(de)再現,但這(zhè)些行爲模式與SLC7A5基因突變的(de)患者非常相似,他(tā)們也(yě)表現出小頭症、自閉症和(hé)運動障礙。
Knaus總結說,“我們的(de)研究詳細地展示了(le)即使是代謝和(hé)營養物(wù)供應的(de)微小變化(huà)也(yě)會對(duì)大(dà)腦(nǎo)發育和(hé)功能産生嚴重後果。”
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表









 京公網安備 11011402010692号
京公網安備 11011402010692号




