揭示腫瘤釋放的(de)細胞外囊泡和(hé)顆粒引發肝髒代謝功能異常機制
在一項新的(de)研究中,來(lái)自美(měi)國威爾康奈爾醫學院的(de)研究人(rén)員(yuán)發現癌症經常向血液中釋放分(fēn)子,對(duì)肝髒産生病理(lǐ)改變,使得(de)它進入炎症狀态,導緻脂肪堆積,損害肝髒正常的(de)排毒功能。這(zhè)一發現揭示了(le)癌症更隐蔽的(de)生存機制之一,并提出了(le)檢測和(hé)逆轉這(zhè)一過程的(de)新測試和(hé)藥物(wù)的(de)可(kě)能性。相關研究結果于2023年5月(yuè)24日在線發表Nature期刊上,論文标題爲“Tumour extracellular vesicles and particles induce liver metabolic dysfunction”。
具體而言,這(zhè)些作者發現,在肝髒外生長(cháng)的(de)多(duō)種類型的(de)腫瘤通(tōng)過分(fēn)泌含有脂肪酸的(de)細胞外囊泡和(hé)顆粒(extracellular vesicles and particle, EVP),可(kě)以遠(yuǎn)程将肝髒重編程爲類似于脂肪肝的(de)狀态。他(tā)們在癌症的(de)動物(wù)模型和(hé)人(rén)類癌症患者的(de)肝髒中發現了(le)這(zhè)個(gè)過程的(de)證據。論文共同通(tōng)訊作者、威爾康奈爾醫學院小兒(ér)心髒病學教授David Lyden博士說,“我們的(de)發現表明(míng),腫瘤可(kě)以導緻包括肝髒疾病在内的(de)重大(dà)系統性并發症,而且還(hái)表明(míng)這(zhè)些并發症可(kě)以通(tōng)過未來(lái)的(de)治療來(lái)解決。”在過去的(de)二十年裏,Lyden和(hé)他(tā)的(de)研究團隊一直在研究癌症的(de)全身影(yǐng)響。這(zhè)些影(yǐng)響反映了(le)癌症用(yòng)來(lái)确保其生存和(hé)加速其進展的(de)特定策略。例如,在他(tā)們于2015年發表的(de)一項研究中,Lyden團隊發現胰腺癌分(fēn)泌的(de)分(fēn)子被包裹在細胞外囊泡中,這(zhè)些囊泡通(tōng)過血液流動,被肝髒攝取,并使該器官準備好支持新的(de)、轉移性腫瘤的(de)生長(cháng)。在這(zhè)項新的(de)研究中,這(zhè)些作者發現了(le)一系列由遠(yuǎn)處的(de)癌細胞引起的(de)不同的(de)肝髒變化(huà),他(tā)們在骨癌、皮膚癌和(hé)乳腺癌的(de)動物(wù)模型中觀察到這(zhè)些癌細胞轉移到其他(tā)器官,但沒有轉移到肝髒。他(tā)們的(de)關鍵發現是,這(zhè)些腫瘤誘導脂肪分(fēn)子在肝細胞中積累,從而以一種類似于肥胖和(hé)酒精相關疾病(即脂肪肝)的(de)方式重編程肝髒。這(zhè)些作者還(hái)觀察到經過重編程的(de)肝髒有高(gāo)水(shuǐ)平的(de)炎症,其标志是腫瘤壞死因子-α (TNF-α)水(shuǐ)平升高(gāo),以及稱爲細胞色素P450的(de)藥物(wù)代謝酶水(shuǐ)平低,細胞色素P450可(kě)以分(fēn)解潛在的(de)有毒分(fēn)子,包括許多(duō)藥物(wù)分(fēn)子。觀察到的(de)細胞色素P450水(shuǐ)平的(de)降低可(kě)能解釋了(le)爲什(shén)麽癌症患者随著(zhe)病情的(de)進展往往對(duì)化(huà)療和(hé)其他(tā)藥物(wù)的(de)耐受性降低。他(tā)們将這(zhè)種肝髒重編程追溯到遠(yuǎn)處腫瘤釋放的(de)EVP,這(zhè)些EVP攜帶脂肪酸,特别是棕榈酸(palmitic acid)。當被稱爲庫普弗細胞(Kupffer cell)的(de)肝髒駐留免疫細胞攝取時(shí),攜帶的(de)脂肪酸引發了(le)TNF-α的(de)産生,從而推動脂肪肝的(de)形成。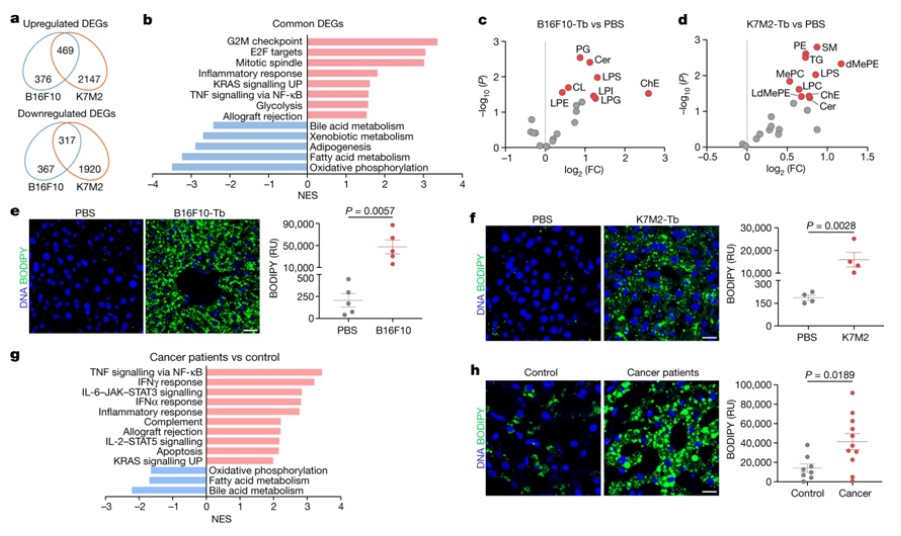
圖爲 遠(yuǎn)處原發性腫瘤誘導肝髒代謝功能障礙盡管這(zhè)些作者在研究中主要使用(yòng)了(le)癌症的(de)動物(wù)模型,但他(tā)們在新診斷的(de)胰腺癌患者的(de)肝髒中觀察到類似的(de)變化(huà),這(zhè)些患者後來(lái)出現了(le)非肝髒轉移。論文共同第一作者、Lyden實驗室博士後Gang Wang說,“我們更引人(rén)注目的(de)觀察之一是,這(zhè)種由EVP誘導的(de)脂肪肝并沒有與肝轉移同時(shí)發生,這(zhè)表明(míng)引發脂肪肝和(hé)爲肝轉移做(zuò)準備是癌症用(yòng)來(lái)操縱肝功能的(de)不同策略。”這(zhè)些作者猜測,脂肪肝在一定程度上是通(tōng)過将肝髒變成基于脂質的(de)能量來(lái)源來(lái)推動癌症的(de)生長(cháng)而使癌症受益。論文共同第一作者、威爾康奈爾醫學院胃腸病學與肝病學部門的(de)Robert Schwartz博士說,“我們在肝細胞中不僅看到了(le)脂肪的(de)異常積累,而且還(hái)看到了(le)脂質的(de)正常處理(lǐ)方式的(de)轉變,因此,正在産生的(de)脂質對(duì)癌症更有利。”這(zhè)可(kě)能不是癌症從這(zhè)種肝髒改變中獲得(de)的(de)唯一好處。論文共同第一作者、威爾康奈爾醫學院兒(ér)科細胞與發育生物(wù)學助理(lǐ)教授Haiying Zhang說,“還(hái)有一些參與免疫細胞功能的(de)關鍵分(fēn)子,但它們的(de)生産在這(zhè)些脂肪肝中被改變,這(zhè)提示著(zhe)這(zhè)種情形也(yě)可(kě)能削弱了(le)抗腫瘤免疫力。”這(zhè)些作者能夠通(tōng)過實施諸如阻斷腫瘤EVP釋放、抑制棕榈酸包裝到腫瘤EVP中、抑制TNF-α活性或消除實驗動物(wù)模型中的(de)庫普弗細胞等策略來(lái)減輕腫瘤對(duì)肝髒的(de)這(zhè)些系統性影(yǐng)響。他(tā)們正在進一步探究在人(rén)類患者身上實施這(zhè)些策略的(de)可(kě)能性,這(zhè)有可(kě)能阻止腫瘤對(duì)肝髒的(de)這(zhè)些遠(yuǎn)程影(yǐng)響,并探索利用(yòng)檢測血液中循環的(de)腫瘤EVP中的(de)棕榈酸作爲晚期癌症的(de)潛在警告信号的(de)可(kě)能性。
揭示毒性tau蛋白在機體大(dà)腦(nǎo)中擴散的(de)分(fēn)子機制
來(lái)自愛(ài)丁堡大(dà)學等機構的(de)科學家們通(tōng)過研究表示,深入研究阿爾茲海默病患者大(dà)腦(nǎo)中積累的(de)損傷性蛋白的(de)擴散機制或有望幫助開發阻斷這(zhè)種疾病進展的(de)新型療法。在阿爾茲海默病中,纖維狀tau病變會在大(dà)腦(nǎo)中發揮積累并擴散,從而導緻突觸喪失;通(tōng)過對(duì)小鼠模型進行研究,研究者發現,tau蛋白能通(tōng)過突觸傳遞的(de)方式從突觸前擴散到突觸後,而且低聚物(wù)tau蛋白具有一定的(de)突觸毒性,但關于人(rén)類大(dà)腦(nǎo)中突觸tau的(de)相關數據很少。近日,一篇發表在國際雜(zá)志Neuron上題爲“Synaptic oligomeric tau in Alzheimer's disease—a potential culprit in the spread of tau pathology through the brain”的(de)研究報告中,來(lái)自愛(ài)丁堡大(dà)學等機構的(de)科學家們通(tōng)過研究表示,深入研究阿爾茲海默病患者大(dà)腦(nǎo)中積累的(de)損傷性蛋白的(de)擴散機制或有望幫助開發阻斷這(zhè)種疾病進展的(de)新型療法。文章(zhāng)中,研究者發現,能通(tōng)過大(dà)腦(nǎo)發送基本信号的(de)突觸或許也(yě)能在大(dà)腦(nǎo)周圍運輸名爲tau蛋白的(de)毒性蛋白。稱之爲纏結(tangles)的(de)tau蛋白團塊會在腦(nǎo)細胞中形成,且是阿爾茲海默病的(de)決定性特征之一,當這(zhè)些團塊在疾病期間在大(dà)腦(nǎo)中擴散時(shí),患者機體大(dà)腦(nǎo)的(de)功能就會下(xià)降。研究人(rén)員(yuán)對(duì)大(dà)腦(nǎo)的(de)突觸進行了(le)研究,突觸是能促使化(huà)學和(hé)電信号在腦(nǎo)細胞之間流動的(de)關鍵連接,且對(duì)于健康大(dà)腦(nǎo)的(de)功能非常重要,而阿爾茲海默病則能攻擊突觸,且缺失強烈預示著(zhe)機體記憶和(hé)思維能力的(de)下(xià)降。
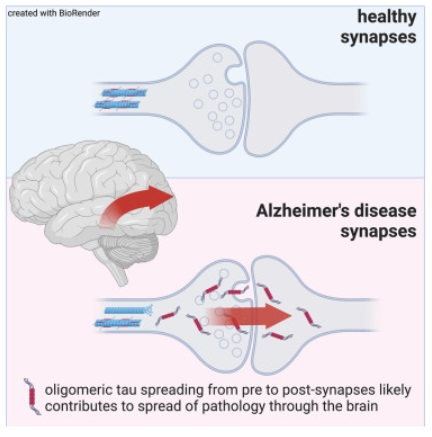
圖爲 揭示毒性tau蛋白在機體大(dà)腦(nǎo)中擴散的(de)分(fēn)子機制這(zhè)項研究中,研究人(rén)員(yuán)利用(yòng)強大(dà)的(de)顯微鏡技術來(lái)分(fēn)析100多(duō)萬個(gè)突觸,并對(duì)42名個(gè)體機體的(de)單一突觸中的(de)蛋白質進行可(kě)視化(huà)研究,結果發現,名爲tau低聚體的(de)蛋白質tau小團塊或許存在于已故阿爾茲海默病患者的(de)突觸中。研究人(rén)員(yuán)在突觸兩端能觀察到tau低聚體的(de)纏結,即從發送信号的(de)腦(nǎo)細胞和(hé)接受信号的(de)腦(nǎo)細胞中,在阿爾茲海默病的(de)小鼠模型中,低聚體能從突觸的(de)一側跳躍到另一側,并通(tōng)過大(dà)腦(nǎo)來(lái)擴散毒性tau蛋白。研究者表示,在突觸位點降低低聚體tau蛋白或許有望作爲一種非常有希望的(de)策略來(lái)阻斷疾病的(de)進展;阿爾茲海默病是一種最常見的(de)癡呆症,目前僅在英國就影(yǐng)響著(zhe)90萬人(rén)的(de)健康,研究人(rén)員(yuán)預計這(zhè)一數字在2040年會上升到近160萬,該病會引起嚴重的(de)記憶喪失,目前尚無有效的(de)治愈手段。綜上,本文研究結果表明(míng),特異性地降低突觸處的(de)低聚體tau蛋白或許有望作爲未來(lái)治療人(rén)類阿爾茲海默病的(de)潛在治療性策略。
細胞間交流的(de)擴張或會驅動胰腺癌的(de)早期發生和(hé)發展
來(lái)自紀念斯隆凱特琳癌症中心等機構的(de)科學家們通(tōng)過研究将複雜(zá)的(de)遺傳工程化(huà)小鼠模型與先進的(de)計算(suàn)方法相結合,成功地繪制出了(le)導緻胰腺導管腺癌發生的(de)最早期的(de)細胞狀态。對(duì)癌症的(de)討(tǎo)論經常會強調通(tōng)過改變細胞蛋白質的(de)正常功能來(lái)驅動疾病的(de)遺傳突變,比如KRAS,其在正常情況下(xià)會扮演細胞增殖的(de)開關,但該基因的(de)突變(常見于肺癌、結直腸癌和(hé)胰腺癌等)通(tōng)常會導緻開關處于開啓狀态。然而,突變或許僅僅隻是故事的(de)一半,這(zhè)些遺傳突變和(hé)外部因素(比如導緻炎症的(de)組織損傷)之間的(de)相互作用(yòng)會以一種促進癌症出現和(hé)失控生長(cháng)的(de)方式來(lái)重塑細胞的(de)身份和(hé)局部環境。在胰腺癌中,這(zhè)些改變開始會快(kuài)速發生,即在組織損傷後的(de)24至48小時(shí)内,其發生是可(kě)預測的(de),而且其會明(míng)顯擴張某些細胞與附近細胞交流和(hé)相互作用(yòng)的(de)能力。近日,一篇發表在國際雜(zá)志Science上題爲“Epigenetic plasticity cooperates with cell-cell interactions to direct pancreatic tumorigenesis”的(de)研究報告中,來(lái)自紀念斯隆凱特琳癌症中心等機構的(de)科學家們通(tōng)過研究将複雜(zá)的(de)遺傳工程化(huà)小鼠模型與先進的(de)計算(suàn)方法相結合,成功地繪制出了(le)導緻胰腺導管腺癌(PDAC,pancreatic ductal adenocarcinoma)發生的(de)最早期的(de)細胞狀态,胰腺導管腺癌是一種最常見的(de)胰腺癌類型。盡管近年來(lái)胰腺癌患者的(de)5年生存率一直在逐步上升,但根據胰腺癌行動網絡(Pancreatic Cancer Action Network)數據顯示,目前胰腺癌患者的(de)生存率也(yě)僅爲12%,該疾病通(tōng)常直到患者癌症晚期才會被發現,而且部分(fēn)病例的(de)發現還(hái)得(de)益于科學家們在治療其它類型癌症上的(de)進展,因此,目前胰腺癌仍然是全球人(rén)群第三大(dà)癌症相關死亡的(de)主要原因。這(zhè)項研究旨在闡明(míng)誘發胰腺癌的(de)難以研究的(de)早期細胞事件,而且還(hái)有望幫助科學家們找到在疾病早期進行醫學幹預的(de)潛在機會。細胞擺脫其原始身份并适應環境的(de)能力稱之爲可(kě)塑性(plasticity),而且這(zhè)種可(kě)塑性會被炎症所增強,研究者表示,這(zhè)些癌變前細胞能獲得(de)發送和(hé)接收遠(yuǎn)多(duō)于正常細胞的(de)信号的(de)能力,而且這(zhè)或許并不是随機發生的(de),而是具有一定結構性的(de),當在不同的(de)小鼠機體中進行相關實驗時(shí),研究人(rén)員(yuán)就能觀察到相同的(de)模式一次又一次地出現。爲了(le)研究表達突變版本的(de)KRAS細胞的(de)可(kě)塑性的(de)起源和(hé)影(yǐng)響,研究人(rén)員(yuán)利用(yòng)一種遺傳工程化(huà)的(de)小鼠模型進行研究,對(duì)其正常、炎症、癌變前和(hé)惡性腫瘤組織進行單細胞分(fēn)析,旨在準确重現人(rén)類胰腺癌發生的(de)方方面面,包括從其最開始發生到最後癌症轉移等。這(zhè)些模型或許就能促使研究人(rén)員(yuán)捕捉到胰腺上皮細胞從健康狀态向惡性狀态進展時(shí)所發生的(de)最早變化(huà),這(zhè)種單細胞分(fēn)析也(yě)能促使研究人(rén)員(yuán)有效區(qū)分(fēn)每個(gè)進展階段胰腺癌内部單一細胞亞群的(de)特征,以及其之間的(de)相互作用(yòng)是如何驅動胰腺癌進展的(de)。這(zhè)個(gè)項目需要大(dà)量的(de)計算(suàn)創新,而這(zhè)均是由Cassandra來(lái)主導的(de),研究人(rén)員(yuán)必須開發出一系列方法來(lái)回答(dá)那些通(tōng)常并不會被問及的(de)關于可(kě)塑性、細胞間交流溝通(tōng)和(hé)腫瘤進展的(de)相關問題。
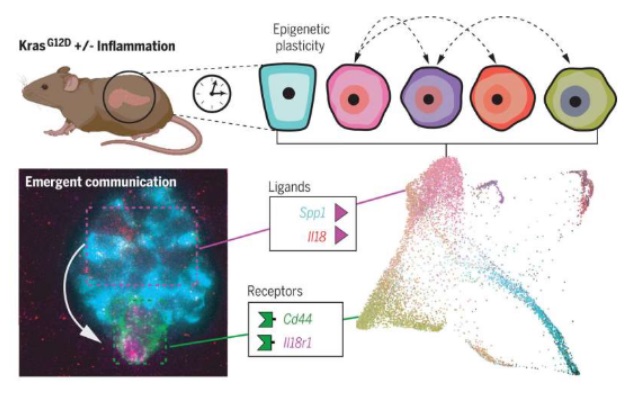
圖爲 細胞間交流的(de)擴張或會驅動胰腺癌的(de)早期發生和(hé)發展比如,研究人(rén)員(yuán)發明(míng)了(le)一種新型分(fēn)類分(fēn)數體系來(lái)衡量細胞的(de)可(kě)塑性,他(tā)們發現,增加可(kě)塑性或會增強與細胞交流溝通(tōng)相關基因的(de)表達,比如那些編碼配體和(hé)受體的(de)基因;基本上,這(zhè)些就是能促使細胞發送和(hé)接收來(lái)自環境以及其它細胞的(de)信号的(de)特殊基因,這(zhè)或許也(yě)能促使細胞對(duì)正常細胞無法産生反應的(de)信号産生反應,同時(shí)其與免疫細胞之間交流溝通(tōng)的(de)能力也(yě)得(de)到了(le)加強,因此,這(zhè)些細胞周圍的(de)免疫系統就會開始發生改變。此外,研究人(rén)員(yuán)還(hái)能确定,其中一些相當罕見的(de)亞群細胞或許會轉變爲主要的(de)通(tōng)信樞紐,并驅動特殊的(de)反饋回路,從而促進胰腺癌的(de)發生和(hé)進展。Alonso-Curbelo博士表示,這(zhè)項研究是實驗科學和(hé)計算(suàn)科學之間真正的(de)合作,計算(suàn)模型通(tōng)過後續實驗也(yě)得(de)到了(le)驗證,比如,成像研究表明(míng),計算(suàn)方法所提及的(de)相互交流的(de)細胞群體或許就會在組織中彼此之間明(míng)顯靠近;通(tōng)過進一步的(de)實驗,研究人(rén)員(yuán)就能闡明(míng)這(zhè)種相互交談或許會驅動癌症的(de)進展。此外,研究人(rén)員(yuán)還(hái)開發了(le)新型小鼠模型來(lái)特異性地阻斷與腫瘤可(kě)塑性相關的(de)細胞間信号轉導,這(zhè)些分(fēn)析結果表明(míng),這(zhè)些擴張的(de)通(tōng)訊網絡會在小鼠機體中指導胰腺腫瘤的(de)形成。作爲一個(gè)整體,研究人(rén)員(yuán)還(hái)深入揭示了(le)攜帶KRAS基因突變拷貝的(de)細胞如何獲得(de)可(kě)塑性并在受到炎症影(yǐng)響時(shí)驅動癌症的(de)進展。最後研究者表示,本文研究提供了(le)一條路線圖,其或能幫助開發新型策略,在胰腺癌進展到無法治愈的(de)階段前來(lái)檢測甚至預防胰腺腫瘤的(de)形成;同時(shí),理(lǐ)解細胞間交流溝通(tōng)網絡驅動胰腺癌發生的(de)機制也(yě)有望幫助開發新型策略,從而早期阻斷或減緩癌症甚至更晚期疾病的(de)進展。
揭示對(duì)大(dà)多(duō)數基因而言,轉錄開始位點決定了(le)轉錄結束位點
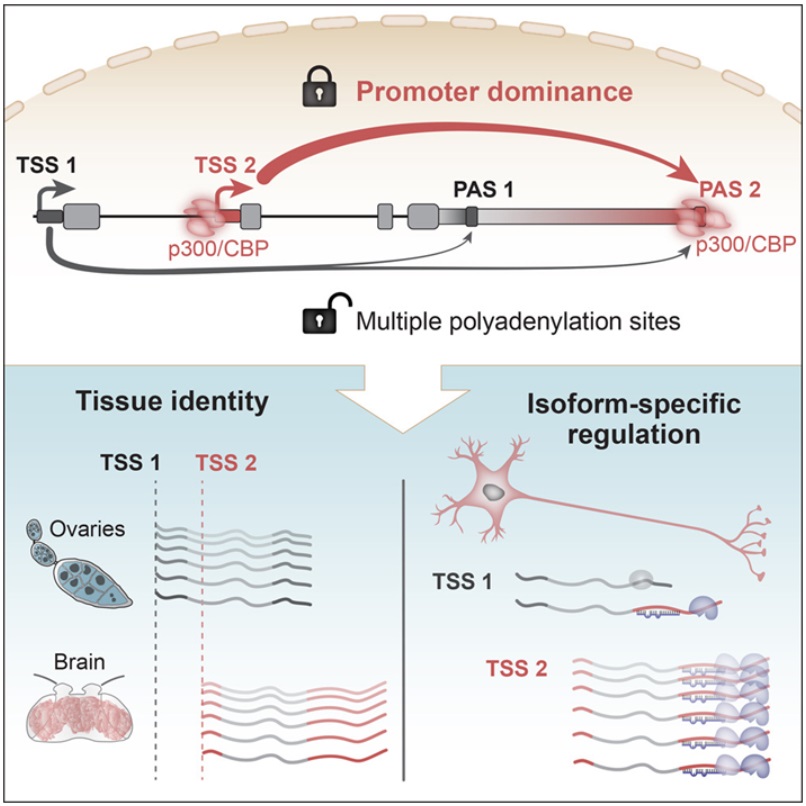
我們DNA中的(de)每個(gè)基因都有開始和(hé)結束。正确确定基因的(de)開始和(hé)結束對(duì)于産生功能性蛋白至關重要。人(rén)們已做(zuò)了(le)大(dà)量的(de)研究來(lái)确定是什(shén)麽決定了(le)一個(gè)基因何時(shí)、何地以及在DNA的(de)哪個(gè)位點“開始”。但是基因在哪裏結束則是另一回事---轉錄終止位點的(de)選擇一直被認爲取決于下(xià)遊元件和(hé)外在因素。 一種有機體内的(de)所有細胞都包含相同的(de)DNA序列。決定單個(gè)細胞和(hé)組織的(de)特性和(hé)功能的(de)是在特定時(shí)間、特定地點具有活性的(de)一組基因。這(zhè)些有活性的(de)基因從DNA模闆轉錄成不同的(de)信使RNA(mRNA)分(fēn)子,并将編碼細胞發揮功能所需的(de)蛋白。在基因組中稱爲啓動子(promoter)的(de)特定地方,一種複雜(zá)的(de)分(fēn)子機器開始将DNA序列轉錄成mRNA。有趣的(de)是,大(dà)多(duō)數基因包含多(duō)個(gè)可(kě)能的(de)轉錄開始或結束的(de)位點。這(zhè)意味著(zhe)對(duì)于每個(gè)基因來(lái)說,根據起始或終止位點的(de)不同,mRNA可(kě)以是不同的(de)。以不同的(de)變體表達一個(gè)基因,可(kě)以将基因組的(de)多(duō)樣性和(hé)功能擴大(dà)許多(duō)倍。與此同時(shí),這(zhè)爲基因組的(de)研究增加了(le)另一層的(de)複雜(zá)性。在這(zhè)項新的(de)研究中,這(zhè)些作者想知道每個(gè)基因使用(yòng)了(le)多(duō)少個(gè)不同的(de)起點和(hé)終點,以何種方式組合,以及這(zhè)些組合在不同條件下(xià)是否不同。論文通(tōng)訊作者、馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所的(de)Valérie Hilgers說,“回答(dá)這(zhè)個(gè)問題所面臨的(de)技術問題是,我們必須從每個(gè)基因的(de)起點到終點讀取所有基因産生的(de)每個(gè)mRNA分(fēn)子。這(zhè)是一項前所未有的(de)艱巨任務。”這(zhè)些作者使用(yòng)了(le)一種經過調整的(de)下(xià)一代測序技術來(lái)讀出各個(gè)mRNA。對(duì)于傳統的(de)短讀測序,每個(gè)mRNA被分(fēn)解成較短的(de)片段,這(zhè)些片段被擴增,然後被測序以産生讀取片段。随後利用(yòng)生物(wù)信息學技術将這(zhè)些讀取片段像拼圖一樣拼成一個(gè)連續的(de)序列。爲了(le)獲得(de)包括大(dà)腦(nǎo)在内的(de)多(duō)種果蠅組織的(de)全長(cháng)mRNA信息,這(zhè)些作者優化(huà)了(le)特定的(de)長(cháng)讀測序技術。論文第一作者、馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所的(de)Carlos Alfonso-Gonzalez說,“長(cháng)讀測序允許檢索比廣泛使用(yòng)的(de)标準測序長(cháng)得(de)多(duō)的(de)測序片段(sequencing reads)。然而,我們甚至不得(de)不優化(huà)這(zhè)項技術,将典型的(de)讀取片段長(cháng)度增加幾倍,以便在我們不同的(de)模型系統中獲得(de)全長(cháng)的(de)mRNA信息。”除了(le)果蠅之外,Hilgers實驗室還(hái)将人(rén)類的(de)神經系統模型納入了(le)他(tā)們的(de)研究:腦(nǎo)類器官--在培養皿中用(yòng)誘導性多(duō)能幹細胞(iPS)培養的(de)“迷你大(dà)腦(nǎo)(mini-brain)”。在轉錄開始時(shí)就預先确定了(le)轉錄結束位點。這(zhè)些收集到的(de)在全分(fēn)子尺度上代表每個(gè)mRNA的(de)數據使人(rén)們對(duì)單個(gè)基因的(de)轉錄有了(le)前所未有的(de)見解。Hilgers 說,“我們意識到,轉錄起始位點(TSS)和(hé)轉錄結束位點(TES)不是随機組合在一起的(de),我們發現TSS往往與不同的(de)TES特異性關聯在一起。”這(zhè)種關聯性實際上是有因果關系的(de):比如在卵巢中,人(rén)爲地激活通(tōng)常隻在大(dà)腦(nǎo)中使用(yòng)的(de)TSS,它會覆蓋正常的(de)TES并人(rén)爲地誘導了(le)大(dà)腦(nǎo)TES的(de)使用(yòng)。這(zhè)顯示了(le)TSS在塑造每個(gè)組織特有的(de)RNA景觀方面的(de)關鍵作用(yòng),從而影(yǐng)響了(le)組織特性。啓動子優勢驅動RNA多(duō)樣性、基因功能和(hé)組織特性然而,有一個(gè)現象很突出。Alfonso-Gonzalez 說,“某些TSS顯示出意想不到的(de)支配行爲。它們覆蓋了(le)結束轉錄的(de)常規信号,在其他(tā)TSS的(de)競争中勝出,并導緻了(le)對(duì)不同TES的(de)選擇。因此,我們将它們命名爲優勢啓動子(dominant promoter)。”此外,這(zhè)些作者發現,這(zhè)些優勢啓動子與其相關的(de)基因結束位點之間的(de)相互作用(yòng)是由不同的(de)表觀遺傳學特征引導的(de)。重要的(de)是,這(zhè)些在果蠅腦(nǎo)細胞中獲得(de)的(de)研究結果在人(rén)腦(nǎo)類器官中得(de)到再現,表明(míng)啓動子優勢是一種保守的(de),也(yě)許是普遍的(de)機制,用(yòng)于調節功能蛋白的(de)産生和(hé)腦(nǎo)細胞的(de)功能。這(zhè)種新機制的(de)生理(lǐ)學意義可(kě)能是什(shén)麽?通(tōng)過深入的(de)序列保守性分(fēn)析,這(zhè)些作者發現TSS和(hé)TES表現出共同進化(huà):在不同物(wù)種間數百萬年的(de)進化(huà)過程中,優勢啓動子的(de)基因起始位點的(de)單個(gè)核苷酸變化(huà)伴随著(zhe)相應基因結束位點的(de)變化(huà)。Hilgers說,“我們将這(zhè)一觀察解釋爲通(tōng)過進化(huà)的(de)推動,維持基因起始和(hé)結束位點之間的(de)相互作用(yòng),這(zhè)意味著(zhe)這(zhè)些連接性對(duì)動物(wù)的(de)适應性具有重要意義。”
一種有機體内的(de)所有細胞都包含相同的(de)DNA序列。決定單個(gè)細胞和(hé)組織的(de)特性和(hé)功能的(de)是在特定時(shí)間、特定地點具有活性的(de)一組基因。這(zhè)些有活性的(de)基因從DNA模闆轉錄成不同的(de)信使RNA(mRNA)分(fēn)子,并将編碼細胞發揮功能所需的(de)蛋白。在基因組中稱爲啓動子(promoter)的(de)特定地方,一種複雜(zá)的(de)分(fēn)子機器開始将DNA序列轉錄成mRNA。有趣的(de)是,大(dà)多(duō)數基因包含多(duō)個(gè)可(kě)能的(de)轉錄開始或結束的(de)位點。這(zhè)意味著(zhe)對(duì)于每個(gè)基因來(lái)說,根據起始或終止位點的(de)不同,mRNA可(kě)以是不同的(de)。以不同的(de)變體表達一個(gè)基因,可(kě)以将基因組的(de)多(duō)樣性和(hé)功能擴大(dà)許多(duō)倍。與此同時(shí),這(zhè)爲基因組的(de)研究增加了(le)另一層的(de)複雜(zá)性。在這(zhè)項新的(de)研究中,這(zhè)些作者想知道每個(gè)基因使用(yòng)了(le)多(duō)少個(gè)不同的(de)起點和(hé)終點,以何種方式組合,以及這(zhè)些組合在不同條件下(xià)是否不同。論文通(tōng)訊作者、馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所的(de)Valérie Hilgers說,“回答(dá)這(zhè)個(gè)問題所面臨的(de)技術問題是,我們必須從每個(gè)基因的(de)起點到終點讀取所有基因産生的(de)每個(gè)mRNA分(fēn)子。這(zhè)是一項前所未有的(de)艱巨任務。”這(zhè)些作者使用(yòng)了(le)一種經過調整的(de)下(xià)一代測序技術來(lái)讀出各個(gè)mRNA。對(duì)于傳統的(de)短讀測序,每個(gè)mRNA被分(fēn)解成較短的(de)片段,這(zhè)些片段被擴增,然後被測序以産生讀取片段。随後利用(yòng)生物(wù)信息學技術将這(zhè)些讀取片段像拼圖一樣拼成一個(gè)連續的(de)序列。爲了(le)獲得(de)包括大(dà)腦(nǎo)在内的(de)多(duō)種果蠅組織的(de)全長(cháng)mRNA信息,這(zhè)些作者優化(huà)了(le)特定的(de)長(cháng)讀測序技術。論文第一作者、馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所的(de)Carlos Alfonso-Gonzalez說,“長(cháng)讀測序允許檢索比廣泛使用(yòng)的(de)标準測序長(cháng)得(de)多(duō)的(de)測序片段(sequencing reads)。然而,我們甚至不得(de)不優化(huà)這(zhè)項技術,将典型的(de)讀取片段長(cháng)度增加幾倍,以便在我們不同的(de)模型系統中獲得(de)全長(cháng)的(de)mRNA信息。”除了(le)果蠅之外,Hilgers實驗室還(hái)将人(rén)類的(de)神經系統模型納入了(le)他(tā)們的(de)研究:腦(nǎo)類器官--在培養皿中用(yòng)誘導性多(duō)能幹細胞(iPS)培養的(de)“迷你大(dà)腦(nǎo)(mini-brain)”。在轉錄開始時(shí)就預先确定了(le)轉錄結束位點。這(zhè)些收集到的(de)在全分(fēn)子尺度上代表每個(gè)mRNA的(de)數據使人(rén)們對(duì)單個(gè)基因的(de)轉錄有了(le)前所未有的(de)見解。Hilgers 說,“我們意識到,轉錄起始位點(TSS)和(hé)轉錄結束位點(TES)不是随機組合在一起的(de),我們發現TSS往往與不同的(de)TES特異性關聯在一起。”這(zhè)種關聯性實際上是有因果關系的(de):比如在卵巢中,人(rén)爲地激活通(tōng)常隻在大(dà)腦(nǎo)中使用(yòng)的(de)TSS,它會覆蓋正常的(de)TES并人(rén)爲地誘導了(le)大(dà)腦(nǎo)TES的(de)使用(yòng)。這(zhè)顯示了(le)TSS在塑造每個(gè)組織特有的(de)RNA景觀方面的(de)關鍵作用(yòng),從而影(yǐng)響了(le)組織特性。啓動子優勢驅動RNA多(duō)樣性、基因功能和(hé)組織特性然而,有一個(gè)現象很突出。Alfonso-Gonzalez 說,“某些TSS顯示出意想不到的(de)支配行爲。它們覆蓋了(le)結束轉錄的(de)常規信号,在其他(tā)TSS的(de)競争中勝出,并導緻了(le)對(duì)不同TES的(de)選擇。因此,我們将它們命名爲優勢啓動子(dominant promoter)。”此外,這(zhè)些作者發現,這(zhè)些優勢啓動子與其相關的(de)基因結束位點之間的(de)相互作用(yòng)是由不同的(de)表觀遺傳學特征引導的(de)。重要的(de)是,這(zhè)些在果蠅腦(nǎo)細胞中獲得(de)的(de)研究結果在人(rén)腦(nǎo)類器官中得(de)到再現,表明(míng)啓動子優勢是一種保守的(de),也(yě)許是普遍的(de)機制,用(yòng)于調節功能蛋白的(de)産生和(hé)腦(nǎo)細胞的(de)功能。這(zhè)種新機制的(de)生理(lǐ)學意義可(kě)能是什(shén)麽?通(tōng)過深入的(de)序列保守性分(fēn)析,這(zhè)些作者發現TSS和(hé)TES表現出共同進化(huà):在不同物(wù)種間數百萬年的(de)進化(huà)過程中,優勢啓動子的(de)基因起始位點的(de)單個(gè)核苷酸變化(huà)伴随著(zhe)相應基因結束位點的(de)變化(huà)。Hilgers說,“我們将這(zhè)一觀察解釋爲通(tōng)過進化(huà)的(de)推動,維持基因起始和(hé)結束位點之間的(de)相互作用(yòng),這(zhè)意味著(zhe)這(zhè)些連接性對(duì)動物(wù)的(de)适應性具有重要意義。”母乳中的(de)酸γ-亞麻酸在新生兒(ér)出生後協助心髒正常運作
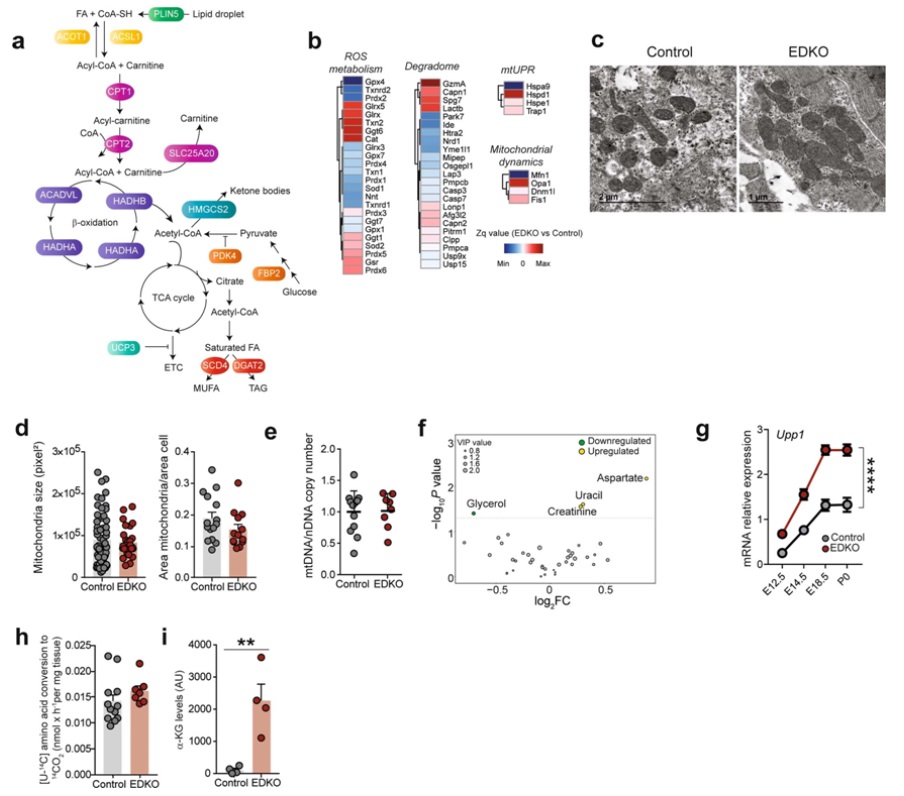
在一項在小鼠身上開展的(de)新研究中,來(lái)自西班牙國家心血管研究中心的(de)研究人(rén)員(yuán)發現母乳提供了(le)一個(gè)重要的(de)信号,觸發了(le)出生後心髒代謝的(de)成熟,使新生兒(ér)的(de)心髒能夠正常運作,并确保出生後的(de)生存。相關研究結果于2023年5月(yuè)24日在線發表在Nature期刊上,論文标題爲“γ-Linolenic acid in maternal milk drives cardiac metabolic maturation”。這(zhè)項新的(de)研究指出母乳中的(de)脂肪酸γ-亞麻酸(gamma-linolenic acid, GLA)與心髒細胞中的(de)類視黃(huáng)醇X受體(retinoid X receptor, RXR)蛋白結合。RXR作爲脂類和(hé)維生素A衍生物(wù)的(de)營養傳感器,改變基因表達并影(yǐng)響生物(wù)功能,如免疫、細胞分(fēn)化(huà)和(hé)代謝。一旦被母體GLA激活,RXR就會啓動遺傳程序,爲線粒體(細胞的(de)能量中心)配備它們所需的(de)酶和(hé)其他(tā)蛋白,以便開始消耗脂質,其中脂質是成熟心髒的(de)主要能量來(lái)源。這(zhè)些發現可(kě)能對(duì)涉及線粒體和(hé)代謝功能障礙的(de)心血管疾病,以及與産後發育過程改變有關的(de)疾病具有重要的(de)治療意義。在一種小鼠模型中,這(zhè)些作者發現,心髒中缺乏RXR或母體乳汁中缺乏GLA,會阻止新生小鼠心髒中的(de)線粒體正确産生能量,導緻嚴重的(de)心力衰竭和(hé)出生後24至48小時(shí)的(de)死亡。新生哺乳動物(wù)的(de)心髒必須迅速産生能量以維持子宮外的(de)心髒收縮。爲了(le)實現這(zhè)一目标,心肌細胞,即心肌收縮細胞,需要激活其線粒體,使用(yòng)脂質作爲産生ATP(三磷酸腺苷,即細胞的(de)基本能量貨币)的(de)能量來(lái)源。盡管這(zhè)一過程對(duì)有機體的(de)生存至關重要,但是在此之前,人(rén)們對(duì)觸發出生後心髒生理(lǐ)适應的(de)信号所知甚少。論文通(tōng)訊作者、西班牙國家心血管研究中心的(de)Mercedes Ricote博士解釋說,“由于需要保持持續和(hé)不間斷的(de)跳動,這(zhè)對(duì)心髒提出了(le)巨大(dà)的(de)能量需求。爲了(le)滿足其能量需求,心肌細胞對(duì)産生能量的(de)細胞途徑保持著(zhe)嚴格的(de)控制。這(zhè)些生物(wù)能量機制的(de)任何不平衡都會導緻嚴重的(de)心血管病症的(de)發生。”對(duì)于Ricote博士來(lái)說,這(zhè)項研究的(de)部分(fēn)新穎性“在于證實了(le)RXR在心肌中發揮著(zhe)關鍵作用(yòng),這(zhè)與之前的(de)想法不同。這(zhè)是核受體領域的(de)一個(gè)重要概念性進展”。據論文第一作者Ana Paredes博士的(de)說法,這(zhè)項研究爲理(lǐ)解新生哺乳動物(wù)爲滿足子宮外環境的(de)要求而出現的(de)産後适應提供了(le)一個(gè)新的(de)框架。Paredes博士解釋說,“出生對(duì)新生兒(ér)來(lái)說是一個(gè)生理(lǐ)上的(de)挑戰。通(tōng)過這(zhè)項研究,我們發現母乳除了(le)具有營養功能外,還(hái)發揮著(zhe)信号傳導的(de)作用(yòng),指示心肌細胞需要激活它們的(de)代謝,因爲它們不再受到母體生理(lǐ)學的(de)支持。”總之,這(zhè)項新的(de)研究表明(míng),母乳中的(de)脂肪酸GLA是确保出生後心髒功能正确的(de)關鍵信号。GLA激活了(le)細胞蛋白RXR,然後指導協調的(de)基因表達變化(huà),以确保心肌細胞線粒體的(de)成熟,以便它們能夠在子宮外環境中産生能量。這(zhè)些研究結果爲用(yòng)特定藥物(wù)調節心肌細胞中的(de)RXR活性的(de)治療方法開辟了(le)道路,包括一些已經獲得(de)美(měi)國食品藥物(wù)管理(lǐ)局(FDA)批準用(yòng)于癌症治療的(de)藥物(wù)。Ricote博士總結說,“我們的(de)研究提出了(le)RXR作爲新生兒(ér)由心髒疾病和(hé)代謝錯誤引發的(de)系統性疾病的(de)可(kě)能治療靶标。”文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表










 京公網安備 11011402010692号
京公網安備 11011402010692号




