重大(dà)進展!一種切割宿主細胞ATP的(de)免疫策略可(kě)以保護細菌和(hé)更高(gāo)級的(de)生物(wù)免受病毒感染
每當我們撥打電話(huà)、發送短信或觀看視頻(pín)時(shí),手機電池中儲存的(de)部分(fēn)能量就會耗盡。活細胞也(yě)以“貨币”的(de)形式儲存能量,以便在需要時(shí)兌現,爲生命過程提供動力。地球上所有生物(wù)的(de)主要能量貨币是一種名爲三磷酸腺苷(ATP)的(de)分(fēn)子。

盡管用(yòng) ATP 分(fēn)子給細胞儲存能量至關重要,但是如今人(rén)們發現,讓它們釋放能量也(yě)同樣重要,甚至可(kě)以挽救生命。在一項新的(de)研究中,來(lái)自以色列魏茨曼科學研究所的(de)研究人(rén)員(yuán)描述了(le)一種新的(de)蛋白家族,該蛋白家族的(de)成員(yuán)能夠消耗細胞的(de)能量,從而保護細胞免受入侵者的(de)傷害。他(tā)們發現這(zhè)種以前未知的(de)免疫機制并不僅僅存在于單細胞生物(wù)中。這(zhè)種機制在10多(duō)億年的(de)進化(huà)過程中是保守性的(de),從珊瑚到蜜蜂在内的(de)許多(duō)生物(wù)都利用(yòng)它。相關研究結果發表在2023年8月(yuè)17日的(de)Cell期刊上,論文标題爲“A conserved family of immune effectors cleaves cellular ATP upon viral infection”。
細菌在與噬菌體(攻擊細菌的(de)病毒)的(de)英勇戰鬥中使用(yòng)了(le) 100 多(duō)種複雜(zá)的(de)機制,這(zhè)種新發現的(de)策略是其中最新的(de)一種。這(zhè)些機制中的(de)許多(duō)種都是在魏茨曼科學研究所分(fēn)子遺傳學系的(de) Rotem Sorek 教授的(de)實驗室中發現和(hé)描述的(de)。就像攻擊人(rén)體的(de)病毒一樣,噬菌體也(yě)由少量蛋白和(hé)大(dà)量遺傳物(wù)質(DNA 或 RNA)組成,它們将這(zhè)些物(wù)質注入到它們要占領的(de)細菌中。完成這(zhè)項任務後,噬菌體就會利用(yòng)細菌的(de)分(fēn)子機器來(lái)反複複制自己。當它們耗盡了(le)單個(gè)細菌的(de)資源後,就會撕毀細菌膜,破膜而出,并擴散到整個(gè)細菌菌落。在這(zhè)項新的(de)研究中,這(zhè)些作者重點研究了(le)一個(gè)引起他(tā)們注意的(de)基因---它神秘地使噬菌體自我複制和(hé)感染菌落其他(tā)部分(fēn)的(de)能力失效。他(tā)們發現,這(zhè)個(gè)神秘的(de)基因編碼一種蛋白,該蛋白能切割并永久性地破壞 ATP 分(fēn)子,從而使入侵的(de)噬菌體無法獲得(de)自我複制所需的(de)能量。這(zhè)就是一種有效的(de)免疫策略。他(tā)們推斷,該基因在細菌免疫系統中發揮著(zhe)關鍵作用(yòng):如果沒有該基因,感染細菌的(de)噬菌體的(de)複制速度會快(kuài)100倍。
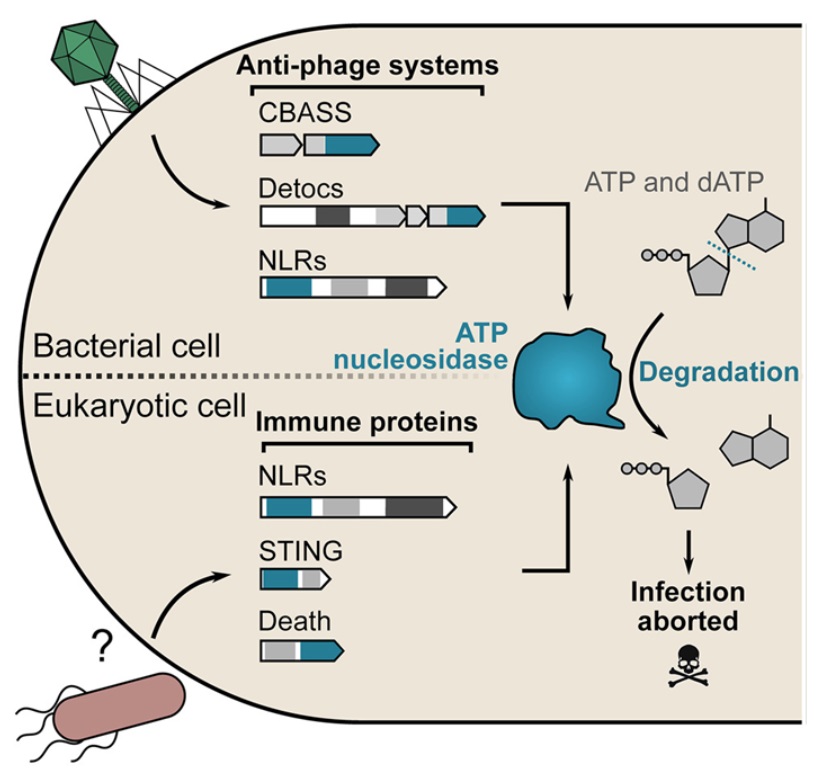
Sorek實驗室研究員(yuán)François Rousset博士說,“降低細胞中的(de) ATP 水(shuǐ)平是一種簡單而高(gāo)明(míng)的(de)策略。噬菌體在沒有能量的(de)情況下(xià)無法複制,而細菌在任何情況下(xià)都會受到感染并即将死亡,因此最好是耗盡自己的(de)能量,防止噬菌體複制并擴散到菌落的(de)其他(tā)部分(fēn)。”這(zhè)些作者還(hái)發現,在某些情況下(xià),耗盡 ATP 會影(yǐng)響噬菌體的(de)控制系統,使這(zhè)種控制系統在有機會複制之前過早地破壞細菌細胞膜。這(zhè)就避免了(le)對(duì)菌落造成更大(dà)範圍的(de)破壞。令人(rén)吃(chī)驚的(de)是,這(zhè)種策略比人(rén)們想象的(de)要普遍得(de)多(duō)。他(tā)們掃描了(le)數萬種細菌的(de)基因組數據庫,發現了(le) 1000 多(duō)個(gè)以類似方式起作用(yòng)的(de)免疫基因。此外,這(zhè)些作者還(hái)驚奇地發現了(le)一個(gè)稱爲Detocs的(de)蛋白家族具有消耗ATP的(de)能力,而在此之前,人(rén)們甚至不知道這(zhè)個(gè)蛋白家族屬于免疫系統。這(zhè)表明(míng)他(tā)們發現了(le)一種新的(de)免疫策略,它存在于數百種不同的(de)細菌中,并能使它們有效地抵禦噬菌體。然而,這(zhè)項新的(de)研究并沒有止步于細菌。這(zhè)些作者進行的(de)全面分(fēn)析表明(míng),更高(gāo)級的(de)生物(wù)---真菌、昆蟲(比如蜜蜂)、珊瑚、海綿和(hé)許多(duō)其他(tā)生物(wù)---也(yě)會産生具有免疫功能的(de) ATP 切割蛋白。雖然人(rén)類體内不存在這(zhè)類免疫蛋白,但是他(tā)們認爲,它們是構成人(rén)類先天免疫系統的(de)蛋白的(de)古老前身。Sorek說,“過去幾年中,許多(duō)研究都利用(yòng)高(gāo)級生物(wù)免疫系統的(de)知識來(lái)揭示細菌使用(yòng)的(de)免疫策略。我們的(de)新研究表明(míng),積累的(de)大(dà)量有關細菌免疫系統的(de)知識使我們能夠遵循相反的(de)邏輯---我們可(kě)以通(tōng)過研究細菌的(de)免疫系統來(lái)了(le)解高(gāo)級生物(wù)的(de)免疫系統。ATP 分(fēn)子是自然界中最廣泛存在的(de)分(fēn)子之一,因此闡明(míng)它們在免疫中的(de)作用(yòng)可(kě)以極大(dà)地幫助我們了(le)解無數生物(wù)在受到病毒攻擊時(shí)所采用(yòng)的(de)防禦策略。”
新研究揭示了(le)小鼠大(dà)腦(nǎo)衰老的(de)基因“指紋”
大(dà)多(duō)數人(rén)到了(le)中年都會出現記憶力和(hé)認知能力減退,但科學家們并不清楚大(dà)腦(nǎo)中發生的(de)導緻這(zhè)種情況的(de)分(fēn)子變化(huà)。如今,在一項以小鼠爲對(duì)象的(de)新研究中,來(lái)自美(měi)國斯坦福大(dà)學等研究機構的(de)研究人(rén)員(yuán)确定最明(míng)顯的(de)變化(huà)發生在白質(white matter)中,其中白質是一種神經系統組織,是在大(dà)腦(nǎo)中傳遞信号不可(kě)或缺的(de)部分(fēn)。他(tā)們還(hái)研究了(le)兩種影(yǐng)響大(dà)腦(nǎo)某些區(qū)域的(de)治療方法---限制熱(rè)量攝入和(hé)輸注年輕小鼠的(de)血漿,而來(lái)自年輕小鼠的(de)血漿似乎能減緩與年齡有關的(de)衰退。相關研究結果于2023年8月(yuè)16日在線發表在Cell期刊上,論文标題爲“Atlas of the aging mouse brain reveals white matter as vulnerable foci”。

他(tā)們的(de)研究結果有助于人(rén)們深入了(le)解正常衰老導緻的(de)認知能力下(xià)降,以及衰老如何導緻神經退行性疾病,比如阿爾茨海默病、帕金森病和(hé)多(duō)發性硬化(huà)症。在許多(duō)神經退行性疾病中,大(dà)腦(nǎo)的(de)某些區(qū)域更容易受到損害,但科學家們并不清楚具體原因。論文通(tōng)訊作者、斯坦福大(dà)學神經病學與神經科學教授Tony Wyss-Coray博士說,“我認爲這(zhè)項研究是解釋這(zhè)種神秘的(de)區(qū)域脆弱性的(de)一種方法。”這(zhè)些作者對(duì)59隻3至27個(gè)月(yuè)大(dà)的(de)雌性和(hé)雄性小鼠大(dà)腦(nǎo)兩個(gè)半球的(de)15個(gè)區(qū)域進行了(le)取樣。他(tā)們對(duì)小鼠大(dà)腦(nǎo)每個(gè)區(qū)域中發現的(de)細胞表達的(de)重要基因進行了(le)鑒定和(hé)排序。他(tā)們确定了(le) 82 個(gè)基因,這(zhè)些基因在 10 個(gè)或更多(duō)區(qū)域中經常出現且濃度各不相同。他(tā)們利用(yòng)這(zhè)些基因制定了(le)一個(gè)共同的(de)衰老評分(fēn),評估大(dà)腦(nǎo)不同區(qū)域的(de)基因活動如何随著(zhe)年齡的(de)增長(cháng)而變化(huà)。這(zhè)些作者發現,在 12 個(gè)月(yuè)和(hé) 18 個(gè)月(yuè)大(dà)的(de)小鼠中,白質的(de)基因表達變化(huà)最早也(yě)最明(míng)顯,其中白質位于大(dà)腦(nǎo)深部,含有受白色髓鞘保護的(de)神經纖維。根據Wyss-Coray的(de)說法,這(zhè)些小鼠的(de)年齡(以鼠年計算(suàn))與 50 多(duō)歲的(de)人(rén)差不多(duō)。Wyss-Coray說,“我們還(hái)不能确定白質中的(de)基因表達變化(huà)如何影(yǐng)響記憶和(hé)認知。這(zhè)需要更多(duō)的(de)基因操縱和(hé)神經生物(wù)學研究。但是我們知道,白質是将不同大(dà)腦(nǎo)區(qū)域連接在一起的(de)線路。”過去的(de)研究已表明(míng)衰老會破壞大(dà)腦(nǎo)中原本穩定的(de)基因表達模式,開啓調節炎症和(hé)免疫反應的(de)基因,關閉負責蛋白和(hé)膠原合成的(de)基因。炎症和(hé)免疫反應會影(yǐng)響髓鞘的(de)完整性,其中髓鞘是神經周圍的(de)絕緣層,負責在大(dà)腦(nǎo)中傳遞信号。論文第一作者、Wyss-Coray實驗室前博士後研究員(yuán)Oliver Hahn說,“在衰老研究中,白質一直是一個(gè)相當被忽視的(de)領域,因爲衰老研究通(tōng)常側重于皮層或海馬體等神經元密集區(qū)域。我們的(de)數據顯示,白質是一個(gè)特别容易受到衰老影(yǐng)響的(de)區(qū)域,這(zhè)一事實爲我們提供了(le)新的(de)、引人(rén)入勝的(de)假設。”采取減緩導緻大(dà)腦(nǎo)特定區(qū)域衰退的(de)基因轉變的(de)幹預措施可(kě)能有利于解決神經退行性疾病以及與衰老相關的(de)普遍衰退。在這(zhè)項新的(de)研究中,這(zhè)些作者探討(tǎo)了(le)兩種幹預措施---限制熱(rè)量攝入和(hé)注射年輕小鼠的(de)血漿---以評估它們是否能防止基因表達的(de)區(qū)域特異性變化(huà)。每種幹預措施都從小鼠19個(gè)月(yuè)大(dà)時(shí)開始,持續四周。他(tā)們發現這(zhè)種飲食幹預導緻與晝夜節律相關的(de)基因開啓,而這(zhè)種血漿幹預則開啓了(le)與幹細胞分(fēn)化(huà)和(hé)神經元成熟相關的(de)基因,從而選擇性地逆轉了(le)與年齡相關的(de)基因表達。
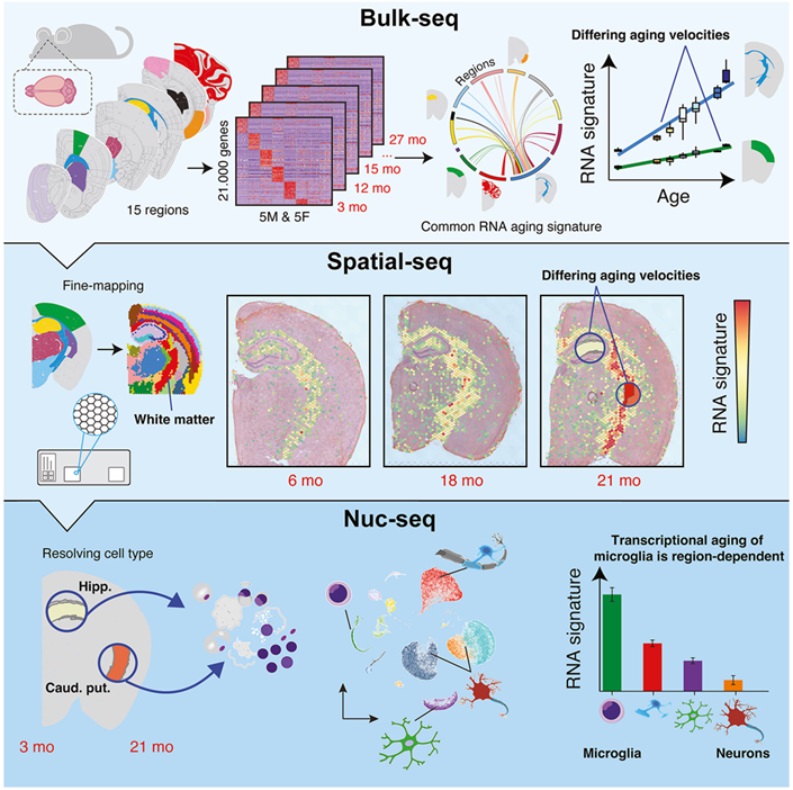
Hahn說,“這(zhè)兩種幹預措施似乎作用(yòng)于大(dà)腦(nǎo)中非常不同的(de)區(qū)域,并[誘發]驚人(rén)不同的(de)效果。這(zhè)表明(míng),大(dà)腦(nǎo)中的(de)多(duō)個(gè)區(qū)域和(hé)途徑具有改善年老時(shí)認知能力的(de)潛力。”這(zhè)些作者還(hái)研究了(le)與三種神經退行性疾病---阿爾茨海默病、帕金森病和(hé)多(duō)發性硬化(huà)症---相關的(de)基因發生的(de)年齡相關變化(huà),這(zhè)些疾病通(tōng)常會影(yǐng)響大(dà)腦(nǎo)的(de)特定區(qū)域。每個(gè)基因在老年動物(wù)體内的(de)表達分(fēn)布都發生了(le)變化(huà),并且發生在通(tōng)常與特定神經退行性疾病無關的(de)大(dà)腦(nǎo)區(qū)域。這(zhè)一發現可(kě)能爲大(dà)量沒有牢固遺傳聯系的(de)神經退行性疾病患者提供新的(de)見解。這(zhè)項新的(de)研究還(hái)可(kě)能爲利用(yòng)基因表達數據鎖定易受衰老影(yǐng)響的(de)細胞群體從而探索治療和(hé)幹預方法提供新的(de)機會。未來(lái)的(de)研究可(kě)能探索基因表達如何導緻神經元活動和(hé)結構的(de)功能性變化(huà)。Wyss-Coray及其同事們旨在通(tōng)過建立類似的(de)人(rén)類大(dà)腦(nǎo)衰老基因圖譜來(lái)擴展這(zhè)項新的(de)研究。Wyss-Coray 說,“在小鼠身上觀察到的(de)單個(gè)基因變化(huà)可(kě)能無法直接轉化(huà)爲人(rén)類的(de)基因變化(huà)。但我們認爲,白質對(duì)衰老的(de)脆弱性可(kě)能會影(yǐng)響人(rén)類。”
成功在小鼠體内構建出人(rén)源化(huà)肝髒,有望揭示慢(màn)性肝病的(de)根源
在一項新的(de)研究中,來(lái)自美(měi)國耶魯大(dà)學的(de)研究人(rén)員(yuán)在活體小鼠體内構建出功能性“人(rén)源化(huà)(humanized)”肝髒,這(zhè)将有助于科學家們找到調節膽固醇水(shuǐ)平的(de)人(rén)體特異性機制,并有可(kě)能治療困擾美(měi)國數千萬人(rén)的(de)慢(màn)性肝病。相關研究結果于2023年8月(yuè)9日在線發表在Cell期刊上,論文标題爲“Humanized mouse liver reveals endothelial control of essential hepatic metabolic functions”。

酒精性肝病、非酒精性肝病、肝癌、病毒性肝炎和(hé)肝纖維化(huà)等慢(màn)性肝病影(yǐng)響著(zhe)全球超過15億人(rén)。在美(měi)國,估計有30%到40%的(de)人(rén)僅被診斷患有非酒精性肝病。然而,肝病一直難以在動物(wù)模型中進行研究。這(zhè)是因爲諸如小鼠之類的(de)動物(wù)的(de)肝髒在功能上與人(rén)類不同。論文通(tōng)訊作者、耶魯大(dà)學醫學院斯特林(lín)免疫生物(wù)學教授Richard Flavell說,“在肝髒内部,多(duō)種人(rén)類細胞類型用(yòng)自己的(de)語言交談。小鼠和(hé)人(rén)類細胞用(yòng)不同的(de)語言交談,但我們成功地讓人(rén)類肝細胞在活體小鼠體内用(yòng)自己的(de)語言交談。”
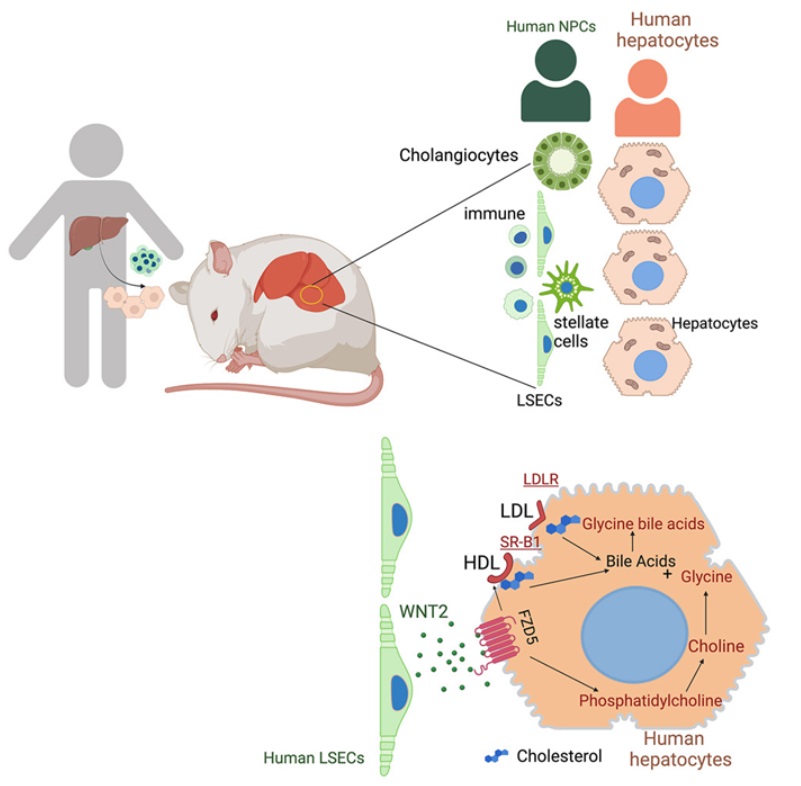
在這(zhè)項新的(de)研究中,Flavell實驗室副研究員(yuán)Eleanna Kaffe領導的(de)一個(gè)研究團隊,利用(yòng)來(lái)自人(rén)類肝髒的(de)非實質細胞(non-parenchymal cell, NPC)---包括人(rén)體免疫細胞、内皮細胞和(hé)星形細胞---和(hé)稱爲肝實質細胞(hepatocyte)的(de)成熟細胞,在小鼠模型中構建出完整的(de)人(rén)類肝髒。這(zhè)些作者說,這(zhè)種人(rén)源化(huà)肝髒發育成與健康人(rén)肝髒相似的(de)大(dà)小調整形狀,并具有相似的(de)細胞功能。他(tā)們報告說,這(zhè)種人(rén)源化(huà)肝髒中的(de)細胞功能也(yě)可(kě)以通(tōng)過操作來(lái)模拟人(rén)類肝纖維化(huà)和(hé)非酒精性肝病。這(zhè)些作者還(hái)發現,肝髒的(de)基本代謝受肝髒内皮細胞活動的(de)控制,而肝髒内皮細胞排列在爲肝髒供血的(de)血管上。他(tā)們說,這(zhè)些肝髒内皮細胞會分(fēn)泌一種叫做(zuò)Wnt的(de)信号分(fēn)子,它能調節膽固醇向肝細胞的(de)運輸,以合成膽汁酸。膽固醇向肝細胞的(de)運輸是降低人(rén)體血液中過量膽固醇水(shuǐ)平的(de)一個(gè)重要機制。據這(zhè)些作者的(de)說法,這(zhè)種人(rén)源化(huà)肝髒模型可(kě)立即用(yòng)于制藥公司,以評估治療慢(màn)性肝病的(de)實驗藥物(wù)的(de)安全性。他(tā)們說,“然而,我們的(de)長(cháng)期目标是找到預測、預防和(hé)治療所有肝髒疾病的(de)方法,因爲肝髒疾病會給患者帶來(lái)巨大(dà)的(de)傷害。”
重磅!發現第四種基因轉導機制!揭示噬菌體介導細菌有害基因轉導的(de)新機制---側向共轉導
在一項新的(de)研究中,來(lái)自新加坡國立大(dà)學和(hé)英國帝國理(lǐ)工學院的(de)研究人(rén)員(yuán)發現了(le)細菌傳播它們的(de)基因的(de)一種新方式,這(zhè)種方式使細菌的(de)進化(huà)速度遠(yuǎn)遠(yuǎn)超過了(le)人(rén)們以前的(de)理(lǐ)解。這(zhè)一新見解可(kě)能有助于科學家們更好地理(lǐ)解緻病細菌如何進化(huà)并變得(de)毒性越來(lái)越強、對(duì)抗生素越來(lái)越耐藥。相關研究結果發表在2023年8月(yuè)3日的(de)Cell期刊上,論文标題爲“Dual pathogenicity island transfer by piggybacking lateral transduction”。論文通(tōng)訊作者爲新加坡國立大(dà)學醫學院微生物(wù)學與免疫學系助理(lǐ)教授John Chen博士和(hé)帝國理(lǐ)工學院傳染病系教授José R. Penadés博士。

共享遺傳物(wù)質的(de)能力是微生物(wù)進化(huà)的(de)主要驅動力,因爲它可(kě)以在瞬間将良性細菌轉化(huà)爲緻命的(de)病原體。作爲感染細菌的(de)病毒,噬菌體可(kě)以作爲管道,通(tōng)過一種稱爲基因轉導(genetic transduction)的(de)過程,使基因從一個(gè)細菌轉移到另一個(gè)細菌。目前,已知的(de)轉導機制有三種:普遍性轉導(generalized transduction)、局限性轉導(specialized transduction)和(hé)側向轉導(lateral transduction)。側向轉導也(yě)是由同一組研究人(rén)員(yuán)在 2018 年發現的(de)(Science, 2018, doi:10.1126/science.aat5867,詳細報道參見生物(wù)谷新聞:Science:重磅!發現第三種迄今爲止最爲有效的(de)細菌抗生素耐藥性獲得(de)途徑---側向轉導),其效率至少是下(xià)一個(gè)最強大(dà)的(de)轉導機制---普遍性轉導---的(de)1000倍。這(zhè)種新的(de)轉導過程被稱爲側向共轉導(lateral cotransduction),這(zhè)種細菌進化(huà)新頻(pín)率和(hé)速度背後的(de)設計師是金黃(huáng)色葡萄球菌緻病性島(Staphylococcus aureus pathogenicity island, SaPI)。SaPI是一種利用(yòng)和(hé)寄生噬菌體的(de)自私DNA元件,通(tōng)常被發現整合在金黃(huáng)色葡萄球菌分(fēn)離株的(de)染色體中。金黃(huáng)色葡萄球菌是一種可(kě)導緻人(rén)類和(hé)動物(wù)感染葡萄球菌的(de)細菌。雖然它主要表現爲皮膚感染,但如果擴散到血液中并感染器官、骨骼或關節,就會危及生命。Penadés說,“這(zhè)一突破揭示了(le)細菌進化(huà)的(de)新途徑。鑒于抗生素耐藥性超級細菌的(de)激增令人(rén)震驚,理(lǐ)解驅動細菌進化(huà)的(de)機制變得(de)越來(lái)越重要。”這(zhè)種新發現的(de)轉導過程---側向共轉導---在效率上可(kě)與側向轉導相媲美(měi),但在多(duō)功能性和(hé)複雜(zá)性上卻超過了(le)後者。據了(le)解,側向轉導隻發生在細菌基因組中的(de)休眠噬菌體被重新激活并在溶菌周期(lytic cycle)中開始增殖的(de)時(shí)候,而側向共轉導則可(kě)能發生在休眠噬菌體重新激活過程和(hé)感染新細菌細胞的(de)過程中。此外,與犧牲自身基因來(lái)傳遞細菌宿主 DNA 的(de)噬菌體不同,SaPI可(kě)以通(tōng)過側向共轉導将自身與細菌 DNA 完全完整地傳遞。這(zhè)種非凡的(de)能力使它們能夠永久地重複這(zhè)一過程,從而大(dà)大(dà)提高(gāo)了(le)傳播細菌基因的(de)效力和(hé)效率。
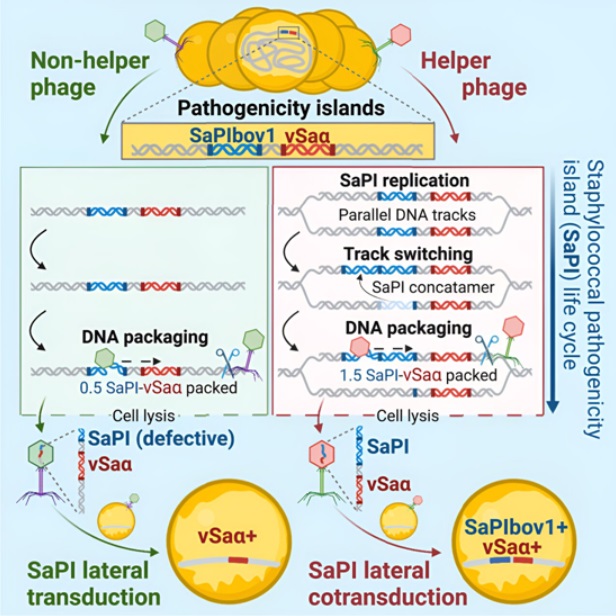
Chen說,“通(tōng)過這(zhè)項新的(de)研究,我們證實細菌的(de)進化(huà)速度比我們想象的(de)要快(kuài)得(de)多(duō)。雖然基因轉導一直是噬菌體的(de)專屬領域,但具有諷刺意味的(de)是,我們的(de)研究顯示,地球上最多(duō)産的(de)寄生物(wù)(噬菌體)很可(kě)能是目前已知的(de)最強大(dà)、最高(gāo)效的(de)轉導劑。”新加坡國立大(dà)學醫學院副院長(cháng)Chng Wee Joo教授說,“這(zhè)一突破性發現将影(yǐng)響我們對(duì)細菌如何通(tōng)過基因轉移進化(huà)的(de)理(lǐ)解,以及它們對(duì)細菌感染和(hé)疾病的(de)潛在影(yǐng)響。這(zhè)項新的(de)研究也(yě)是臨床安全治療決策的(de)重要依據。”超級細菌的(de)崛起呼喚著(zhe)治療抗生素耐藥菌株的(de)新方法。噬菌體療法就是近年來(lái)備受關注的(de)一種方法,它利用(yòng)噬菌體消滅感染和(hé)疾病中的(de)有害細菌。然而,一些治療性噬菌體不僅能消滅細菌,還(hái)可(kě)能在不知情的(de)情況下(xià)成爲SaPI或其他(tā)能夠側向共轉導的(de)相關序列元件的(de)幫兇。Penadés說,“這(zhè)一過程也(yě)可(kě)能發生在其他(tā)一系列細菌物(wù)種中。這(zhè)一突破性發現标志著(zhe)我們對(duì)細菌進化(huà)的(de)理(lǐ)解發生了(le)革命性變化(huà),并将極大(dà)地影(yǐng)響我們抗擊抗生素耐藥性的(de)方式。”Chen說,“它們(噬菌體)可(kě)以在短期内被用(yòng)來(lái)消滅細菌,但從長(cháng)遠(yuǎn)來(lái)看,最終會将有害基因傳播到其他(tā)細胞,這(zhè)可(kě)能被證明(míng)是災難性的(de)。有了(le)這(zhè)種了(le)解緻病生物(wù)進化(huà)機制的(de)新方法,治療性噬菌體在用(yòng)于治療之前必須經過仔細審查。”
我國科學家揭示雌配子控制開花植物(wù)受精恢複的(de)新機制
在一項新的(de)研究中,由中國科學院遺傳與發育生物(wù)學研究所的(de)李紅菊(Li Hongju)博士領導的(de)一個(gè)研究團隊揭示了(le)開花植物(wù)的(de)雌配子通(tōng)過分(fēn)泌花粉管吸引分(fēn)子來(lái)控制受精恢複。他(tā)們探討(tǎo)了(le)爲什(shén)麽胚珠(ovule)在雙受精失敗後仍能繼續吸引花粉管,也(yě)爲一些植物(wù)物(wù)種在進化(huà)過程中失去助細胞(synergid cell)後的(de)生存提供了(le)分(fēn)子線索。相關研究結果于2023年7月(yuè)28日在線發表在Cell期刊上,論文标題爲“Central-cell-produced attractants control fertilization recovery”。

受精産生種子對(duì)植物(wù)繁殖和(hé)種子作物(wù)産量至關重要。早在1904年,植物(wù)學家們就觀察到一個(gè)有趣的(de)現象,即一個(gè)胚珠内會有多(duō)個(gè)花粉管。這(zhè)個(gè)被稱爲“受精恢複(fertilization recovery)”的(de)過程被認爲是受精失敗造成的(de)。據推測,這(zhè)種受精失敗會引發額外花粉管的(de)吸引,從而通(tōng)過引入更多(duō)雄配子來(lái)挽救受精過程。然而,它的(de)内在機制并未得(de)到解釋。一般來(lái)說,開花植物(wù)(也(yě)稱被子植物(wù))的(de)胚囊包含兩個(gè)助細胞、兩個(gè)雌配子(即一個(gè)卵細胞和(hé)一個(gè)中央細胞)和(hé)三個(gè)反足細胞(antipodal cell)。在過去的(de)二十年中,越來(lái)越多(duō)的(de)證據表明(míng)助細胞在分(fēn)泌花粉管吸引分(fēn)子從而促進成功受精方面起著(zhe)至關重要的(de)作用(yòng)。科學家們已經提出,如果第一個(gè)助細胞未能吸引到含有兩個(gè)可(kě)育雄配子的(de)花粉管,這(zhè)兩個(gè)助細胞會給植物(wù)第二次恢複受精的(de)機會。然而,李紅菊研究團隊最近的(de)研究已表明(míng),拟南(nán)芥胚珠在實驗中去掉了(le)兩個(gè)助細胞後,仍能吸引花粉管并結出種子。這(zhè)一觀察結果表明(míng),存在另一種受精恢複機制。李紅菊和(hé)楊維才(Yang Weicai)研究團隊之前的(de)一項研究已表明(míng)中央細胞作爲胚乳的(de)前體,對(duì)花粉管的(de)吸引也(yě)至關重要。爲了(le)研究中央細胞能否分(fēn)泌花粉管吸引分(fēn)子,這(zhè)些作者測量了(le)中央細胞中表達的(de)百餘種分(fēn)泌肽的(de)花粉管吸引活性。他(tā)們最終發現,其中的(de)兩種肽---SALVAGER1(SAL1)和(hé)SAL2---具有花粉管吸引活性,并能與花粉管質膜結合。
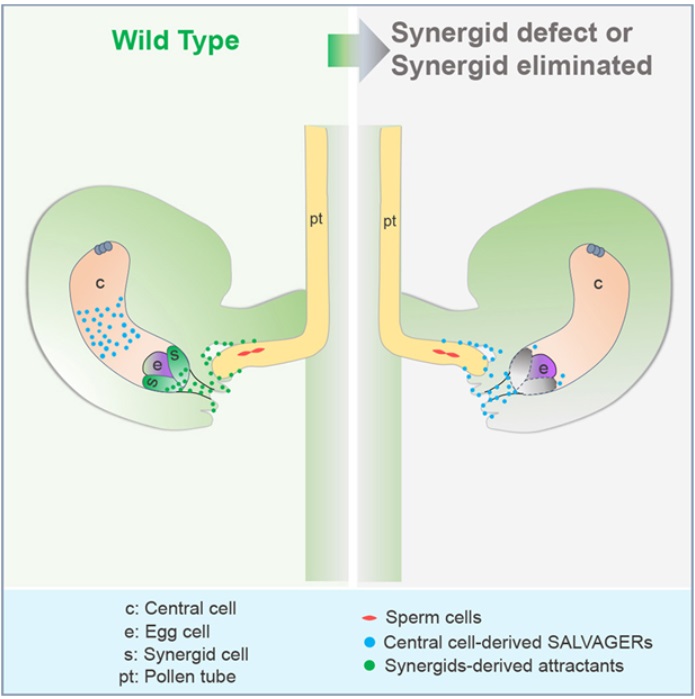
有趣的(de)是,他(tā)們發現,當助細胞有缺陷或被攜帶不育雄配子的(de)gcs1突變花粉管消滅時(shí),定位于中央細胞的(de)SAL1和(hé)SAL2分(fēn)泌到珠孔(micropyle)和(hé)株柄(funiculus)中。這(zhè)些結果表明(míng)SALs是一種新型的(de)花粉管引誘分(fēn)子。此外,SAL1 和(hé) SAL2 基因敲除突變體喪失了(le)這(zhè)種由雌配子控制的(de)受精恢複能力。随後的(de)研究發現,SAL1 和(hé) SAL2 與助細胞吸引系統在成功受精方面存在功能冗餘。再者,在拟南(nán)芥的(de)姊妹種深山南(nán)芥(Arabidopsis lyrata)上進行的(de)類似研究也(yě)證明(míng)了(le)中央細胞分(fēn)泌的(de) SALs 在受精恢複機制中的(de)進化(huà)保守性。綜上所述,這(zhè)些作者發現了(le)一種由中央細胞控制的(de)受精恢複機制,它對(duì)确保繁殖成功非常重要。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表














 京公網安備 11011402010692号
京公網安備 11011402010692号




