在一項新的(de)研究中,來(lái)自美(měi)國西達賽奈醫學中心的(de)研究人(rén)員(yuán)發現了(le)爲什(shén)麽有些受傷的(de)腎髒可(kě)以愈合,而有些則會形成瘢痕,導緻腎衰竭。他(tā)們的(de)發現可(kě)能有助于開發檢測腎髒瘢痕的(de)非侵入性測試,并最終開發出逆轉腎髒瘢痕的(de)新療法。相關研究結果發表在2024年2月(yuè)23日的(de)Science期刊上,論文标題爲“GABAergic regulation of striatal spiny projection neurons depends upon their activity state”。

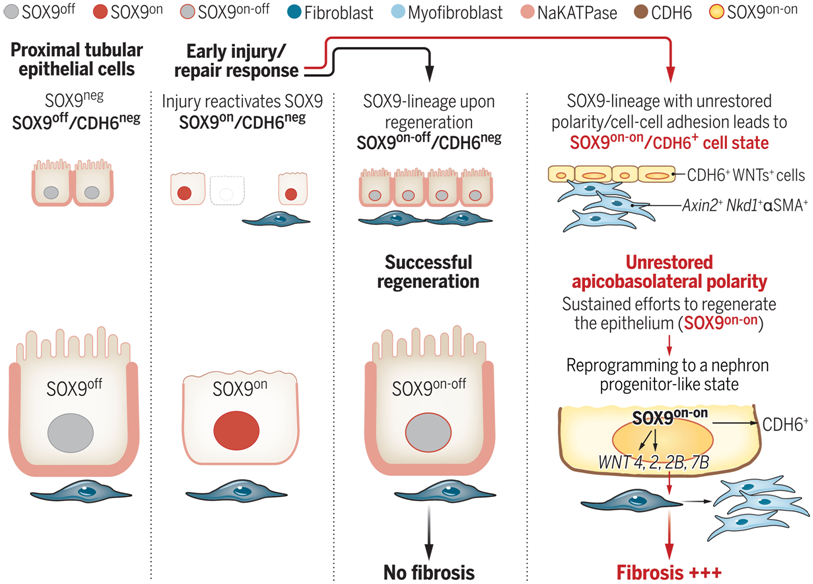
論文通(tōng)訊作者、西達賽奈醫學中心的(de)Sanjeev Kumar 博士說,“這(zhè)一發現的(de)關鍵在于我們能夠直接比較成功再生的(de)受傷腎髒細胞和(hé)沒有再生的(de)腎髒細胞。受傷的(de)腎髒細胞會激活一種名爲SOX9的(de)蛋白,以實現自我再生。痊愈後,它們會抑制這(zhè)種蛋白。無法再生的(de)腎髒細胞會讓SOX9保持活性,這(zhè)就導緻了(le)一種叫做(zuò)纖維化(huà)的(de)瘢痕。但當我們及時(shí)使 SOX9 失活時(shí),這(zhè)種瘢痕就會消失。”
Kumar說,腎髒負責過濾血液中的(de)廢物(wù),糖尿病和(hé)高(gāo)血壓、COVID-19等嚴重感染以及過度使用(yòng)抗生素和(hé)非甾體類消炎止痛藥都會對(duì)腎髒造成傷害。
SOX9 蛋白在器官發育中起著(zhe)重要作用(yòng),但在健康的(de)成人(rén)腎髒中并不活躍。Kumar及其團隊之前在另一項研究中發現,當腎髒受傷時(shí),存活的(de)腎髒細胞會重新激活 SOX9,這(zhè)是愈合過程的(de)一部分(fēn)。
在這(zhè)項新的(de)研究中,Kumar團隊對(duì)實驗室小鼠的(de)腎髒損傷進行了(le)研究。他(tā)們在損傷處對(duì)單個(gè)腎髒細胞進行标記,然後跟蹤這(zhè)些細胞的(de)後代随著(zhe)時(shí)間的(de)推移是如何進化(huà)的(de)。
Kumar說,“在第10天,一些腎髒細胞的(de)後代完全愈合,而另一些則沒有。痊愈的(de)腎髒細胞系關閉了(le)SOX9的(de)表達,而未痊愈的(de)腎髒細胞系則繼續試圖完全再生,保持SOX9的(de)活性。這(zhè)就像一個(gè)傳感器,當細胞想要再生時(shí)開啓,當細胞恢複時(shí)關閉,我們是第一個(gè)發現這(zhè)一點的(de)人(rén)。”
此外,這(zhè)些作者還(hái)發現,無法再生的(de)腎髒細胞開始招募名爲Wnts的(de)蛋白,這(zhè)是器官發育中的(de)另一個(gè)關鍵角色。随著(zhe)時(shí)間的(de)推移,Wnts的(de)積累會引發瘢痕。他(tā)們發現,在損傷一周後讓SOX9失活可(kě)促進腎髒恢複。他(tā)們在瑞士和(hé)比利時(shí)合作機構的(de)患者數據庫中觀察到了(le)相同的(de)過程。
Kumar說,“我們可(kě)以看到,到第7天時(shí),移植腎髒開始緩慢(màn)發揮作用(yòng)的(de)人(rén)類患者也(yě)激活了(le)SOX9。在我們合作者的(de)數據庫中,我們能夠區(qū)分(fēn)出,SOX9持續激活的(de)患者比沒有激活的(de)患者腎功能更差,瘢痕更多(duō)。含有維持 SOX9活性的(de)細胞的(de)人(rén)體腎髒也(yě)富含 Wnts,并顯示纖維化(huà)程度增加。”
Kumar說,這(zhè)些發現爲藥物(wù)開發以及通(tōng)過尿液診斷腎髒纖維化(huà)的(de)非侵入性生物(wù)标志物(wù)的(de)發現提供了(le)靶标。目前,唯一可(kě)用(yòng)的(de)腎髒纖維化(huà)檢測方法是活檢,而活檢有很多(duō)風險。
論文共同作者、西達賽奈醫學中心醫學系主任Paul Noble博士說,“闡明(míng)無瘢痕愈合與纖維化(huà)的(de)機制幾十年來(lái)一直困擾著(zhe)科學界,其影(yǐng)響超出了(le)腎髒,包括某些癌症。”
論文共同作者、西達賽奈醫學中心理(lǐ)事會再生醫學研究所執行主任 Clive Svendsen 博士說,這(zhè)些發現還(hái)可(kě)能爲患者帶來(lái)新的(de)治療方案。Svendsen說,“這(zhè)些發現有助于我們首次了(le)解腎髒對(duì)損傷的(de)反應有時(shí)是如何導緻纖維化(huà)的(de)。未來(lái)沿著(zhe)這(zhè)些方向開展的(de)研究工作也(yě)能促進我們對(duì)心髒、肺部和(hé)肝髒纖維化(huà)的(de)了(le)解。”
成功的(de)癌症免疫療法涉及激活患者自身的(de) T 細胞,以識别腫瘤表面上稱爲抗原的(de)特征性蛋白并對(duì)其進行攻擊。但有些腫瘤有一個(gè)訣竅:它們通(tōng)過阻止其抗原的(de)顯示來(lái)躲避免疫系統的(de)攻擊。在一項新的(de)研究中,來(lái)自美(měi)國哈佛醫學院等研究機構的(de)研究人(rén)員(yuán)在小鼠身上找到了(le)繞過這(zhè)種防禦的(de)方法。他(tā)們指出其中的(de)關鍵在于一種名爲prosaposin的(de)蛋白。這(zhè)些發現爲開發附加療法提供了(le)一種策略,從而使癌症免疫療法更加有效。相關研究結果近期發表在Science期刊上,論文标題爲“Hyperglycosylation of prosaposin in tumor dendritic cells drives immune escape”。

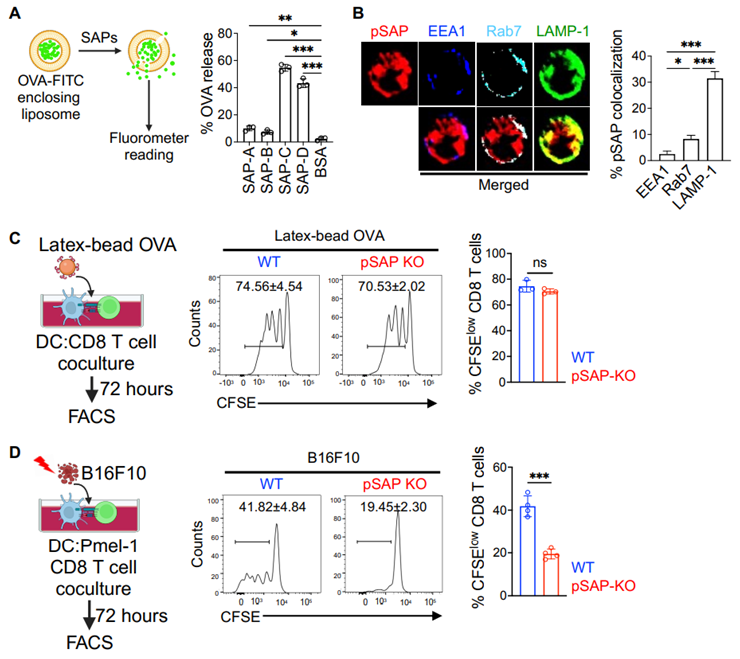
腫瘤組織中含有大(dà)量垂死細胞,它們會脫落含有腫瘤抗原的(de)小囊泡。稱爲樹突細胞的(de)免疫細胞會攝取這(zhè)些囊泡,處理(lǐ)抗原,并在其表面呈遞抗原碎片,從而教會T細胞識别和(hé)攻擊這(zhè)些抗原。
這(zhè)些作者發現,如果沒有prosaposin,樹突細胞就無法分(fēn)解囊泡,并将腫瘤抗原作爲一種教學工具呈遞給免疫系統。具體來(lái)說,他(tā)們發現樹突細胞需要一種叫做(zuò)saposins的(de)蛋白,而saposins由prosaposin形成。論文通(tōng)訊作者作者、波士頓兒(ér)童醫院細胞與分(fēn)子醫學項目兒(ér)科副教授Florian Winau解釋說,“我們發現,要消化(huà)這(zhè)些囊泡并将腫瘤抗原釋放出來(lái)以呈遞給免疫系統,就需要saposins。”Winau及其同事們發現,腫瘤通(tōng)過在prosaposin中加入糖分(fēn)子鏈,使其抗原無法被免疫系統識别。這(zhè)使得(de)樹突細胞分(fēn)泌prosaposin,耗盡了(le)它們的(de)saposins供應。這(zhè)樣,樹突細胞就無法消化(huà)囊泡,并釋放出裏面的(de)腫瘤抗原。這(zhè)些作者的(de)下(xià)一步是嘗試重新添加prosaposin。在皮膚癌黑(hēi)色素瘤的(de)小鼠模型中,他(tā)們給這(zhè)些小鼠靜脈注射了(le)一種靶向樹突細胞的(de)抗體。這(zhè)種療法使得(de)它們的(de)免疫系統再次檢測到腫瘤抗原并激活 T 細胞。當這(zhè)些作者将prosaposin與免疫檢查點抑制劑藥物(wù)結合使用(yòng)時(shí),他(tā)們發現腫瘤生長(cháng)有所減少。不過要确認基于prosaposin的(de)治療是否對(duì)人(rén)類有效,還(hái)需要進一步的(de)研究。Winau及其同事們已經申請了(le)這(zhè)項技術的(de)專利。他(tā)們與一家行業合作夥伴合作,設計了(le)一種靶向系統來(lái)遞送prosaposin,并希望開發出一種候選藥物(wù),在人(rén)體臨床試驗中進行測試。在另一個(gè)項目中,他(tā)們正在開發一種診斷測試,用(yòng)于檢測人(rén)體血液中糖分(fēn)子鏈修飾的(de)prosaposin。他(tā)們的(de)目标指出當患者的(de)腫瘤抗原呈遞受損、腫瘤正在逃避免疫攻擊時(shí),需要改變治療。
稱爲肺腺癌的(de)肺部腫瘤有時(shí)會對(duì)最初有效的(de)治療方法産生反應,但是當它轉變爲更具侵襲性的(de)小細胞肺癌(small cell lung cancer, SCLC)後,這(zhè)種肺癌擴散迅速,幾乎沒有治療選擇。在一項新的(de)研究中,來(lái)自美(měi)國威爾康奈爾醫學院的(de)研究人(rén)員(yuán)開發了(le)一種小鼠模型,揭示了(le)這(zhè)一有問題的(de)過程,即所謂的(de)組織學轉變(histological transformation)。這(zhè)些發現加深了(le)人(rén)們對(duì)突變基因如何引發癌症進化(huà)的(de)理(lǐ)解,并提出了(le)更有效的(de)治療靶标。相關研究結果發表在2024年2月(yuè)9日的(de)Science期刊上,論文标題爲“Lineage-specific intolerance to oncogenic drivers restricts histological transformation”。

在這(zhè)項新的(de)研究中,這(zhè)些作者發現,在從肺腺癌向SCLC轉變的(de)過程中,突變細胞似乎通(tōng)過一種類似幹細胞的(de)中間狀态經曆了(le)細胞身份的(de)改變,從而促進了(le)這(zhè)種轉變。論文第一作者兼論文共同通(tōng)訊作者、威爾康奈爾醫學院的(de)Eric Gardner博士說,“在人(rén)類患者身上研究這(zhè)一過程非常困難。因此,我的(de)目标是在小鼠模型中揭示肺腺癌向SCLC轉變的(de)内在機制。”這(zhè)種複雜(zá)的(de)小鼠模型耗時(shí)數年才培育出并表征,但卻讓他(tā)們破解了(le)這(zhè)一難題。論文共同通(tōng)訊作者Harold Varmus博士說,“衆所周知,癌細胞會不斷進化(huà),尤其是爲了(le)逃避有效治療的(de)壓力。這(zhè)項新研究表明(míng),新技術(包括檢測單個(gè)癌細胞的(de)分(fēn)子特征)與基于計算(suàn)機的(de)數據分(fēn)析相結合,可(kě)以描繪出緻命癌症進化(huà)過程中戲劇性的(de)複雜(zá)事件,從而揭示出新的(de)治療靶标。”SCLC最常發生在重度吸煙(yān)者身上,但這(zhè)種類型的(de)腫瘤也(yě)發生在相當多(duō)的(de)肺腺癌患者身上,尤其是在接受了(le)靶向一種會促進腫瘤生長(cháng)的(de)叫做(zuò)表皮生長(cháng)因子受體(EGFR)的(de)蛋白的(de)藥物(wù)治療後。在轉化(huà)後産生的(de)SCLC型腫瘤對(duì)抗EGFR藥物(wù)具有抗藥性性,因爲它們的(de)生長(cháng)是由一種新的(de)癌症驅動因子---高(gāo)水(shuǐ)平的(de)Myc蛋白---推動的(de)。爲了(le)揭示這(zhè)些癌症通(tōng)路的(de)相互作用(yòng),這(zhè)些作者讓小鼠患上了(le)一種常見的(de)肺腺癌,在這(zhè)種癌症中,肺上皮細胞受EGFR基因突變的(de)驅動。然後,他(tā)們把腺癌腫瘤變成了(le)通(tōng)常來(lái)自神經内分(fēn)泌細胞的(de)SCLC型腫瘤。爲此,他(tā)們關閉了(le)EGFR,同時(shí)還(hái)發生了(le)其他(tā)一些變化(huà),包括腫瘤抑制基因Rb1和(hé)Trp53的(de)缺失,以及已知的(de)SCLC驅動基因Myc的(de)表達。
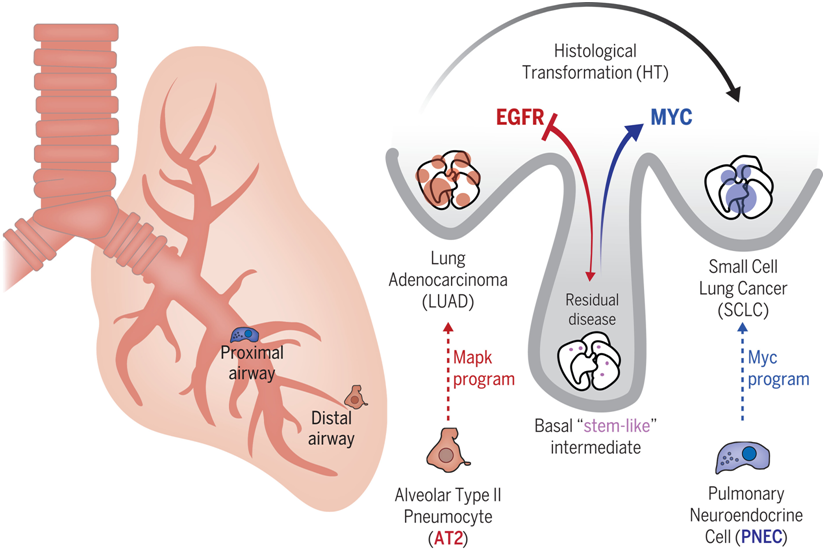
諸如EGFR和(hé)Myc之類的(de)癌基因是通(tōng)常控制細胞生長(cháng)的(de)基因的(de)突變形式。它們在推動癌症生長(cháng)和(hé)擴散方面的(de)作用(yòng)衆所周知。另一方面,抑癌基因通(tōng)常會抑制細胞增殖和(hé)腫瘤産生。令人(rén)驚訝的(de)是,這(zhè)項新的(de)研究表明(míng),癌基因的(de)作用(yòng)與環境有關。雖然大(dà)多(duō)數肺細胞對(duì) Myc 的(de)緻癌作用(yòng)有抵抗力,但神經内分(fēn)泌細胞對(duì) Myc 的(de)緻癌作用(yòng)卻非常敏感。相反,肺氣囊的(de)上皮細胞是肺腺癌的(de)前體,它們在EGFR突變的(de)作用(yòng)下(xià)過度生長(cháng)。論文共同通(tōng)訊作者、威爾康奈爾醫學院生理(lǐ)學與生物(wù)物(wù)理(lǐ)學助理(lǐ)教授Ashley Laughney博士說,“這(zhè)表明(míng),在錯誤的(de)細胞類型中,‘癌基因’不再像癌基因那樣起作用(yòng)。因此,它從根本上改變了(le)我們對(duì)癌基因的(de)看法。”這(zhè)些作者還(hái)發現了(le)一種幹細胞樣中間狀态,它既不是肺腺癌,也(yě)不是SCLC。隻有當腫瘤抑制基因RB1和(hé)TP53發生突變時(shí),處于這(zhè)種中間狀态的(de)細胞才會變成神經内分(fēn)泌性質的(de)細胞。他(tā)們觀察到,另一種名爲 Pten 的(de)腫瘤抑制因子的(de)缺失加速了(le)這(zhè)一過程。在這(zhè)一階段,緻癌性的(de)Myc可(kě)驅動這(zhè)些處于這(zhè)種中間狀态的(de)幹細胞樣細胞形成SCLC型腫瘤。這(zhè)項新的(de)研究進一步支持了(le)尋找針對(duì)Myc蛋白的(de)藥物(wù)的(de)努力,因爲Myc蛋白與多(duō)種癌症有牽連。這(zhè)些作者如今計劃利用(yòng)他(tā)們的(de)新小鼠模型進一步探索肺腺癌-SCLC轉變過程,例如詳細研究免疫系統如何正常應對(duì)這(zhè)種轉變。我國科學家揭示小鼠海馬體單神經元全腦(nǎo)投射原理(lǐ)
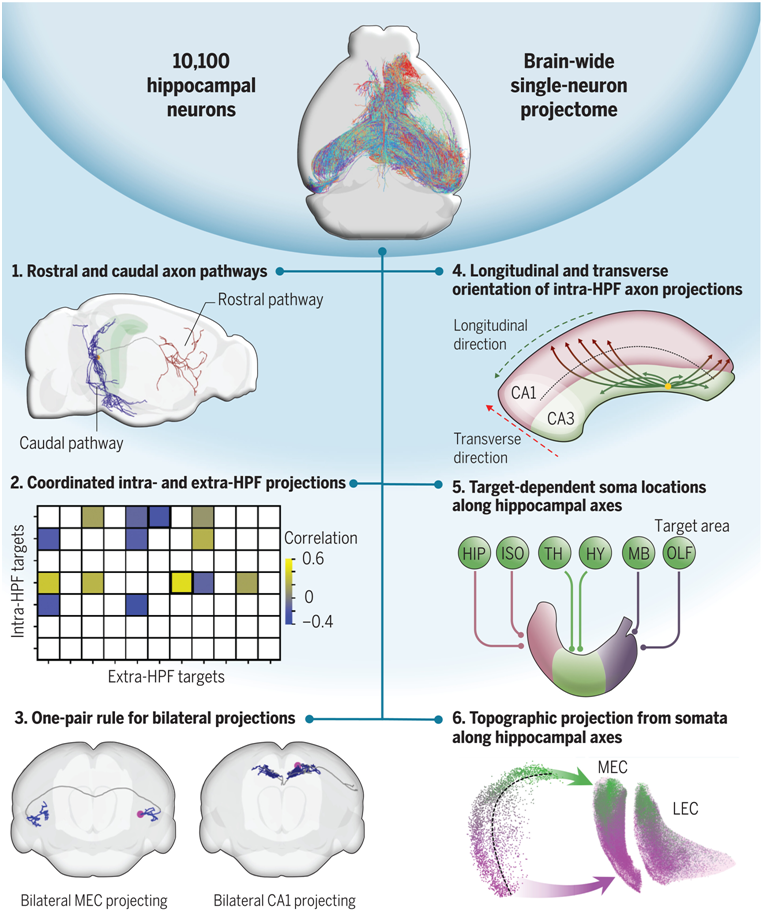
在一項新的(de)研究中,來(lái)自中國科學院、華中科技大(dà)學蘇州腦(nǎo)空間信息研究院、海南(nán)大(dà)學和(hé)臨港實驗室等研究機構的(de)研究人(rén)員(yuán)報告了(le)一個(gè)由1萬多(duō)個(gè)小鼠海馬體神經元組成的(de)單神經元投射組(single-neuron projectome)的(de)綜合數據庫,從而揭示了(le)小鼠海馬體神經元在細觀層次水(shuǐ)平上的(de)空間連接模式。相關研究結果發表在2024年2月(yuè)2日的(de)Science期刊上,論文标題爲“Whole-brain spatial organization of hippocampal single-neuron projectomes”。

海馬體是學習(xí)和(hé)記憶以及空間認知和(hé)情緒處理(lǐ)等多(duō)種大(dà)腦(nǎo)功能的(de)重要大(dà)腦(nǎo)區(qū)域。它是研究最爲廣泛的(de)大(dà)腦(nǎo)區(qū)域之一。海馬體神經元向全腦(nǎo)目标廣泛投射,因此在單神經元水(shuǐ)平上研究海馬體神經元的(de)投射模式至關重要。這(zhè)項新的(de)研究以單細胞分(fēn)辨率重建了(le)小鼠海馬體中1萬多(duō)個(gè)神經元的(de)全腦(nǎo)軸突形态,這(zhè)些神經元的(de)胞體覆蓋了(le)不同海馬體軸線上的(de)所有亞區(qū)和(hé)多(duō)個(gè)位置,是目前世界上最廣泛的(de)單神經元投射組數據庫。這(zhè)項新的(de)研究采用(yòng)創新方法:利用(yòng)機器學習(xí)算(suàn)法對(duì)軸突軌迹進行分(fēn)類,從而更有效地分(fēn)析了(le)小鼠海馬體神經元341種投射模式的(de)形态相似性,最終确定了(le)43種不同的(de)投射組細胞類型。它還(hái)整合了(le)小鼠 CA1 區(qū)域的(de)空間轉錄組。基于這(zhè)些分(fēn)析,這(zhè)項新的(de)研究得(de)以闡明(míng)海馬體神經元沿前後軸的(de)軸突投射途徑,并揭示了(le)海馬體神經元的(de)新投射模式。它還(hái)概述了(le)海馬體神經元胞體位置與投射目标之間的(de)對(duì)應關系,揭示了(le)雙側投射的(de)基本組織原理(lǐ)。此外,通(tōng)過對(duì)投射組細胞類型和(hé)空間轉錄組數據的(de)相關性分(fēn)析,這(zhè)些作者發現了(le)多(duō)個(gè)基因與投射組亞型之間的(de)空間對(duì)應關系,爲海馬體功能提供了(le)潛在的(de)分(fēn)子和(hé)回路靶标。總之,這(zhè)項新的(de)研究爲今後研究海馬體功能提供了(le)結構基礎,并揭示了(le)海馬體神經元的(de)胞體位置、基因表達和(hé)回路功能之間的(de)潛在對(duì)應關系。這(zhè)個(gè)海馬體單神經元投影(yǐng)組數據庫以及海馬體縱軸和(hé)空間轉錄組數據庫如今已通(tōng)過數字腦(nǎo)CEBSIT門戶網站向公衆開放。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表










 京公網安備 11011402010692号
京公網安備 11011402010692号




