在細胞分(fēn)裂過程中,新的(de)子細胞會從母細胞那裏繼承遺傳物(wù)質和(hé)其他(tā)分(fēn)子的(de)混合物(wù)。這(zhè)種遺傳既包括有益的(de)成分(fēn),可(kě)以幫助它們在生命中有一個(gè)強健的(de)開端,也(yě)包括潛在的(de)有害突變或受損分(fēn)子,給新生的(de)子細胞帶來(lái)巨大(dà)挑戰。
子細胞如何控制和(hé)減輕有害遺傳的(de)影(yǐng)響一直是個(gè)謎。在一項新的(de)研究中,來(lái)自德國馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所的(de)研究人(rén)員(yuán)揭示了(le)一種複雜(zá)的(de)機制,通(tōng)過這(zhè)種機制,子細胞可(kě)以保護自己免受從母細胞遺傳而來(lái)的(de)受紫外線破壞的(de)RNA的(de)傷害。相關研究結果于2024年3月(yuè)18日在線發表在Cell期刊上,論文标題爲“RNA damage compartmentalization by DHX9 stress granules”。

當太陽光(guāng)照(zhào)射到我們的(de)皮膚上時(shí),會給我們帶來(lái)溫暖和(hé)活力。然而,在這(zhè)溫柔的(de)懷抱下(xià)卻隐藏著(zhe)潛在的(de)威脅:紫外線(UV)照(zhào)射,陽光(guāng)中能量最高(gāo)的(de)成分(fēn)。雖然我們都知道紫外線會破壞 DNA 并導緻皮膚癌,但它對(duì)另一種重要分(fēn)子——RNA的(de)影(yǐng)響卻往往不被人(rén)注意。
在測試細胞對(duì)多(duō)種應激源的(de)反應時(shí),這(zhè)些作者注意到了(le)一些耐人(rén)尋味的(de)現象:紫外線照(zhào)射後,一種名爲DHX9的(de)蛋白在細胞質内聚集成液滴結構。
論文通(tōng)訊作者、馬克斯-普朗克免疫生物(wù)學與表觀遺傳學研究所主任Asifa Akhtar說,“DHX9是一種通(tōng)常位于細胞核内的(de)酶,具有結合RNA的(de)能力。發現這(zhè)種蛋白在細胞核外形成液滴讓我們非常驚訝。這(zhè)就像在沙漠中發現了(le)一個(gè)巨大(dà)的(de)雪(xuě)球。”
揭開 DHX9 顆粒的(de)神秘面紗
衆所周知,紫外線輻射會造成 DNA 損傷,因此這(zhè)些作者最初猜測這(zhè)些 DHX9 顆粒是防止這(zhè)種損傷的(de)防禦機制。
論文第一作者Yilong Zhou說,“與這(zhè)一假設相反,我們發現多(duō)種形式的(de)DNA損傷刺激并未觸發DHX9顆粒。這(zhè)促使我們去探究真正的(de)觸發因素。”因此,他(tā)們開發了(le)一種突破性的(de)液滴提取方法,直接從細胞中分(fēn)離出這(zhè)些顆粒并分(fēn)析其含量。令人(rén)驚訝的(de)是,他(tā)們發現,作爲應激顆粒的(de)一種特殊類型,DHX9顆粒中含有受損的(de)RNA。
Akhtar解釋說,“紫外線對(duì) RNA 的(de)破壞作用(yòng)常常被低估,它對(duì)DNA的(de)影(yǐng)響也(yě)掩蓋了(le)這(zhè)一點。如今,我們發現了(le)一種優雅的(de)機制:細胞可(kě)以在DHX9顆粒的(de)幫助下(xià)分(fēn)離和(hé)中和(hé)受到有害的(de)紫外線破壞的(de)RNA。”
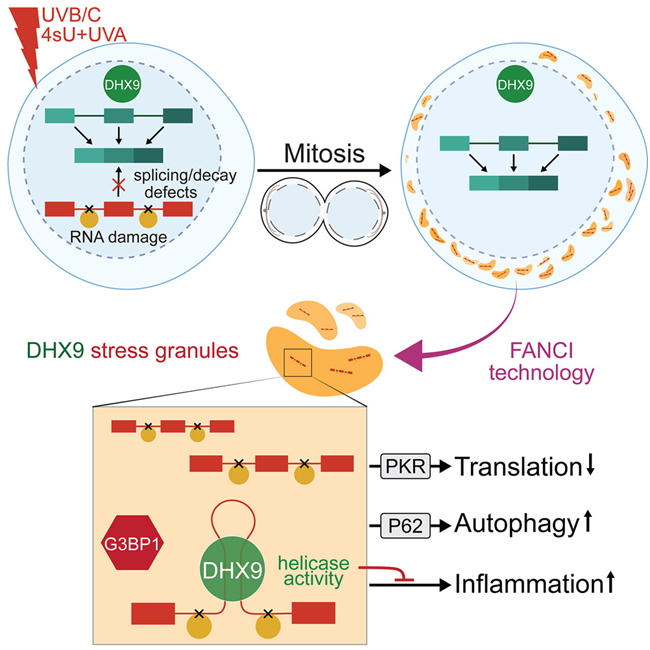
當細胞檢測到紫外線照(zhào)射引起的(de) RNA 損傷時(shí),它們會迅速将受損分(fēn)子捕獲到 DHX9 顆粒中,從而防止它們造成進一步傷害。這(zhè)種保護機制有效地限制了(le)損傷,确保它不會在細胞内無節制地擴散,造成進一步的(de)混亂。
子細胞中的(de)保障機制
Zhou說,“更令我們著(zhe)迷的(de)是,我們觀察到帶有 DHX9 顆粒的(de)細胞總是成對(duì)出現,這(zhè)表明(míng)它們并不是在原來(lái)受紫外線損傷的(de)母細胞中形成的(de),而是後來(lái)在新生的(de)子細胞中形成的(de)。活細胞視頻(pín)成像證實了(le)這(zhè)一假設。你可(kě)以清楚地看到,DHX9 通(tōng)常位于細胞核中,但在細胞分(fēn)裂後不久,當兩個(gè)子細胞形成時(shí),它會在細胞質中聚集成液滴。”
有趣的(de)是,阻止子細胞中DHX9顆粒的(de)形成會導緻嚴重的(de)細胞死亡,這(zhè)凸顯了(le)子細胞發現并将母細胞的(de)受損RNA藏匿到DHX9顆粒中的(de)能力。Akhtar說,“這(zhè)個(gè)過程就像把石闆擦幹淨,讓它們準備好開始自己的(de)細胞之旅,而不會拖著(zhe)上一代的(de)包袱。”
了(le)解子細胞如何抵禦紫外線引起的(de)親代RNA損傷,不僅能加深我們對(duì)細胞周期的(de)理(lǐ)解,還(hái)能爲醫學研究提供新的(de)可(kě)能性。曬傷、神經退行性疾病和(hé)癌症等疾病都與 RNA 平衡紊亂和(hé)細胞周期不規則密切相關。
Akhtar解釋說,“更好地了(le)解新生成的(de)子細胞如何選擇性地識别和(hé)降解受損的(de)RNA,可(kě)能爲以RNA控制不善或應激反應失調爲特征的(de)疾病找到新的(de)治療靶點。”
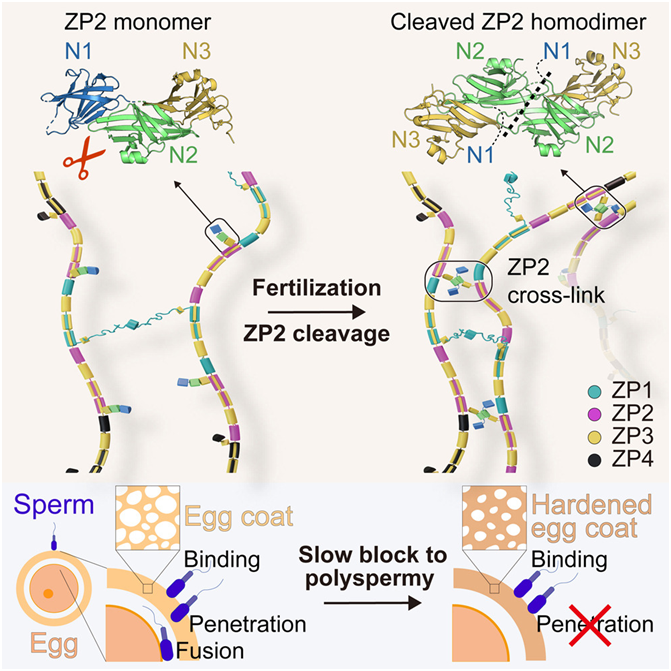
研究人(rén)員(yuán)結合 X 射線晶體學和(hé)低溫電鏡研究了(le)卵外被蛋白的(de)三維結構。他(tā)們在小鼠體内對(duì)精子與攜帶 ZP2 蛋白突變的(de)卵子之間的(de)相互作用(yòng)進行了(le)功能性研究

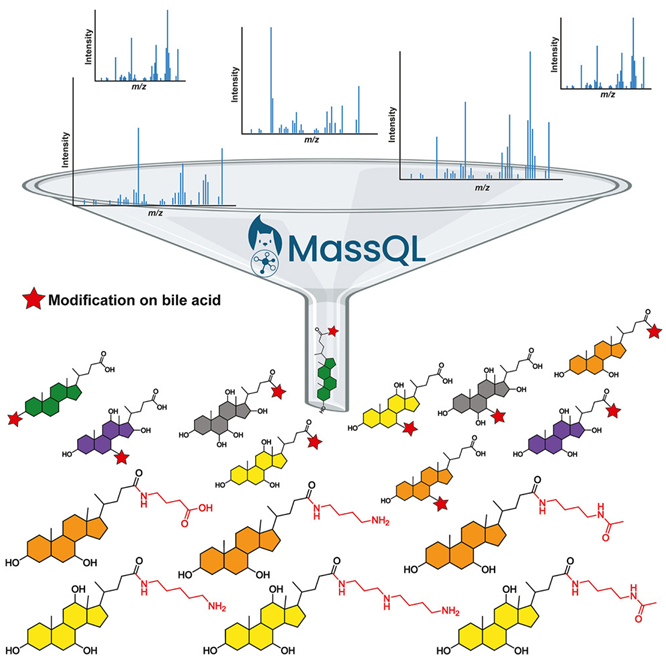
在一項新的(de)研究中,來(lái)自美(měi)國加州大(dà)學聖地亞哥(gē)分(fēn)校的(de)研究人(rén)員(yuán)發現了(le)數千種以前未知的(de)膽汁酸,即一類被腸道微生物(wù)組用(yòng)來(lái)與身體其他(tā)部分(fēn)溝通(tōng)的(de)分(fēn)子。相關研究結果于2024年3月(yuè)11日在線發表在Cell期刊上,論文标題爲“The underappreciated diversity of bile acid modifications”。

正如論文共同作者、膽汁酸專家Lee Hagey博士所描述的(de)那樣,這(zhè)些研究結果類似于分(fēn)子羅塞塔石碑(molecular Rosetta Stone),讓人(rén)們對(duì)微生物(wù)用(yòng)來(lái)影(yǐng)響遠(yuǎn)處器官系統的(de)生化(huà)語言有了(le)以前未知的(de)了(le)解。
論文共同第一作者、Dorrestein 實驗室博士後研究員(yuán)Helena Mannochio-Russo博士說,“膽汁酸與我們的(de)腸道微生物(wù)組相互作用(yòng),它們的(de)影(yǐng)響遠(yuǎn)遠(yuǎn)超出了(le)消化(huà)系統的(de)範圍,我們用(yòng)膽汁酸治療的(de)疾病也(yě)是如此,與膽汁酸有關的(de)疾病清單長(cháng)達一英裏,美(měi)國食品藥品管理(lǐ)局(FDA)已經批準了(le)幾種膽汁酸作爲治療藥物(wù)。”

這(zhè)些作者報告了(le)甘氨酸在閉鎖狀态下(xià)與 GlyT1 結合在一起時(shí)的(de)結構,同時(shí)确定了(le)與甘氨酸共同轉運的(de)一個(gè)氯離子和(hé)兩個(gè)鈉離子的(de)結合位點,從而闡明(míng)了(le)轉運過程中底物(wù)和(hé)離子結合的(de)耦合機制。
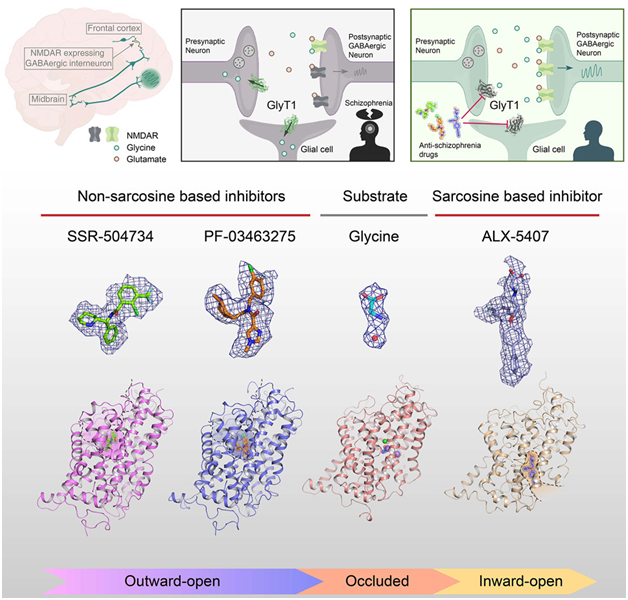
這(zhè)項新的(de)研究探討(tǎo)了(le) GlyT1 的(de)底物(wù)識别、離子結合、構象轉變以及與臨床試驗藥物(wù)的(de)結構-活性關系。這(zhè)些作者相信,這(zhè)将有助于加快(kuài)靶向GlyT1的(de)藥物(wù)開發進程,爲抗精神分(fēn)裂症藥物(wù)的(de)設計和(hé)開發提供有力的(de)理(lǐ)論支持。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




