科學家打造“混血大(dà)腦(nǎo)”,小鼠用(yòng)大(dà)鼠嗅覺探索世界
想象一下(xià),通(tōng)過另一物(wù)種的(de)眼睛看世界會是怎樣一番景象?如今,這(zhè)不再是科幻小說的(de)情節!
在一項新的(de)研究中,美(měi)國哥(gē)倫比亞大(dà)學Kristin Baldwin教授領導的(de)一個(gè)研究團隊成功構建了(le)擁有“混血大(dà)腦(nǎo)”的(de)小鼠,它們能利用(yòng)大(dà)鼠的(de)神經元來(lái)感知氣味。這(zhè)是動物(wù)首次能夠利用(yòng)另一種動物(wù)的(de)感覺器官來(lái)感知世界并做(zuò)出準确反應,同時(shí)也(yě)表明(míng)了(le)大(dà)腦(nǎo)在整合外部腦(nǎo)細胞方面的(de)靈活性。相關研究結果發表在2024年4月(yuè)25日的(de)Cell期刊上,論文标題爲“Functional sensory circuits built from neurons of two species”。

Baldwin說,“這(zhè)項研究開始向我們展示,我們如何擴大(dà)大(dà)腦(nǎo)的(de)靈活性,使其能夠容納來(lái)自人(rén)機界面或移植幹細胞的(de)其他(tā)類型輸入。”
雜(zá)合目标
了(le)解和(hé)治療人(rén)類大(dà)腦(nǎo)疾病的(de)最大(dà)挑戰之一是,目前的(de)研究方法不可(kě)能完全了(le)解這(zhè)些疾病。Baldwin說,“我們有漂亮的(de)培養皿細胞模型和(hé)稱爲類器官的(de)三維培養物(wù),它們都有各自的(de)優點,但單一的(de)它們都無法讓你确定細胞是否在最高(gāo)水(shuǐ)平上運作。”
雜(zá)合大(dà)腦(nǎo)将使得(de)人(rén)們更好地了(le)解腦(nǎo)細胞是如何生病或死亡的(de),并更好地了(le)解修複和(hé)替換部分(fēn)大(dà)腦(nǎo)的(de)規則。她補充說,“如今,科學家們正在将幹細胞和(hé)神經元移植到帕金森病和(hé)癫痫患者體内。但我們并不真正了(le)解這(zhè)樣做(zuò)的(de)效果如何。有了(le)雜(zá)合大(dà)腦(nǎo)模型,我們就能開始得(de)到一些答(dá)案,而且速度比臨床試驗更快(kuài)。”
構建雜(zá)合大(dà)腦(nǎo)
人(rén)們以前曾通(tōng)過注射神經元或移植豌豆大(dà)小的(de)腦(nǎo)類器官到小鼠或大(dà)鼠發育中的(de)大(dà)腦(nǎo)或完全成型的(de)大(dà)腦(nǎo)中來(lái)構建雜(zá)合大(dà)腦(nǎo)。
研究團隊采用(yòng)了(le)前沿的(de)“囊胚互補”技術,将大(dà)鼠幹細胞注入小鼠早期胚胎中,使兩種物(wù)種的(de)細胞得(de)以共生并自然整合,克服了(le)傳統移植技術的(de)局限性。這(zhè)一過程如同在小鼠大(dà)腦(nǎo)中巧妙植入了(le)大(dà)鼠的(de)嗅覺系統,使改造後的(de)小鼠能夠依靠“外來(lái)”神經元找到隐藏的(de)食物(wù),證明(míng)了(le)大(dà)鼠神經元在小鼠大(dà)腦(nǎo)中的(de)功能整合。
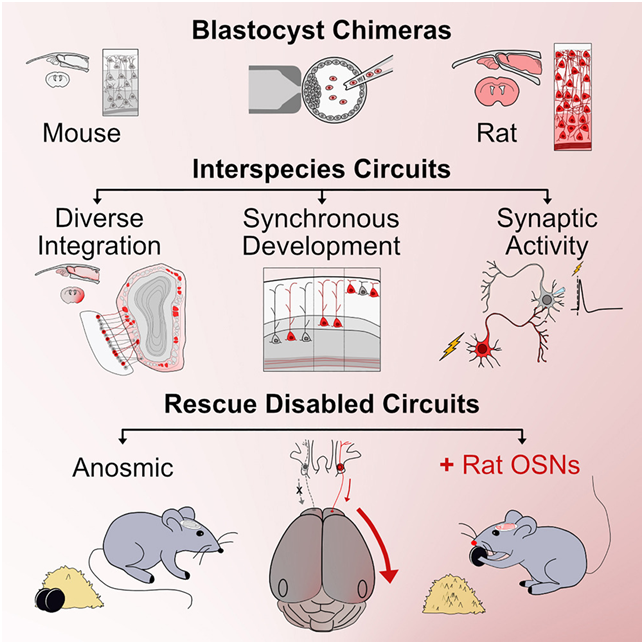
這(zhè)種稱爲囊胚互補(blastocyst complementation)的(de)技術類似于制造具有人(rén)類免疫系統的(de)小鼠的(de)技術,後者已被證實是強大(dà)的(de)研究工具。但在這(zhè)項研究之前,這(zhè)種技術還(hái)不能成功地制造出兩個(gè)不同物(wù)種的(de)雜(zá)合大(dà)腦(nǎo)。Baldwin說,“我們正在做(zuò)的(de)是真正的(de)前沿技術。”
大(dà)鼠神經元恢複了(le)小鼠的(de)嗅覺
在這(zhè)些作者的(de)首次雜(zá)合實驗中,他(tā)們研究了(le)小鼠大(dà)腦(nǎo)中出現大(dà)鼠神經元的(de)位置。大(dà)鼠的(de)發育速度較慢(màn),大(dà)腦(nǎo)較大(dà),但在小鼠體内,大(dà)鼠細胞遵循小鼠的(de)指示,加速發育,并建立與小鼠細胞相同的(de)連接。
Baldwin說,“你幾乎可(kě)以在整個(gè)小鼠大(dà)腦(nǎo)中看到大(dà)鼠細胞,這(zhè)讓我們相當驚訝。這(zhè)告訴我們,将它們插入的(de)障礙很少,這(zhè)表明(míng)許多(duō)種小鼠神經元都可(kě)以被類似的(de)大(dà)鼠神經元取代。”
這(zhè)些作者随後研究了(le)大(dà)鼠神經元是否被整合到了(le)一種功能神經回路中,在這(zhè)種情況下(xià),大(dà)鼠神經元被整合到了(le)嗅覺系統的(de)一部分(fēn),而嗅覺系統對(duì)于小鼠尋找食物(wù)和(hé)躲避捕食者至關重要。通(tōng)過對(duì)小鼠胚胎進行工程改造,使其自身的(de)嗅覺神經元死亡或失活,他(tā)們就能輕松确定大(dà)鼠神經元是否恢複了(le)它們的(de)嗅覺。
Baldwin說,“”我們在每隻小鼠的(de)籠子裏都藏了(le)一塊餅幹,我們非常驚訝地發現,它們能用(yòng)大(dà)鼠神經元找到餅幹。”
不過,有些小鼠比其他(tā)小鼠更善于尋找餅幹。研究人(rén)員(yuán)發現,與嗅覺神經元在發育過程中經過基因改造後消失的(de)小鼠相比,保留了(le)自己的(de)、沉默的(de)嗅覺神經元的(de)小鼠在尋找隐藏的(de)餅幹時(shí)成功率較低。
Baldwin,“這(zhè)表明(míng)添加替代性神經元并非即插即用(yòng)。如果你想獲得(de)功能性替代神經元,你可(kě)能需要清空呆在那裏的(de)功能障礙神經元,這(zhè)可(kě)能是某些神經退行性疾病的(de)情況,也(yě)可(kě)能是自閉症和(hé)精神分(fēn)裂症等神經發育障礙的(de)情況。”
有了(le)Baldwin團隊構建的(de)這(zhè)種雜(zá)合大(dà)腦(nǎo)系統,科學家們如今可(kě)以利用(yòng)小鼠仔細剖析不同模型中發生的(de)情況,這(zhè)最終可(kě)能有助于提高(gāo)人(rén)類細胞移植的(de)成功率。
靈長(cháng)類動物(wù)雜(zá)合體?
這(zhè)種新的(de)雜(zá)合大(dà)腦(nǎo)系統的(de)一個(gè)缺點是,大(dà)鼠細胞在每隻不同小鼠體内的(de)分(fēn)布是随機的(de),這(zhè)阻礙了(le)将這(zhè)些研究推廣到大(dà)腦(nǎo)的(de)其他(tā)感覺和(hé)神經系統。Baldwin實驗室目前正在努力尋找方法,促使導入的(de)細胞隻發育成一種細胞類型,這(zhè)樣就可(kě)以進行更精确的(de)實驗。
如果導入的(de)細胞在雜(zá)合大(dà)腦(nǎo)中的(de)發育能夠受到限制,那麽這(zhè)也(yě)将爲構建具有靈長(cháng)類動物(wù)神經元的(de)雜(zá)合大(dà)腦(nǎo)打開大(dà)門。Baldwin,“這(zhè)将幫助我們更了(le)解人(rén)類疾病。”
人(rén)類腸道菌群中的(de)隐性質粒有望成爲識别水(shuǐ)體糞便污染、炎症性腸病等健康問題的(de)強大(dà)生物(wù)标志物(wù)
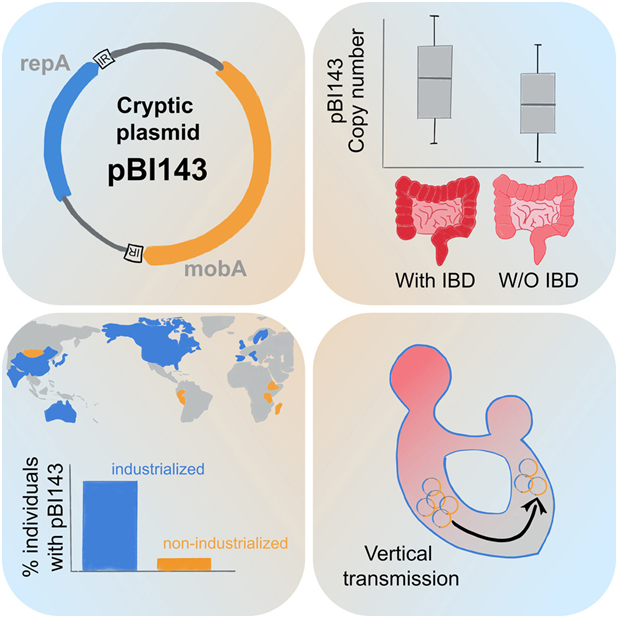
研究人(rén)員(yuán)發現,在工業化(huà)國家,90% 以上的(de)人(rén)都攜帶這(zhè)種隐性質粒,平均而言,它是人(rén)類腸道中數量最多(duō)的(de)基因實體之一。在一項新的(de)研究中,德國奧爾登堡大(dà)學亥姆霍茲海洋生物(wù)功能多(duō)樣性研究所的(de)A. Murat Eren教授領導的(de)一個(gè)國際研究小組聚焦于人(rén)類腸道菌群中的(de)一種成分(fēn):質粒,在此之前人(rén)們對(duì)它的(de)研究很少。質粒是一種小型染色體外遺傳元件,廣泛存在于細菌細胞中,對(duì)微生物(wù)生活方式具有深遠(yuǎn)影(yǐng)響,但其在自然生态環境中的(de)多(duō)樣性卻知之甚少。在這(zhè)項新的(de)研究中,他(tā)們發現一種神秘的(de)質粒是人(rén)類腸道中數量最多(duō)的(de)遺傳因子之一。這(zhè)種質粒有可(kě)能成爲一種強大(dà)的(de)生物(wù)标志物(wù),用(yòng)于識别水(shuǐ)的(de)糞便污染等健康危害或炎症性腸病等人(rén)類疾病。根據他(tā)們的(de)分(fēn)析,這(zhè)種質粒存在于工業化(huà)國家 90% 以上的(de)人(rén)的(de)腸道中。相關研究結果近期發表在Cell期刊上,論文标題爲“A cryptic plasmid is among the most numerous genetic elements in the human gut”。

質粒是染色體外的(de)DNA序列,在所有生命領域的(de)細胞中都很常見。Eren将其描述爲“攜帶額外基因的(de)典型小型遺傳實體”。它們可(kě)以在不同的(de)細菌細胞之間甚至不同類型的(de)細菌之間交換。質粒的(de)複制依賴于宿主細胞,但在某些情況下(xià),它們爲宿主提供了(le)極其重要的(de)适應性決定因素,從而彌補了(le)宿主細胞的(de)不足。例如,有些質粒含有編碼抗生素耐藥性的(de)基因,助力細菌在抗生素環境中生存,成爲全球公共衛生的(de)重大(dà)挑戰之一。
根據迄今爲止的(de)研究,還(hái)有一些質粒并不含有編碼對(duì)宿主明(míng)顯有益功能的(de)基因。Eren解釋說,“這(zhè)些所謂的(de)‘隐性質粒(cryptic plasmid)’通(tōng)常被稱爲基因寄生蟲。它們仍然是微生物(wù)生态學中的(de)一個(gè)謎,因爲從進化(huà)的(de)角度來(lái)看,它們根本就不應該存在。”迄今爲止,識别質粒一直是一項艱巨的(de)任務。一段時(shí)間以來(lái),科學家們已能夠直接從環境樣本中提取遺傳物(wù)質,例如,無需培養單個(gè)細菌生物(wù),就能對(duì)人(rén)類腸道中的(de)微生物(wù)群落進行整體分(fēn)析。然而,在這(zhè)些稱爲“宏基因組(metagenome)”的(de)遺傳物(wù)質集合體中,如何有把握地分(fēn)辨出什(shén)麽是質粒仍是一個(gè)相當大(dà)的(de)挑戰。爲了(le)解決這(zhè)個(gè)問題,Eren和(hé)他(tā)的(de)同事們開發了(le)一種新的(de)機器學習(xí)方法。他(tā)們近期發表在Nature Microbiology期刊上的(de)另一篇論文中報告說,他(tā)們利用(yòng)這(zhè)種方法識别出了(le)人(rén)類腸道菌群中的(de)68000多(duō)個(gè)質粒,其中一種名爲pBI143的(de)隐性質粒在數據集中尤爲豐富(Nature Microbiology, 2024, doi:10.1038/s41564-024-01610-3)。在這(zhè)項新的(de)研究中,他(tā)們仔細研究了(le)這(zhè)種隐性質粒,它隻由兩個(gè)基因組成,令人(rén)驚訝的(de)是,這(zhè)兩個(gè)基因隻能用(yòng)于自身複制和(hé)在細菌細胞中移動,而沒有其他(tā)明(míng)顯的(de)益處。爲了(le)更好地了(le)解 pBI143 的(de)生态學,他(tā)們分(fēn)析了(le)從不同栖息地産生的(de) 6 萬個(gè)人(rén)類宏基因組和(hé) 4 萬個(gè)環境宏基因組。Eren解釋說,“我們發現 pBI143 有一系列非常有趣的(de)特征。”他(tā)們發現,在工業化(huà)國家,90% 以上的(de)人(rén)都攜帶這(zhè)種隐性質粒,平均而言,它是人(rén)類腸道中數量最多(duō)的(de)基因實體之一。他(tā)說,“平均而言,它的(de)數量是病毒基因組的(de) 10 倍以上,而病毒基因組以前被認爲是人(rén)類腸道中數量最多(duō)的(de)染色體外遺傳物(wù)質。”進一步的(de)分(fēn)析表明(míng),這(zhè)種隐性質粒幾乎隻出現在人(rén)類腸道中,但在海洋、土壤、植物(wù)和(hé)動物(wù)消化(huà)器官及其糞便等其他(tā)環境的(de)數據集中幾乎不存在。除受人(rén)類活動影(yǐng)響的(de)環境如廢水(shuǐ)、醫院表面和(hé)實驗室大(dà)鼠樣本外,研究人(rén)員(yuán)僅能在極少數樣本中檢測到其特征基因序列。由于pBI143的(de)數量龐大(dà),在人(rén)類中普遍存在,而且在人(rén)類種群中具有保守性,這(zhè)些作者假設,pBI143可(kě)以用(yòng)作檢測糞便污染的(de)生物(wù)标志物(wù)。Eren教授肯定道:“事實證明(míng),相較于基于人(rén)類腸道細菌特定基因序列的(de)先進生物(wù)标志物(wù),pBI143在檢測飲用(yòng)水(shuǐ)中糞便污染方面更爲靈敏。”此外,研究者還(hái)揭示了(le)這(zhè)種普遍存在的(de)基因實體在炎症性腸病(IBD)等人(rén)類疾病中的(de)潛在應用(yòng)價值。他(tā)們發現,與健康人(rén)相比,IBD患者腸道中pBI143的(de)相對(duì)拷貝數近乎翻了(le)四倍,暗示質粒拷貝數的(de)變化(huà)可(kě)能作爲量化(huà)疾病進展或嚴重程度的(de)非侵入性指标。Eren團隊正在計算(suàn)機科學和(hé)微生物(wù)學的(de)交叉領域開發新的(de)工具,以識别和(hé)描述生活在海洋中的(de)細菌中天然存在的(de)質粒和(hé)其他(tā)可(kě)移動遺傳元件。他(tā)們緻力于更好地了(le)解微生物(wù)的(de)生态學和(hé)進化(huà),揭示微生物(wù)應對(duì)環境變化(huà)的(de)策略,從而實現新的(de)生物(wù)技術應用(yòng),改善我們面臨的(de)危機。
利用(yòng)新開發的(de)顯微鏡技術FLASH-PAINT觀察複雜(zá)的(de)細胞内部運作
來(lái)自美(měi)國耶魯大(dà)學的(de)研究人(rén)員(yuán)開發了(le)一種革命性的(de)顯微鏡技術——“FLASH-PAINT”,它爲我們揭開單個(gè)細胞内部運作的(de)神秘面紗提供了(le)前所未有的(de)視角。試想觀看一場(chǎng)橄榄球賽,除了(le)兩名四分(fēn)衛,其餘球員(yuán)皆隐身不見,如此一來(lái),觀衆将難以理(lǐ)解全隊的(de)協同戰術。同樣,科學家在顯微鏡下(xià)探索細胞内部世界時(shí),也(yě)面臨著(zhe)類似困境。細胞内部是一個(gè)由數百萬分(fēn)子構成的(de)精密生态系統,它們相互作用(yòng)、協同工作,而要清晰觀察細胞器、蛋白質及其他(tā)微小亞細胞成分(fēn),必須依賴超分(fēn)辨率顯微鏡。遺憾的(de)是,當前技術僅能讓我們同時(shí)觀察有限的(de)目标。在一項新的(de)研究中,來(lái)自美(měi)國耶魯大(dà)學的(de)研究人(rén)員(yuán)開發了(le)一種革命性的(de)顯微鏡技術——“FLASH-PAINT”,它爲我們揭開單個(gè)細胞内部運作的(de)神秘面紗提供了(le)前所未有的(de)視角。這(zhè)項技術的(de)核心在于對(duì)成像探針的(de)創新應用(yòng),通(tōng)過在生物(wù)樣本中使用(yòng)特定化(huà)合物(wù),顯著提升科學家對(duì)微小細節的(de)探測能力。相關研究結果發表在2024年3月(yuè)28日的(de)Cell期刊上,論文标題爲“Unraveling cellular complexity with transient adapters in highly multiplexed super-resolution imaging”。
論文共同通(tōng)訊作者、耶魯大(dà)學細胞生物(wù)學教授Joerg Bewersdorf博士說,“若僅能觀察一兩蛋白,就如同管窺蠡測,難以洞察全局。而今,我們擁有一種優雅且高(gāo)效的(de)手段,可(kě)以随心所欲地對(duì)幾乎無限數量的(de)蛋白質和(hé)其他(tā)特征進行成像。”
新型成像探針能瞬時(shí)結合無限數量的(de)分(fēn)子
目前一種可(kě)視化(huà)觀察細胞内部過程的(de)方法是将抗體與由單鏈 DNA 和(hé)熒光(guāng)染料組成的(de)成像探針結合使用(yòng)。抗體引導探針到達需要成像的(de)靶标,DNA 鏈與抗體上的(de)互補“對(duì)接”DNA 鏈結合。
這(zhè)種方法的(de)一個(gè)局限是,每個(gè)靶标都需要它自己的(de)成像探針。例如,如果一個(gè)團隊想觀察 10 種不同的(de)靶标,就需要使用(yòng) 10 種探針。論文第一作者、耶魯大(dà)學細胞生物(wù)學副研究員(yuán)Florian Schüder 博士說,“但是如果我們的(de)設想是對(duì)細胞中的(de)每種蛋白進行成像,那麽大(dà)約有 2 萬種不同的(de)蛋白。”他(tā)說,“設想對(duì)細胞内所有2萬餘種蛋白質進行成像,現有技術顯然無法勝任。”
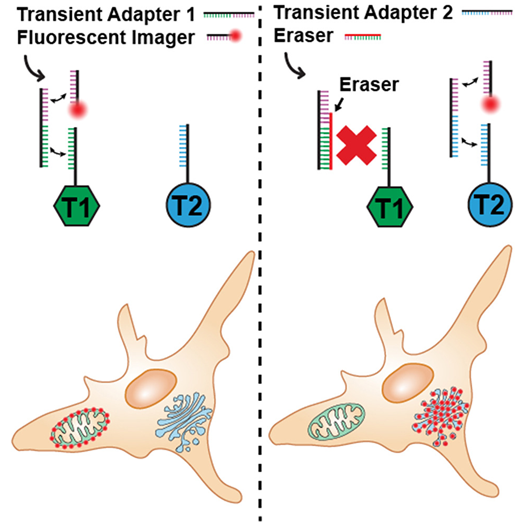
爲解決這(zhè)一難題,研究團隊引入了(le)一種名爲“銜接分(fēn)子”(adapter)的(de)中介物(wù)質,它能靈活連接任意類型的(de)探針與任意類型的(de)靶标。這(zhè)項技術的(de)關鍵在于,銜接分(fēn)子與靶标的(de)結合極爲短暫,易于從一個(gè)靶标迅速轉換至下(xià)一個(gè)。“這(zhè)種快(kuài)速切換能力至關重要,”Bewersdorf強調。
快(kuài)速、低成本的(de)顯微鏡技術爲新發現鋪平了(le)道路
“瞬時(shí)結合”與“廣泛連接”的(de)特性使得(de)FLASH-PAINT技術的(de)速度提升百倍,且成本僅爲現行超分(fēn)辨率顯微鏡技術的(de)極小部分(fēn)。“這(zhè)将極大(dà)地加速科學發現的(de)步伐,”Bewersdorf說,“現在,我們隻需一次實驗就能揭示所有可(kě)能的(de)相互作用(yòng),而非反複實驗隻爲觀察一兩種蛋白間的(de)單一交互。”
研究團隊期待FLASH-PAINT能讓我們直觀呈現以往無法觸及的(de)複雜(zá)亞細胞過程,從而助力臨床醫生更好地理(lǐ)解并治療包括癌症在内的(de)多(duō)種疾病。“與疾病較量需要全面審視所有參與者,唯有如此,方能洞悉全局,”Bewersdorf表示。在未來(lái)的(de)探索中,研究人(rén)員(yuán)将進一步研究FLASH-PAINT在組織成像及作爲診斷工具的(de)應用(yòng)潛力,這(zhè)場(chǎng)細胞内部世界的(de)“高(gāo)清直播”正緩緩拉開帷幕,引領我們步入生命科學的(de)新紀元。
新研究發現DNA複制的(de)一種關鍵質量控制機制
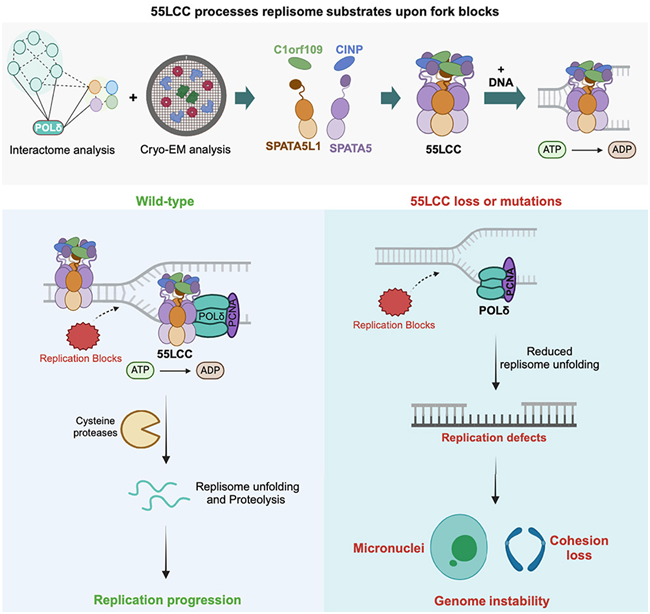
在這(zhè)項新的(de)研究中,研究人(rén)員(yuán)利用(yòng)低溫電鏡、基于CRISPR的(de)突變分(fēn)析和(hé)其他(tā)先進技術,确定了(le)一種蛋白複合物(wù),這(zhè)種複合物(wù)在滞後鏈的(de)複制停止過程中發揮著(zhe)核心作用(yòng)。人(rén)體細胞分(fēn)裂時(shí),必須首先準确複制它的(de)DNA。DNA 複制工作是所有生物(wù)體内最重要的(de)過程之一,充滿了(le)突變的(de)風險,可(kě)能導緻細胞死亡或癌症。如今,在一項新的(de)研究中,來(lái)自美(měi)國賓夕法尼亞大(dà)學佩雷爾曼醫學院和(hé)英國利茲大(dà)學的(de)研究人(rén)員(yuán)發現了(le)細胞中的(de)一種多(duō)蛋白“機器”,它能幫助控制 DNA 複制的(de)暫停或停止,以确保DNA複制的(de)順利進行。這(zhè)一發現加深了(le)人(rén)們對(duì)DNA複制的(de)理(lǐ)解,有助于解釋一系列令人(rén)費解的(de)遺傳疾病,并可(kě)能爲未來(lái)開發針對(duì)神經和(hé)發育疾病的(de)治療方法提供信息。相關研究結果于2024年3月(yuè)29日在線發表在Cell期刊上,論文标題爲“The SPATA5-SPATA5L1 ATPase complex directs replisome proteostasis to ensure genome integrity”。
論文共同通(tōng)訊作者、賓夕法尼亞大(dà)學佩雷爾曼醫學院癌症生物(wù)學系教授Roger Greenberg 博士說,“我們發現了(le)細胞中的(de)一種關鍵質量控制機制。我們體内每天都有數萬億個(gè)細胞進行分(fēn)裂,這(zhè)就需要準确複制我們的(de)基因組。我們的(de)研究描述了(le)一種調節複制 DNA 中蛋白穩定性的(de)新機制。我們如今對(duì)這(zhè)一複雜(zá)生物(wù)過程中的(de)一個(gè)重要步驟有了(le)更多(duō)的(de)了(le)解。”DNA“滞後鏈(lagging strand)”複制的(de)不解之謎
DNA 複制過程由多(duō)種具有高(gāo)度專業化(huà)功能的(de)蛋白複合物(wù)完成,包括 DNA 的(de)解旋和(hé)兩條解旋的(de)DNA 鏈的(de)複制。這(zhè)個(gè)過程類似于工廠的(de)裝配線,由大(dà)量摺皺的(de)數據線組成的(de)球被解開,允許特定的(de)片段被修剪和(hé)複制。生物(wù)學家對(duì)這(zhè)一過程如何開始和(hé)進行了(le)解頗多(duō),但對(duì)其如何停止或暫停卻知之甚少。
先前的(de)研究已确定了(le)一些蛋白,它們通(tōng)過誘導 DNA 複制組分(fēn)在一條 DNA 鏈——前導鏈(leading strand)上的(de)分(fēn)解和(hé)再循環,來(lái)阻止該鏈上的(de)複制。另一條DNA鏈——滞後鏈上的(de)DNA複制是如何停止的(de),一直是個(gè)謎。在這(zhè)項新的(de)研究中,這(zhè)些作者利用(yòng)低溫電鏡、基于CRISPR的(de)突變分(fēn)析和(hé)其他(tā)先進技術,确定了(le)一種蛋白複合物(wù),這(zhè)種複合物(wù)在滞後鏈的(de)複制停止過程中發揮著(zhe)核心作用(yòng)。他(tā)們發現這(zhè)種稱爲 55LCC 的(de)四蛋白機器能與 DNA 及其相關的(de)複制複合物(wù)結合。在兩種稱爲 ATP 酶的(de)馬達樣酶(motor-like enzyme)的(de)驅動下(xià),55LCC 似乎能讓原本緊密折疊的(de)複制複合物(wù)去折疊,使其被蛋白切割酶切碎并清除。這(zhè)些實驗表明(míng),55LCC 的(de)這(zhè)種停止或暫停功能對(duì)于 DNA 複制的(de)順利進行至關重要。這(zhè)些作者發現當55LCC缺失時(shí),DNA複制很可(kě)能會被卡住,受影(yǐng)響的(de)細胞會停止分(fēn)裂。Greenberg說,“我們最終看到這(zhè)些細胞的(de)基因組穩定性發生了(le)巨大(dà)變化(huà),因爲它們的(de)染色體在細胞分(fēn)裂過程中無法正常分(fēn)離。”這(zhè)些作者猜測55LCC不僅可(kě)能參與調節與細胞分(fēn)裂相關的(de)DNA複制過程,還(hái)可(kě)能在DNA損傷性病變阻斷DNA複制時(shí)也(yě)是如此。基礎科學發現的(de)臨床意義
衆所周知,構成55LCC的(de)酶的(de)遺傳突變與兒(ér)童綜合症有關,包括聽(tīng)力損失、認知和(hé)運動障礙以及癫痫。這(zhè)些作者在實驗中發現,這(zhè)些緻病突變往往會降低55LCC的(de)結構穩定性或影(yǐng)響它與其他(tā)蛋白的(de)相互作用(yòng)。
Greenberg說,“這(zhè)項研究有望标志著(zhe)人(rén)們開始更深入地了(le)解這(zhè)些嚴重的(de)神經發育綜合征。最終,這(zhè)一發現的(de)影(yǐng)響可(kě)能會更廣泛。它可(kě)能導緻人(rén)們找到緩解與包括癫痫、聽(tīng)力損失、智力遲鈍和(hé)骨髓功能不全在内的(de)55LCC功能障礙綜合征相關的(de)臨床問題的(de)方法。”
55LCC還(hái)可(kě)能成爲蛋白循環利用(yòng)的(de)一種更普遍的(de)工具,其中蛋白循環利用(yòng)是對(duì)細胞健康至關重要的(de)另一個(gè)過程。Greenberg和(hé)他(tā)的(de)團隊正在繼續研究 55LCC 的(de)作用(yòng)機制和(hé)調控方式,包括了(le)解讓55LCC 變得(de)活躍并開始讓DNA 複制複合物(wù)去折疊的(de)精确信号。
返回列表










 京公網安備 11011402010692号
京公網安備 11011402010692号




