新的(de)圖譜針對(duì)基因如何在早期胚胎發育中起作用(yòng)提供新見解
研究人(rén)員(yuán)開發了(le)一種自動系統,用(yòng)于分(fēn)析胚胎發生所需的(de)基因功能,其中胚胎發生是受精卵從單細胞發育成具有皮膚、消化(huà)道、神經元和(hé)肌肉等不同組織的(de)有機體的(de)過程。
盡管人(rén)類基因組計劃早在 20 多(duō)年前就宣布完成了(le) 2 萬個(gè)人(rén)類基因的(de)測序工作,但科學家們仍在努力掌握基本遺傳指令如何産生完整的(de)有機體。
研究疾病如何在發育的(de)早期階段形成的(de)生物(wù)醫學工作,将受益于具體了(le)解複雜(zá)生物(wù)是如何從單個(gè)受精卵細胞中産生的(de)。在一項新的(de)研究中,來(lái)自加州大(dà)學聖地亞哥(gē)分(fēn)校的(de)研究人(rén)員(yuán)通(tōng)過一種簡單的(de)模式生物(wù),對(duì)胚胎發育如何展開有了(le)新的(de)認識。相關研究結果于2024年5月(yuè)16日在線發表在Cell期刊上,論文标題爲“Automated profiling of gene function during embryonic development”。

這(zhè)些作者逐一介紹了(le)秀麗隐杆線蟲(Caenorhabditis elegans)胚胎發育過程中基因是如何發揮作用(yòng)的(de)。盡管體型微小,秀麗隐杆線蟲一直是科學家們的(de)研究對(duì)象,因爲它的(de)許多(duō)生物(wù)學特性,包括早期發育階段,都與包括人(rén)類在内的(de)高(gāo)等生物(wù)非常相似。
論文第一作者Rebecca Green說,“通(tōng)過在一種簡單的(de)模式生物(wù)中描述許多(duō)這(zhè)些鮮爲人(rén)知的(de)基因,我們可(kě)以了(le)解它們在像人(rén)類這(zhè)樣更複雜(zá)的(de)系統中的(de)作用(yòng)。雖然這(zhè)項研究是利用(yòng)秀麗隐杆線蟲完成的(de),但所分(fēn)析的(de)大(dà)多(duō)數基因都存在于人(rén)類中,其中許多(duō)基因的(de)突變與人(rén)類發育障礙有關。”
這(zhè)些作者開發了(le)一種自動系統,用(yòng)于分(fēn)析胚胎發生所需的(de)基因功能,其中胚胎發生是受精卵從單細胞發育成具有皮膚、消化(huà)道、神經元和(hé)肌肉等不同組織的(de)有機體的(de)過程。他(tā)們利用(yòng)延時(shí) 4D 成像技術有條不紊地跟蹤了(le)每個(gè)基因在胚胎各個(gè)階段的(de)功能,包括細胞身份确定和(hé)有機體組織成形的(de)時(shí)間。
他(tā)們使用(yòng)一種稱爲“計算(suàn)機視覺(computer vision)”的(de)方法監控這(zhè)一過程,以跟蹤發育的(de)特定方面,包括每個(gè)組織中的(de)細胞數量。他(tā)們還(hái)跟蹤了(le)發育中有機體内組織的(de)質量、位置和(hé)形狀。
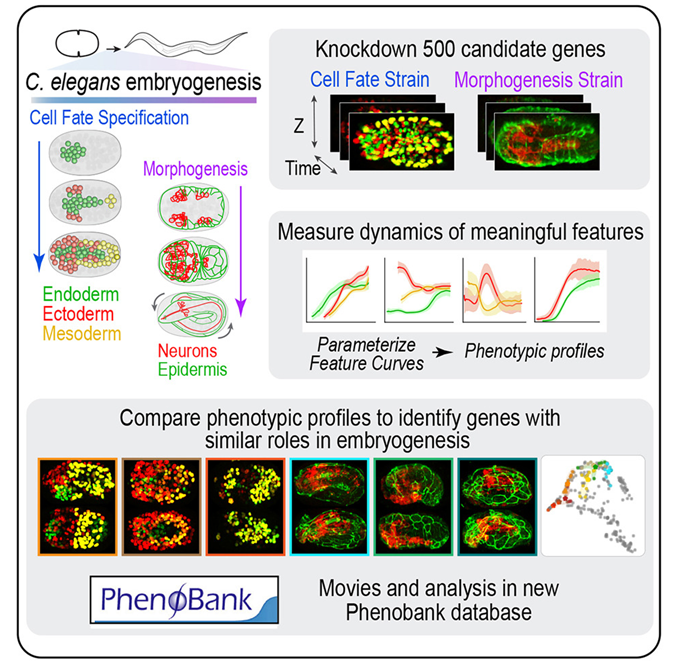
爲了(le)充分(fēn)了(le)解近 500 個(gè)對(duì)胚胎發育非常重要的(de)基因的(de)功能,他(tā)們逐一阻斷了(le)每個(gè)基因的(de)功能。這(zhè)樣,這(zhè)些作者就能将基因歸入共同的(de)基因簇,從而揭示每個(gè)基因的(de)作用(yòng)。Green将這(zhè)一過程比作自動面部識别,在這(zhè)一過程中,具有相似特征的(de)圖像會被組合在一起。
通(tōng)過使用(yòng)這(zhè)個(gè)細緻的(de)過程來(lái)分(fēn)析近7000個(gè)4D胚胎發生影(yǐng)片集,他(tā)們能夠爲單個(gè)基因創建 “指紋”,如細胞成爲肌肉或皮膚所需的(de)基因。這(zhè)有助于他(tā)們了(le)解這(zhè)些基因在胚胎發生過程中發揮的(de)生理(lǐ)作用(yòng),如控制腸道或神經系統等組織的(de)形成。
Karen Oegema說,“我們的(de)研究表明(míng),我們的(de)方法正确地對(duì)以前表征過的(de)基因的(de)功能進行了(le)分(fēn)類,确定了(le)未被表征的(de)基因的(de)功能,并描述了(le)新的(de)基因和(hé)通(tōng)路關系。很多(duō)我們認爲功能平凡的(de)基因被發現具有被低估的(de)重要作用(yòng)。”
來(lái)自這(zhè)項研究的(de)大(dà)量數據也(yě)促成了(le)一個(gè)新的(de)在線資源的(de)推出,其中包含了(le)所有的(de)信息。PhenoBank如今提供了(le)一個(gè)門戶網站,可(kě)以訪問這(zhè)項研究期間開發的(de)基因圖譜。
Arshad Desai教授說,“這(zhè)種方法令人(rén)驚奇地揭示了(le)胚胎發生過程中代謝途徑是如何專門化(huà)的(de),并揭示了(le)參與基因調控的(de)不同分(fēn)子機器之間有趣的(de)新聯系。”
除了(le)這(zhè)項研究中涉及的(de) 500 個(gè)基因外,這(zhè)些作者目前正在努力完成與胚胎發生有關的(de)全部 2000 個(gè)秀麗隐杆線蟲基因的(de)研究。
他(tā)說,“研究人(rén)員(yuán)的(de)廣泛興趣在于他(tā)們所開發的(de)解決生物(wù)學中最具挑戰性問題的(de)方法:一個(gè)擁有大(dà)約20000個(gè)基因(與人(rén)類基因的(de)數量相似)的(de)基因組的(de)單個(gè)細胞如何能夠構建一個(gè)完整的(de)有機體。”
胎兒(ér)細胞可(kě)以追溯到人(rén)類胚胎發育的(de)第一天
這(zhè)項研究改變了(le)人(rén)們長(cháng)期以來(lái)的(de)看法,即這(zhè)兩個(gè)細胞在這(zhè)一階段對(duì)發育中胚胎的(de)所有部分(fēn)都有同樣的(de)貢獻,這(zhè)表明(míng)“特化(huà)”——細胞具有特定個(gè)體作用(yòng)的(de)現象,在發育過程中比以前認爲的(de)要早得(de)多(duō)。
雖然已有 800 多(duō)萬嬰兒(ér)通(tōng)過體外受精(IVF)出生,但 70% 的(de)體外受精植入失敗。随著(zhe)體外受精成爲不孕症患者更常見的(de)懷孕途徑,人(rén)們需要更好地了(le)解胚胎在這(zhè)一早期階段的(de)發育情況。在一項新的(de)研究中,加州理(lǐ)工學院生物(wù)學與生物(wù)工程學的(de)Magdalena Zernicka-Goetz教授 Magdalena Zernicka-Goetz及其團隊研究了(le)人(rén)類早期發育的(de)基本生物(wù)過程。他(tā)們發現在胚胎剛出生 1 天時(shí),人(rén)類胚胎由兩個(gè)細胞組成,其中一個(gè)細胞除了(le)産生胎盤細胞外,還(hái)會産生大(dà)部分(fēn)胎兒(ér)體細胞,而另一個(gè)細胞隻會産生胎盤細胞。相關研究結果發表在2024年5月(yuè)23日的(de)Cell期刊上,論文标題爲“The first two blastomeres contribute unequally to the human embryo”。
這(zhè)項研究改變了(le)人(rén)們長(cháng)期以來(lái)的(de)看法,即這(zhè)兩個(gè)細胞在這(zhè)一階段對(duì)發育中胚胎的(de)所有部分(fēn)都有同樣的(de)貢獻,這(zhè)表明(míng)“特化(huà)(specification)”——細胞具有特定個(gè)體作用(yòng)的(de)現象,在發育過程中比以前認爲的(de)要早得(de)多(duō)。這(zhè)些發現對(duì)如何評估準備用(yòng)于試管嬰兒(ér)植入的(de)胚胎是否存在異常具有重要意義。
Zernicka-Goetz說,“在試管嬰兒(ér)診所,通(tōng)常會從6天大(dà)的(de)胚胎外部選取一些胎盤細胞進行基因診斷,以确定它們是否存在染色體異常。我們的(de)研究結果表明(míng),根據推斷,這(zhè)些被選中的(de)外部細胞不太可(kě)能對(duì)胎兒(ér)的(de)身體做(zuò)出貢獻。來(lái)自這(zhè)些細胞的(de)遺傳信息可(kě)能不如對(duì)胎兒(ér)細胞本身取樣那麽有意義。”1天大(dà)的(de)人(rén)類胚胎僅由兩個(gè)細胞組成,每個(gè)細胞稱爲一個(gè)卵裂球(blastomere)。這(zhè)些作者利用(yòng)試管嬰兒(ér)診所捐贈用(yòng)于研究的(de)胚胎,用(yòng)彩色染料标記卵裂球,然後使用(yòng)延時(shí)成像技術觀察這(zhè)兩個(gè)細胞在六天内的(de)分(fēn)裂過程。新細胞帶有與其母細胞相同顔色的(de)染料。通(tōng)過這(zhè)一過程,他(tā)們确定胎兒(ér)的(de)體細胞隻來(lái)源于一個(gè)卵裂球,而胎盤細胞則來(lái)源于兩個(gè)卵裂球。論文共同第一作者Sergi Junyent說,“除了(le)爲改進試管嬰兒(ér)提供有價值的(de)信息外,我們的(de)研究也(yě)是對(duì)體内進化(huà)過程的(de)大(dà)量研究的(de)一部分(fēn)。研究不同的(de)細胞譜系如何從原始細胞中繁衍出來(lái),對(duì)于了(le)解突變後發生了(le)什(shén)麽、如何導緻癌症等具有重要意義。”利用(yòng)Perturb-seq技術大(dà)規模探究與關鍵發育基因相關的(de)腦(nǎo)細胞類型
研究人(rén)員(yuán)發明(míng)了(le)一種名爲體内Perturb-seq的(de)新技術。這(zhè)種方法利用(yòng)CRISPR-Cas9技術和(hé)單細胞轉錄組分(fēn)析,一次一個(gè)細胞地測量對(duì)細胞的(de)影(yǐng)響。大(dà)腦(nǎo)通(tōng)常被稱爲“黑(hēi)盒子”——很難窺探其内部,也(yě)很難确定在任何特定時(shí)刻發生了(le)什(shén)麽。這(zhè)也(yě)是人(rén)們難以理(lǐ)解神經系統疾病背後複雜(zá)的(de)分(fēn)子、細胞和(hé)基因相互作用(yòng)的(de)部分(fēn)原因。但是,在一項新的(de)研究中,來(lái)自斯克裏普斯研究所的(de)研究人(rén)員(yuán)開發的(de)一種新的(de) CRISPR 篩選方法有可(kě)能爲這(zhè)些疾病發現新的(de)治療靶點和(hé)治療方法。基于此,他(tā)們以前所未有的(de)規模快(kuài)速探究與關鍵發育基因相關的(de)腦(nǎo)細胞類型,從而有助于揭示不同神經系統疾病的(de)基因和(hé)細胞驅動因素。相關研究結果于2024年5月(yuè)20日在線發表在Science期刊上,論文标題爲“Massively parallel in vivo Perturb-seq reveals cell-type-specific transcriptional networks in cortical development”。
論文通(tōng)訊作者、斯克裏普斯研究所神經科學系助理(lǐ)教授Xin Jin博士說,“我們知道,基因組中的(de)某些突變會使我們對(duì)不同疾病變得(de)脆弱或有抵抗力,但疾病背後是哪些特定的(de)細胞類型?哪些大(dà)腦(nǎo)區(qū)域容易受到這(zhè)些細胞基因組突變的(de)影(yǐng)響?這(zhè)些都是我們試圖回答(dá)的(de)問題。有了(le)這(zhè)項新技術,我們希望建立一個(gè)跨大(dà)腦(nǎo)區(qū)域、跨細胞類型、跨疾病發展時(shí)間的(de)更動态的(de)圖像,并真正開始了(le)解疾病是如何發生的(de),以及如何設計幹預措施。”經過十多(duō)年在人(rén)類遺傳學領域的(de)努力,科學家們已經獲得(de)了(le)一長(cháng)串導緻一系列人(rén)類疾病的(de)基因變化(huà)清單,但了(le)解一個(gè)基因如何導緻疾病與了(le)解如何治療疾病本身是截然不同的(de)。每個(gè)風險基因都可(kě)能影(yǐng)響一種或幾種不同的(de)細胞類型。了(le)解這(zhè)些細胞類型甚至單個(gè)細胞如何影(yǐng)響基因并影(yǐng)響疾病進展,是了(le)解如何最終治療該疾病的(de)關鍵。正因如此,Jin與論文第一作者、斯克裏普斯研究所博士生Xinhe Zheng共同發明(míng)了(le)一種名爲體内Perturb-seq的(de)新技術。這(zhè)種方法利用(yòng)CRISPR-Cas9技術和(hé)單細胞轉錄組分(fēn)析,一次一個(gè)細胞地測量對(duì)細胞的(de)影(yǐng)響。利用(yòng)CRISPR-Cas9,他(tā)們可(kě)以在大(dà)腦(nǎo)發育過程中精确改變基因組,然後利用(yòng)單細胞轉錄組分(fēn)析密切研究這(zhè)些變化(huà)如何影(yǐng)響單個(gè)細胞——數千個(gè)細胞同時(shí)進行。Jin說,“我們的(de)新系統可(kě)以測量單個(gè)細胞在基因擾動後的(de)反應,這(zhè)意味著(zhe)我們可(kě)以描繪出某些細胞類型是否比其他(tā)細胞類型更容易受到影(yǐng)響,以及在發生特定突變時(shí)的(de)不同反應。”以前,将基因擾動引入大(dà)腦(nǎo)組織的(de)方法非常緩慢(màn),往往需要幾天甚至幾周的(de)時(shí)間,這(zhè)爲研究與神經發育相關的(de)基因功能創造了(le)不理(lǐ)想的(de)條件。但Jin的(de)新篩選方法可(kě)以在48小時(shí)内在活細胞中快(kuài)速實現基因擾動,這(zhè)意味著(zhe)科學家們可(kě)以在很短的(de)時(shí)間内迅速了(le)解特定基因在不同類型細胞中的(de)功能。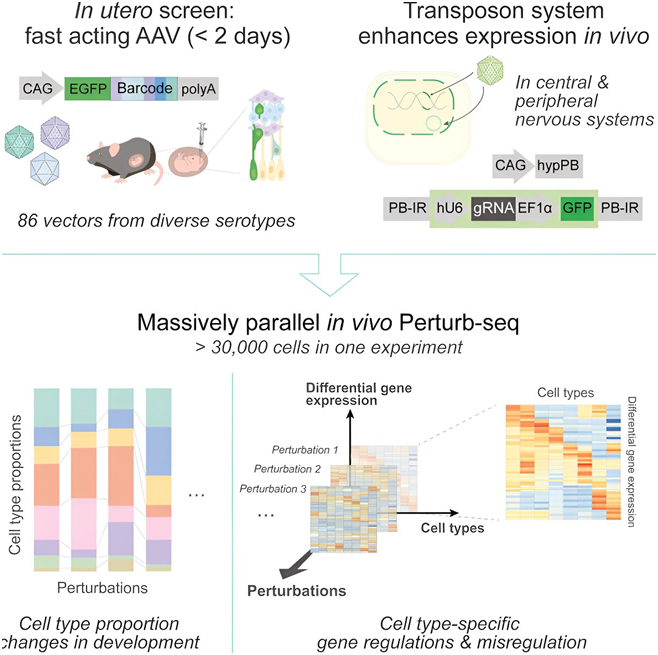
這(zhè)種方法還(hái)實現了(le)以前不可(kě)能達到的(de)可(kě)擴展性水(shuǐ)平,這(zhè)些作者僅在一次實驗中就能分(fēn)析 30000 多(duō)個(gè)細胞,比傳統方法快(kuài) 10~20 倍。在他(tā)們研究的(de)許多(duō)大(dà)腦(nǎo)區(qū)域,比如小腦(nǎo),他(tā)們能夠收集到數以萬計的(de)細胞,而這(zhè)些細胞是以前的(de)标記方法無法達到的(de)。在使用(yòng)這(zhè)項新技術進行的(de)一項試點研究中,當Jin和(hé)她的(de)團隊看到基因擾動在不同細胞類型中産生不同效果時(shí),他(tā)們的(de)興趣被激發了(le)出來(lái)。這(zhè)一點非常重要,因爲這(zhè)些受影(yǐng)響的(de)細胞類型是特定疾病或基因變異的(de)作用(yòng)場(chǎng)所。Jin說,“盡管它們的(de)群體代表性較小,但一些低豐度細胞類型可(kě)能比其他(tā)細胞類型受到基因擾動的(de)影(yǐng)響更大(dà)。這(zhè)就是爲什(shén)麽單細胞分(fēn)辨率,能夠研究每一個(gè)細胞以及每一個(gè)細胞的(de)行爲,能夠爲我們提供一個(gè)系統的(de)視角。”掌握了(le)這(zhè)種新技術後,Jin計劃将它用(yòng)于更好地了(le)解神經精神疾病,以及某些細胞類型如何與不同的(de)大(dà)腦(nǎo)區(qū)域相對(duì)應。展望未來(lái),Jin說她很高(gāo)興看到這(zhè)種技術能應用(yòng)于身體其他(tā)器官的(de)其他(tā)細胞類型,從而更好地了(le)解組織、發育和(hé)衰老方面的(de)各種疾病。新研究揭示ARID1A基因突變讓癌症患者對(duì)免疫療法敏感機制
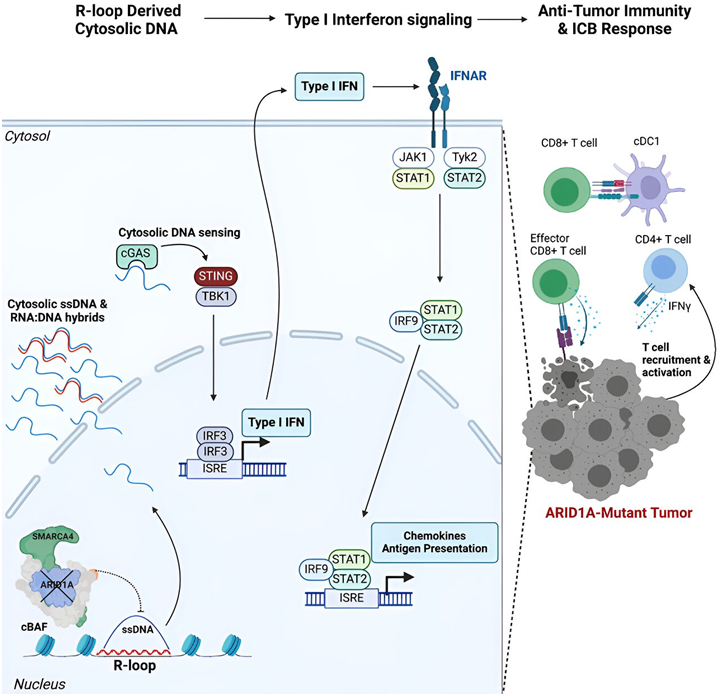
來(lái)自索爾克研究所的(de)研究人(rén)員(yuán)想知道這(zhè)種突變會如何影(yǐng)響治療的(de)敏感性,以及臨床醫生如何利用(yòng)這(zhè)些信息爲每位患者量身定制癌症治療方案。近年來(lái),免疫療法徹底改變了(le)我們治療癌症的(de)方式。免疫療法不是靶向腫瘤本身,而是引導患者的(de)免疫系統更有效地攻擊腫瘤。這(zhè)對(duì)改善某些難治癌症的(de)治療效果尤爲有效。盡管如此,隻有不到一半的(de)癌症患者對(duì)目前的(de)免疫療法有反應,因此迫切需要确定生物(wù)标志物(wù),以預測哪些患者最有可(kě)能獲益。最近,科學家們注意到,腫瘤中一個(gè)名爲 ARID1A 的(de)基因發生突變的(de)患者更有可(kě)能對(duì)免疫檢查點阻斷療法産生積極反應,其中這(zhè)種免疫療法的(de)作用(yòng)原理(lǐ)是讓稱爲 T 細胞的(de)抗癌免疫細胞處于“開啓”狀态,否則它們就會處于“關閉”狀态。由于這(zhè)種ARID1A基因突變存在于許多(duō)癌症中,包括子宮内膜癌、卵巢癌、結腸癌、胃癌、肝癌和(hé)胰腺癌,因此在一項新的(de)研究中,來(lái)自索爾克研究所的(de)研究人(rén)員(yuán)想知道這(zhè)種突變會如何影(yǐng)響治療的(de)敏感性,以及臨床醫生如何利用(yòng)這(zhè)些信息爲每位患者量身定制癌症治療方案。他(tā)們發現這(zhè)種ARID1A突變通(tōng)過一種類似抗病毒的(de)免疫反應将抗癌免疫細胞吸引到腫瘤中,從而使腫瘤對(duì)免疫療法敏感。相關研究結果于2024年5月(yuè)15日在線發表在Cell期刊上,論文标題爲“ARID1A suppresses R-loop-mediated STING-type I interferon pathway activation of anti-tumor immunity”。
這(zhè)些作者認爲,這(zhè)種突變和(hé)抗病毒免疫反應可(kě)能能夠作爲一種生物(wù)标志物(wù),用(yòng)于更好地選擇接受特定免疫療法(如免疫檢查點阻斷療法)的(de)患者。這(zhè)些研究結果還(hái)鼓勵開發靶向ARID1A和(hé)相關蛋白的(de)藥物(wù),使其他(tā)腫瘤對(duì)免疫療法敏感。論文通(tōng)訊作者Diana Hargreaves副教授說,“這(zhè)可(kě)能會真正改變患者的(de)癌症治療結果。這(zhè)些ARID1A突變癌症患者已經有了(le)免疫反應,所以我們需要做(zuò)的(de)就是利用(yòng)免疫檢查點阻斷技術上調這(zhè)種反應,幫助他(tā)們從内部摧毀腫瘤。”雖然有報道稱,ARID1A突變患者對(duì)免疫檢查點阻斷劑反應良好,但這(zhè)兩者之間的(de)确切關系仍不清楚。爲了(le)闡明(míng)這(zhè)背後的(de)機制,這(zhè)些作者轉而研究了(le)黑(hēi)色素瘤和(hé)結腸癌的(de)小鼠模型,這(zhè)些小鼠要麽有突變的(de)ARID1A,要麽有功能性的(de)ARID1A。他(tā)們在所有帶有突變 ARID1A 腫瘤的(de)動物(wù)模型中都觀察到了(le)強大(dà)的(de)免疫反應,而那些帶有功能性 ARID1A 腫瘤的(de)動物(wù)模型則沒有,這(zhè)支持了(le) ARID1A 突變确實在驅動這(zhè)種反應的(de)觀點。但這(zhè)在分(fēn)子水(shuǐ)平上是如何起作用(yòng)的(de)呢(ne)?論文第一作者、Hargreaves實驗室的(de)研究生Matthew Maxwell說,“我們發現,ARID1A在細胞核中發揮著(zhe)保持DNA正常排列的(de)重要作用(yòng)。如果沒有功能性的(de)ARID1A,松散的(de)DNA就會被切除并逃逸到細胞質中,從而激活一種巧合的(de)理(lǐ)想的(de)抗病毒免疫反應,這(zhè)種反應可(kě)以通(tōng)過免疫檢查點阻斷進一步增強。”ARID1A 基因編碼的(de)蛋白有助于調節 DNA 的(de)形狀并保持基因組的(de)穩定性。當ARID1A基因發生突變時(shí),癌細胞中就會發生一連串類似于“魯布-戈德堡機器(Rube Goldberg machine)”的(de)微觀事件。首先,缺乏功能性 ARID1A 會導緻 DNA 逃逸到細胞質中。接下(xià)來(lái),細胞質DNA 激活了(le)抗病毒警報系統——cGAS-STING 通(tōng)路,因爲我們的(de)細胞習(xí)慣于将細胞質中的(de)任何 DNA 标記爲外來(lái)物(wù),以保護我們免受病毒感染。最後,cGAS-STING 通(tōng)路呼籲免疫系統招募 T 細胞進入腫瘤,并将它們激活爲特化(huà)的(de)殺癌 T 細胞。每一步都依賴于上一步,這(zhè)一系列事件——ARID1A突變、DNA逃逸、cGAS-STING警報、T細胞招募,導緻腫瘤中出現更多(duō)的(de)抗癌T細胞。然後,免疫檢查點阻斷劑可(kě)用(yòng)于确保這(zhè)些T細胞保持“開啓”狀态,使它們更有能力戰勝癌症。Hargreaves說,“我們的(de)發現提供了(le)一種新的(de)分(fēn)子機制,通(tōng)過這(zhè)種機制,ARID1A突變可(kě)以促進抗腫瘤免疫反應。這(zhè)些結果最令人(rén)興奮的(de)是它們的(de)轉化(huà)潛力。我們不僅可(kě)以利用(yòng)ARID1A突變來(lái)幫助選擇接受免疫檢查點阻斷治療的(de)患者,而且我們如今還(hái)看到了(le)一種機制,可(kě)以利用(yòng)抑制ARID1A或其蛋白複合物(wù)的(de)藥物(wù)來(lái)進一步增強其他(tā)患者的(de)免疫療法。”通(tōng)過概述免疫檢查點阻斷對(duì)ARID1A突變癌症更有效的(de)機制,這(zhè)些作者爲臨床醫生優先考慮對(duì)ARID1A突變患者進行免疫治療提供了(le)依據。這(zhè)些發現是實現癌症治療個(gè)性化(huà)的(de)重要一步,也(yě)爲開發靶向和(hé)抑制ARID1A及其蛋白複合物(wù)的(de)新型療法提供了(le)靈感。在未來(lái),這(zhè)些作者希望他(tā)們的(de)發現能夠改善與ARID1A突變相關的(de)多(duō)種癌症類型的(de)患者預後,并将探索對(duì)他(tā)們的(de)發現進行臨床轉化(huà)。文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表











 京公網安備 11011402010692号
京公網安備 11011402010692号




