
多(duō)囊卵巢綜合征(polycystic ovarian syndrome, PCOS)是一種常見的(de)生殖内分(fēn)泌疾病,影(yǐng)響著(zhe) 10% 至 13% 的(de)育齡婦女(nǚ),其特點是高(gāo)雄激素血症、排卵功能障礙、多(duō)囊卵巢形态,并經常伴有代謝紊亂。雄激素過多(duō)是導緻多(duō)囊卵巢綜合症諸多(duō)表型特征的(de)關鍵因素。盡管多(duō)囊卵巢綜合征的(de)發病率很高(gāo),但對(duì)這(zhè)種複雜(zá)的(de)綜合征進行藥物(wù)幹預卻面臨著(zhe)巨大(dà)的(de)挑戰。目前可(kě)用(yòng)于多(duō)囊卵巢綜合征的(de)治療方案非常有限,而且主要針對(duì)特定症狀的(de)管理(lǐ)。因此,迫切需要開發創新的(de)治療策略。
提取自青蒿植物(wù)的(de)青蒿素類藥物(wù)(artemisinins)因其對(duì)瘧疾的(de)療效而廣爲人(rén)知。科學家們此前已證實,青蒿素及其衍生物(wù)能夠通(tōng)過激活産熱(rè)脂肪細胞,促進能量消耗和(hé)提升胰島素敏感性,有效阻止飲食誘發的(de)肥胖和(hé)代謝失衡。
在一項新的(de)研究中,來(lái)自中國複旦大(dà)學、重慶醫科大(dà)學和(hé)中國藥科大(dà)學的(de)研究人(rén)員(yuán)通(tōng)過評估青蒿素衍生物(wù)對(duì)睾酮水(shuǐ)平、發情周期和(hé)多(duō)囊卵巢形态的(de)影(yǐng)響,探討(tǎo)了(le)青蒿素類藥物(wù)在齧齒類多(duō)囊卵巢綜合征樣模型和(hé)人(rén)類多(duō)囊卵巢綜合征患者中的(de)治療潛力。他(tā)們采用(yòng)體外和(hé)體内方法研究了(le)青蒿素對(duì)卵巢睾酮合成的(de)影(yǐng)響,還(hái)鑒别出了(le)青蒿素作用(yòng)的(de)直接分(fēn)子靶标,揭示了(le)其調節雄激素合成的(de)機理(lǐ)。
相關研究結果發表在2024年6月(yuè)14日的(de)Science期刊上,論文标題爲“Artemisinins ameliorate polycystic ovarian syndrome by mediating LONP1-CYP11A1 interaction”。論文通(tōng)訊作者爲複旦大(dà)學的(de)湯其群教授。

研究者們發現,青蒿素的(de)一種衍生物(wù),蒿甲醚,能顯著逆轉多(duō)囊卵巢綜合征(PCOS)模型動物(wù)中的(de)多(duō)種症狀,包括雄性激素過高(gāo)、月(yuè)經周期不規律、卵巢多(duō)囊樣改變及生育力下(xià)降。青蒿素類藥物(wù)通(tōng)過減少卵巢内睾酮的(de)産生,有效緩解了(le)雄性激素過高(gāo)的(de)狀況。利用(yòng)蛋白質組學分(fēn)析,他(tā)們發現,青蒿素作用(yòng)後顯著降低了(le)一種關鍵蛋白——參與雄激素合成首步反應的(de)細胞色素P450家族11亞家族A成員(yuán)1(CYP11A1)。
從機理(lǐ)上講,青蒿素類藥物(wù)直接靶向離子肽酶1(lon peptidase 1, LONP1),增強了(le) LONP1 與 CYP11A1 之間的(de)相互作用(yòng),促進了(le)由 LONP1 催化(huà)的(de) CYP11A1 降解。相反,雄激素誘導劑會破壞 LONP1 與 CYP11A1 之間的(de)結合。此外,LONP1 在多(duō)囊卵巢綜合征中表現爲明(míng)顯下(xià)調,導緻 CYP11A1 水(shuǐ)平升高(gāo)和(hé)雄激素合成增加。蛋白對(duì)接模拟和(hé)随後的(de)功能實驗表明(míng)青蒿素類藥物(wù)對(duì) CYP11A1 水(shuǐ)平的(de)抑制作用(yòng)主要取決于它們與 LONP1 蛋白水(shuǐ)解結構域的(de)直接結合。進一步支持上述功能的(de)是,LONP1的(de)過表達能強有力地減少卵巢雄激素生成,這(zhè)與青蒿素類藥物(wù)的(de)作用(yòng)效果相符。
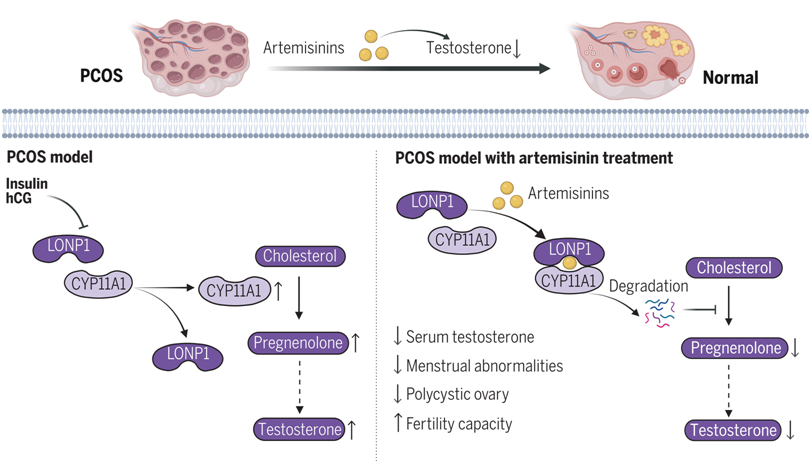
最後,爲了(le)證實青蒿素類藥物(wù)對(duì)多(duō)囊卵巢綜合征患者的(de)治療效果,研究人(rén)員(yuán)進行了(le)一項試點臨床試驗。他(tā)們發現雙氫青蒿素(dihydroartemisinin)治療可(kě)有效改善多(duō)囊卵巢綜合征患者的(de)高(gāo)雄激素血症,降低抗缪勒氏管激素水(shuǐ)平,改善多(duō)囊卵巢形态,并有助于月(yuè)經恢複正常。
綜上所述,這(zhè)些數據證明(míng)了(le)青蒿素類藥物(wù)在緩解齧齒類動物(wù)模型和(hé)人(rén)類患者多(duō)囊卵巢綜合征相關症狀方面的(de)功效。更重要的(de)是,這(zhè)一發現揭示了(le) LONP1 與 CYP11A1 之間以前未知的(de)相互作用(yòng),且青蒿素類藥物(wù)可(kě)以通(tōng)過增強這(zhè)一作用(yòng)路徑來(lái)調控雄激素合成,這(zhè)爲基于LONP1-CYP11A1交互作用(yòng)靶向治療PCOS提供了(le)新的(de)策略方向。






文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




