從結構上揭示人(rén)核外切體靶向複合物(wù)的(de)RNA監測機制
在生物(wù)學中,清除東西可(kě)能與制造東西一樣重要。細胞、蛋白或其他(tā)不再需要的(de)分(fēn)子的(de)堆積會導緻問題,因此生物(wù)已經進化(huà)出幾種清理(lǐ)它們的(de)方法。一個(gè)典型的(de)例子是RNA外切體(exosome,注意是外切體,而不是外泌體,雖然這(zhè)兩者的(de)英文單詞都是一樣的(de))。RNA分(fēn)子在細胞中發揮許多(duō)作用(yòng)。它們中的(de)一些被翻譯成蛋白;另一些形成了(le)細胞的(de)蛋白構建複合物(wù)。RNA外切體是一種細胞分(fēn)子機器,可(kě)以降解有問題、有害或不再需要的(de)RNA分(fēn)子。如果沒有這(zhè)種微小的(de)分(fēn)子機器來(lái)修剪那些不能激發快(kuài)樂(yuè)的(de)東西,我們的(de)細胞将成爲功能失調的(de)囤積者,無法發揮作用(yòng)。
紀念斯隆-凱特琳癌症中心結構生物(wù)學項目主席Christopher Lima博士解釋說,“RNA監控和(hé)降解途徑存在于所有的(de)生命形式中。從細菌到人(rén)類,所有生物(wù)都有監測RNA質量和(hé)有目的(de)地降解RNA的(de)機制。”
Lima博士說,在很長(cháng)一段時(shí)間裏,這(zhè)些途徑被認爲像家務勞動一樣,有點無聊。但事實證明(míng),這(zhè)些降解途徑受到高(gāo)度監管,控制著(zhe)從胚胎發育到細胞周期進展的(de)一切。更重要的(de)是,這(zhè)些途徑中的(de)錯誤可(kě)以導緻許多(duō)類型的(de)疾病,從癌症到神經變性。
在一項新的(de)研究中,Lima博士和(hé)Lima實驗室博士後研究員(yuán)M. Rhyan Puno提出了(le)有助于解釋RNA外切體如何定位需要被降解的(de)RNA的(de)研究結果。在低溫電鏡(cryo-EM)---一種先進的(de)成像技術---的(de)幫助下(xià),他(tā)們能夠破譯一種名爲人(rén)核外切體靶向(Nuclear Exosome Targeting, NEXT)複合物(wù)的(de)蛋白組裝體的(de)結構,這(zhè)種蛋白組裝體是這(zhè)種降解機制的(de)一個(gè)關鍵部分(fēn)。相關研究結果發表在2022年6月(yuè)9日的(de)Cell期刊上,論文标題爲“Structural basis for RNA surveillance by the human nuclear exosome targeting (NEXT) complex”。
Puno博士說,“我們已知道NEXT複合物(wù)靶向遞送RNA到RNA外切體,但從生化(huà)和(hé)結構上看,我們并不知道它是什(shén)麽樣子的(de),也(yě)不知道它是如何起作用(yòng)的(de)。”如今,通(tōng)過低溫電鏡,他(tā)們獲得(de)了(le)NEXT與RNA結合在一起的(de)第一批清晰圖片。這(zhè)些圖片,與伴随的(de)生物(wù)化(huà)學和(hé)生物(wù)學實驗一起,爲RNA分(fēn)子如何被遞送給RNA外切體進行降解提供了(le)新線索。幾年前,Puno博士開始使用(yòng)當時(shí)的(de)金标準方法---X射線晶體學衍射---研究NEXT的(de)結構。在這(zhè)種方法中,首先将蛋白制成晶體,使其以相同的(de)方式排列。然後,讓X射線穿過晶體,擊中探測器的(de)X射線模式經解釋後可(kě)确定蛋白的(de)結構。雖然Puno博士能夠将NEXT進行結晶,但由此産生的(de)X射線衍射圖片并不足以看到它的(de)結構的(de)細節。他(tā)說,“但後來(lái)出現了(le)低溫電鏡革命。低溫電鏡幫助我們看到了(le)NEXT的(de)樣子以及它如何結合它的(de)RNA底物(wù)。”低溫電鏡的(de)工作原理(lǐ)是捕捉冷(lěng)凍但非結晶的(de)蛋白樣本的(de)許多(duō)不同圖像,然後使用(yòng)計算(suàn)方法将它們排列成最終的(de)清晰圖像。Lima博士說,“這(zhè)幾乎就像捕捉一隻飛(fēi)行中的(de)鳥的(de)一堆照(zhào)片。因爲有各種混亂的(de)動作,鳥的(de)翅膀可(kě)能看起來(lái)很模糊。但如果我們能在所有這(zhè)些不同的(de)照(zhào)片中找到翅膀的(de)部分(fēn),那麽我們就能将這(zhè)些照(zhào)片對(duì)齊,以重建鳥類的(de)翅膀是什(shén)麽樣子,并确定它們是如何起作用(yòng)的(de)。”從這(zhè)些低溫電鏡圖片中,他(tā)們能夠看到NEXT蛋白形成了(le)一種非常靈活的(de)二聚體---這(zhè)意味著(zhe)NEXT蛋白的(de)兩個(gè)拷貝作爲一個(gè)功能單元連接在一起。Puno博士說,“這(zhè)真地非常、非常令人(rén)費解”。他(tā)指出,二聚體的(de)形成在以前還(hái)沒有對(duì)這(zhè)些類型的(de)蛋白進行過可(kě)視化(huà)觀察。
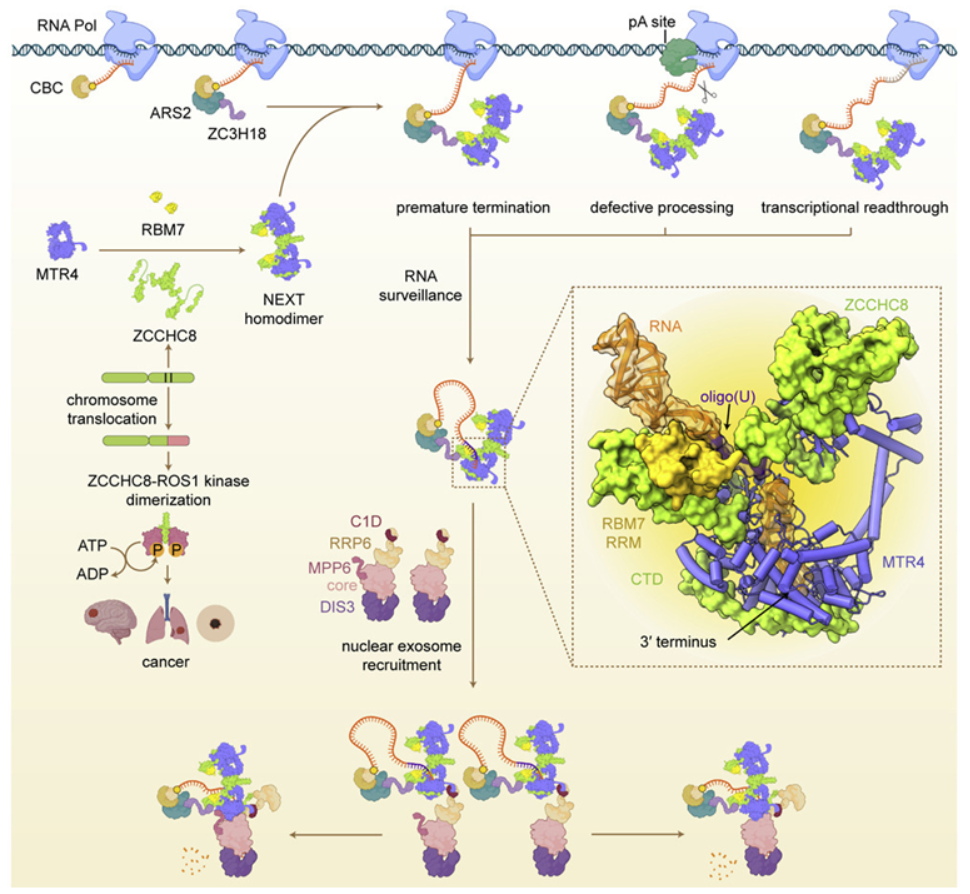
他(tā)繼續說,“從我們進行的(de)生化(huà)實驗中,我們知道二聚體化(huà)對(duì)降解有一定的(de)重要性。但對(duì)我們來(lái)說,這(zhè)種二聚體在引導RNA到RNA外切體中起什(shén)麽作用(yòng)仍然是個(gè)謎。”
爲了(le)幫助解開這(zhè)個(gè)謎團,他(tā)們希望在降解過程的(de)不同步驟中捕捉到NEXT複合物(wù)的(de)相互作用(yòng),然後用(yòng)低溫電鏡将這(zhè)些構象進行可(kě)視化(huà)觀察。這(zhè)其中有很大(dà)的(de)利害關系。RNA降解有多(duō)重要,從一長(cháng)串因降解缺陷或控制不當而導緻的(de)疾病中可(kě)以看出。也(yě)許最有名的(de)例子是囊性纖維化(huà)。在這(zhè)種疾病中,編碼一種在細胞膜上運送離子的(de)蛋白的(de)mRNA被RNA降解途徑所降解。因此,這(zhè)種蛋白不存在于肺部粘膜中,這(zhè)導緻那裏的(de)粘液堆積,并導緻嚴重的(de)呼吸障礙。Lima博士說,“這(zhè)是RNA質量控制導緻不良結果的(de)一個(gè)著名例子。”但RNA降解途徑的(de)缺陷也(yě)在幾種類型的(de)癌症中起作用(yòng)。事實上,在紀念斯隆-凱特琳癌症中心的(de)基因測試平台MSK-IMPACT中檢測到的(de)兩種基因突變是在與RNA外切體途徑相關的(de)基因---包括NEXT複合物(wù)中的(de)一種蛋白---中發現的(de)。Lima博士解釋說,不僅是mRNA需要适當的(de)質量控制。“現實是,如果你的(de)RNA質量控制途徑有缺陷,你的(de)核糖體不工作,你的(de)tRNA不工作,你的(de)剪接體不工作。”這(zhè)樣的(de)例子不勝枚舉。RNA所執行的(de)功能的(de)廣度解釋了(le)爲什(shén)麽有缺陷的(de)RNA降解途徑可(kě)以産生如此連環的(de)緻病影(yǐng)響。理(lǐ)解這(zhè)些影(yǐng)響将需要更深入、更廣泛地了(le)解不僅是RNA外切體本身,而且還(hái)有幫助監視RNA并決定何時(shí)RNA有缺陷或不再需要的(de)“上遊”蛋白,比如NEXT。Lima博士說,“我們的(de)夢想是啓動RNA降解反應,将樣本放入低溫電鏡中,并在它的(de)工作過程中通(tōng)過觀察進行所有可(kě)能的(de)确認。作爲結構生物(wù)學家,我們希望能夠看到實際的(de)過程,然後能夠重新組裝它們。”
基于CRISPR技術的(de)新型圖譜将每個(gè)人(rén)類基因與其功能關聯在一起
人(rén)類基因組計劃(Human Genome Project)是一項雄心勃勃的(de)舉措,旨在對(duì)人(rén)類的(de)每個(gè)DNA片段進行測序。該項目吸引了(le)來(lái)自世界各地研究機構(包括懷特黑(hēi)德研究所)的(de)合作者,并最終于2003年完成。如今,二十多(duō)年過去了(le),懷特黑(hēi)德研究所成員(yuán)Jonathan Weissman及其同事們在一項新的(de)研究中超越了(le)人(rén)類基因組序列,首次全面地構建出人(rén)類細胞中表達的(de)基因的(de)功能圖譜。相關研究結果于2022年6月(yuè)9日在線發表在Cell期刊上,論文标題爲“Mapping information-rich genotype-phenotype landscapes with genome-scale Perturb-seq”。他(tā)們将每個(gè)基因與它在細胞中的(de)作用(yòng)聯系起來(lái),這(zhè)是多(duō)年來(lái)在單細胞測序方法Perturb-seq上合作的(de)成果。
這(zhè)些數據可(kě)以在Weissman實驗室的(de)網站上找到,供其他(tā)科學家使用(yòng)。Weissman說,“這(zhè)是一個(gè)大(dà)資源,就像人(rén)類基因組是一個(gè)大(dà)資源一樣,你可(kě)以進去并進行基于發現的(de)研究。與其提前确定你要研究的(de)生物(wù)學,不如擁有這(zhè)張基因型-表型關系圖,你可(kě)以進去篩選這(zhè)個(gè)數據庫,而不必做(zuò)任何實驗。”這(zhè)種篩選使得(de)這(zhè)些作者能夠深入研究各種生物(wù)學問題。他(tā)們用(yòng)它來(lái)探索功能未知的(de)基因對(duì)細胞的(de)影(yǐng)響,研究線粒體對(duì)應激的(de)反應,并篩選出導緻染色體丢失或增加的(de)基因,一種在過去被證明(míng)很難研究的(de)表型。論文共同通(tōng)訊作者、前Weissman實驗室博士後Tom Norman說,“我認爲這(zhè)個(gè)數據集将使那些來(lái)自生物(wù)學其他(tā)領域的(de)人(rén)能夠進行各種我們甚至還(hái)沒有想到的(de)分(fēn)析,突然之間他(tā)們就有了(le)可(kě)以利用(yòng)的(de)數據。”這(zhè)項新的(de)研究利用(yòng)了(le)Perturb-seq方法,該方法可(kě)以以前所未有的(de)深度追蹤開啓或關閉基因的(de)影(yǐng)響。該方法由包括Weissman和(hé)麻省理(lǐ)工學院教授Aviv Regev在内的(de)一組研究人(rén)員(yuán)于2016年首次發表,但隻能用(yòng)于小規模的(de)基因集,且花費巨大(dà)(Cell, 2016, doi:10.1016/j.cell.2016.11.038)。論文共同第一作者、Weissman實驗室醫學博士生Joseph Replogle的(de)基礎研究工作使得(de)大(dà)規模的(de)Perturb-seq圖譜成爲可(kě)能。Replogle與Norman、Britt Adamson(普林(lín)斯頓大(dà)學分(fēn)子生物(wù)學系助理(lǐ)教授)以及10x Genomics公司的(de)一個(gè)小組合作,著(zhe)手構建一個(gè)可(kě)以擴大(dà)規模的(de)新版Perturb-seq。他(tā)們于2020年在Nature Biotechnology期刊上發表了(le)一篇概念驗證的(de)論文(Nature Biotechnology, 2020, doi:10.1038/s41587-020-0470-y)。Perturb-seq方法使用(yòng)CRISPR/Cas9基因組編輯将遺傳變化(huà)引入細胞,然後使用(yòng)單細胞RNA測序來(lái)捕獲有關因特定遺傳變化(huà)而表達的(de)RNA的(de)信息。因爲RNA控制著(zhe)細胞行爲方式的(de)所有方面,這(zhè)種方法可(kě)以幫助破解遺傳變化(huà)的(de)許多(duō)細胞影(yǐng)響。自從他(tā)們最初的(de)概念驗證論文發表以來(lái),Weissman、Regev和(hé)其他(tā)人(rén)已經在更小的(de)範圍内使用(yòng)這(zhè)種測序方法。例如,他(tā)們在2021年使用(yòng)Perturb-seq來(lái)探索人(rén)類和(hé)病毒基因在感染HCMV(一種常見的(de)疱疹病毒)的(de)過程中如何相互作用(yòng)(Nature Biotechnology, 2021, doi:10.1038/s41587-021-01059-3)。在這(zhè)項新的(de)研究中,Replogle和(hé)包括論文共同第一作者、Weissman實驗室研究生Reuben Saunders在内的(de)合作者,将這(zhè)種方法擴大(dà)到整個(gè)基因組。他(tā)使用(yòng)人(rén)類血癌細胞系以及來(lái)自視網膜的(de)非癌細胞,對(duì)超過250萬個(gè)細胞進行了(le)Perturb-seq,并利用(yòng)這(zhè)些數據建立了(le)一個(gè)将基因型和(hé)表型聯系起來(lái)的(de)全面圖譜。在完成這(zhè)種篩選後,這(zhè)些作者決定将他(tā)們的(de)新數據集投入使用(yòng),并研究一些生物(wù)學問題。Norman說,“Perturb-seq的(de)優勢在于它可(kě)以讓你以無偏見的(de)方式獲得(de)一個(gè)大(dà)數據集。沒有人(rén)完全知道你能從這(zhè)種數據集中得(de)到什(shén)麽限制。現在的(de)問題是,你到底用(yòng)它做(zuò)什(shén)麽?”第一個(gè)最明(míng)顯的(de)應用(yòng)是研究具有未知功能的(de)基因。鑒于這(zhè)種篩選也(yě)讀出了(le)許多(duō)已知基因的(de)表型,這(zhè)些作者可(kě)以用(yòng)這(zhè)些數據來(lái)比較未知基因和(hé)已知基因,并尋找類似的(de)轉錄結果,這(zhè)可(kě)能表明(míng)這(zhè)些基因産物(wù)作爲一個(gè)更大(dà)的(de)複合物(wù)的(de)一部分(fēn)一起發揮作用(yòng)。一個(gè)名爲C7orf26的(de)基因的(de)突變尤其引人(rén)注目。這(zhè)些作者注意到,那些在移除後導緻類似表型的(de)基因是一種叫做(zuò)Integrator的(de)蛋白複合體的(de)一部分(fēn),該複合體在産生小核 RNA方面起著(zhe)作用(yòng)。Integrator複合體由許多(duō)較小的(de)亞基組成---以前的(de)研究表明(míng)有14個(gè)單獨的(de)蛋白---他(tā)們能夠确認C7orf26是該複合體的(de)第15個(gè)組分(fēn)。他(tā)們還(hái)發現,這(zhè)15個(gè)亞基在較小的(de)模塊中一起發揮作用(yòng),在Integrator複合體中執行特定的(de)功能。Saunders說,“如果沒有這(zhè)種高(gāo)清晰的(de)圖譜,就不太清楚這(zhè)些不同的(de)模塊在功能上是如此不同。”Perturb-seq的(de)另一個(gè)好處是,由于這(zhè)種檢測方法專注于單細胞,這(zhè)些作者可(kě)以利用(yòng)這(zhè)些數據來(lái)觀察更複雜(zá)的(de)表型,因爲當它們與其他(tā)細胞的(de)數據一起研究時(shí),這(zhè)些表型就會變得(de)模糊不清。Weissman說,“我們經常把所有‘基因X’被敲除的(de)細胞拿出來(lái),對(duì)它們進行平均取值,看它們如何變化(huà)。但有時(shí)當你敲除一個(gè)基因時(shí),失去同一基因的(de)不同細胞會有不同的(de)行爲,而這(zhè)種行爲可(kě)能會被這(zhè)種平均取值所忽略。”
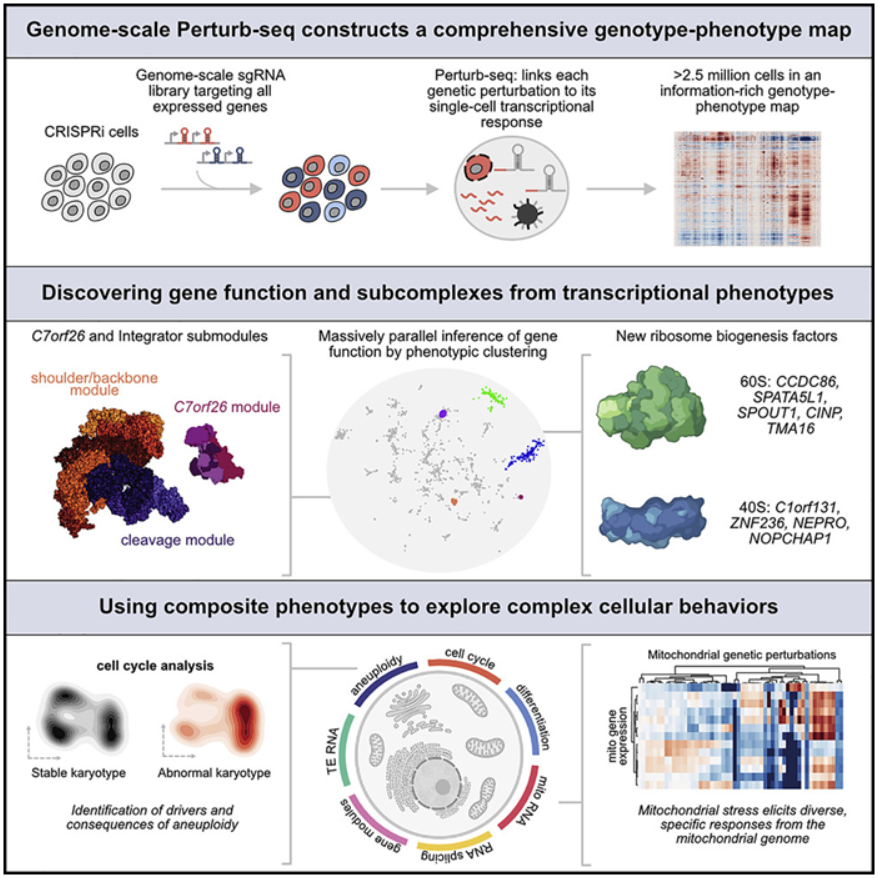
這(zhè)些作者發現,在移除後在不同細胞中出現不同結果的(de)一個(gè)基因子集負責染色體的(de)分(fēn)離。它們的(de)移除導緻細胞失去一條染色體或獲得(de)一條額外的(de)染色體,這(zhè)種情況被稱爲非整倍體。Weissman 說,“你無法預測失去這(zhè)個(gè)基因的(de)轉錄反應是什(shén)麽,因爲它取決于你獲得(de)或失去哪條染色體的(de)次級效應。我們意識到,我們可(kě)以逆轉這(zhè)種情況,構建這(zhè)種複合表型,尋找染色體獲得(de)和(hé)丢失的(de)特征。通(tōng)過這(zhè)種方式,我們對(duì)正确分(fēn)離DNA所需的(de)因子進行了(le)第一次全基因組篩選。”Norman說,“我認爲這(zhè)項非整倍體研究是迄今爲止這(zhè)些數據的(de)最有趣的(de)應用(yòng)。它捕捉了(le)一個(gè)你隻能用(yòng)單細胞讀出的(de)表型。你不能用(yòng)其他(tā)方式去捕捉它。”這(zhè)些作者還(hái)利用(yòng)他(tā)們的(de)數據集來(lái)研究線粒體如何對(duì)應激做(zuò)出反應。從自由生活的(de)細菌進化(huà)而來(lái)的(de)線粒體在它的(de)基因組中攜帶13個(gè)基因。在細胞核DNA内,大(dà)約有1000個(gè)基因與線粒體功能有某種程度的(de)關系。Replogle說,“長(cháng)期以來(lái),人(rén)們一直對(duì)細胞核DNA和(hé)線粒體DNA在不同的(de)細胞條件下(xià)如何協調和(hé)調控很感興趣,尤其是當細胞遭受應激時(shí)。”這(zhè)些作者發現,當他(tā)們幹擾不同的(de)線粒體相關基因時(shí),細胞核基因組對(duì)許多(duō)不同的(de)基因變化(huà)的(de)反應是相似的(de)。然而,線粒體基因組反應的(de)變化(huà)要大(dà)得(de)多(duō)。Replogle說,“線粒體爲什(shén)麽仍有自己的(de)DNA,這(zhè)仍然是一個(gè)懸而未決的(de)問題。從我們的(de)研究中得(de)到的(de)一個(gè)大(dà)的(de)啓示是,擁有獨立的(de)線粒體基因組的(de)一個(gè)好處可(kě)能是對(duì)不同的(de)應激源有局部的(de)或非常特異的(de)遺傳調節作用(yòng)。”Weissman說,“如果一個(gè)線粒體被破壞,而另一個(gè)線粒體以不同的(de)方式被破壞,這(zhè)些線粒體可(kě)能會有不同的(de)反應。”在未來(lái),這(zhè)些作者希望将Perturb-seq用(yòng)于他(tā)們開始使用(yòng)的(de)癌細胞系以外的(de)不同類型的(de)細胞。他(tā)們還(hái)希望繼續探索他(tā)們的(de)基因功能圖譜,并希望其他(tā)人(rén)也(yě)能這(zhè)樣做(zuò)。Norman說,“這(zhè)确實是這(zhè)些作者和(hé)其他(tā)合作者多(duō)年研究工作的(de)結晶,我真地很高(gāo)興看到它繼續成功和(hé)擴大(dà)。”
遺傳進化(huà)和(hé)微環境相互作用(yòng)導緻膠質瘤進展
在一項新的(de)研究中,來(lái)自荷蘭阿姆斯特丹大(dà)學、美(měi)國傑克遜基因組醫學實驗室和(hé)哥(gē)倫比亞大(dà)學醫學中心等研究機構的(de)研究人(rén)員(yuán)發現作爲一種常見的(de)大(dà)腦(nǎo)和(hé)脊髓腫瘤,浸潤性膠質瘤(infiltrating glioma)是由其遺傳進化(huà)和(hé)微環境決定的(de),這(zhè)一發現可(kě)能導緻更有針對(duì)性的(de)治療。相關研究結果發表在2022年6月(yuè)9日的(de)Cell期刊上,論文标題爲“Glioma progression is shaped by genetic evolution and microenvironment interactions”。
論文共同作者、科羅拉多(duō)大(dà)學癌症中心成員(yuán)D.Ryan Ormond博士說,“我們确定了(le)複發時(shí)的(de)表觀遺傳學改變,這(zhè)些改變不僅在某些病例中具有預後作用(yòng),而且可(kě)能導緻針對(duì)不同亞型的(de)不同治療方案,從而改善長(cháng)期生存。”這(zhè)些作者觀察了(le)膠質瘤如何與大(dà)腦(nǎo)相互作用(yòng),随著(zhe)時(shí)間的(de)推移發生變化(huà),産生治療抵抗性并變得(de)更具侵襲性。他(tā)們确定了(le)膠質瘤複發時(shí)的(de)三種不同表型,或者說可(kě)觀察到的(de)特征---神經元型、間充質型和(hé)增殖型。它們中的(de)每一種都有細胞、遺傳和(hé)組織學特征,這(zhè)些特征在複發時(shí)會顯現出來(lái)。其中一些特征與不太有利的(de)結果有關。在這(zhè)項新的(de)研究中,這(zhè)些作者使用(yòng)了(le)膠質瘤縱向分(fēn)析聯盟(Glioma Longitudinal Analysis Consortium, GLASS)的(de)參與者樣本,該聯盟是爲了(le)确定膠質瘤治療抵抗性的(de)驅動因素而成立的(de)。他(tā)們分(fēn)析了(le)來(lái)自304名患有異檸檬酸脫氫酶(IDH)野生型膠質瘤和(hé)IDH突變型膠質瘤的(de)成年患者的(de)腫瘤樣本的(de)RNA和(hé)/或DNA測序數據。腫瘤複發的(de)方式取決于IDH突變狀态。它們在複發過程中發生的(de)變化(huà)取決于它們與它們所居住的(de)微環境的(de)相互作用(yòng)方式。
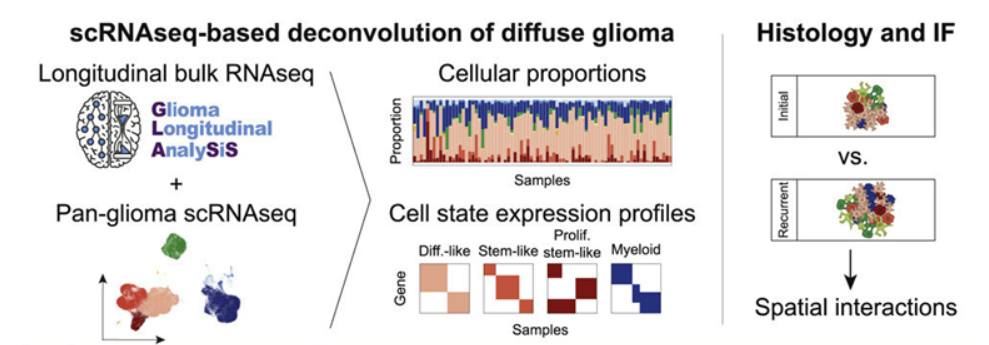
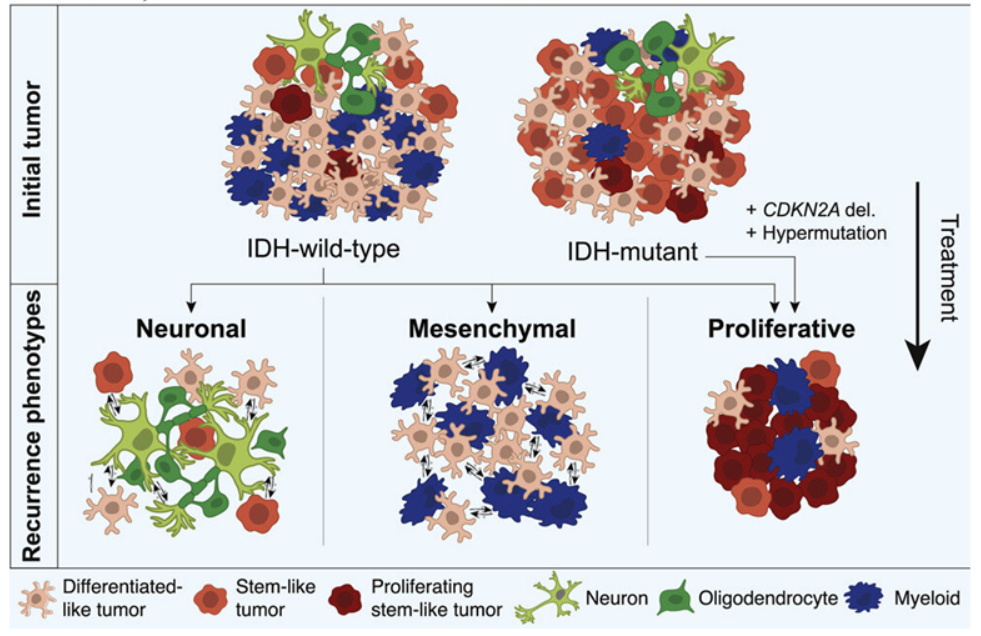
這(zhè)些作者發現,許多(duō)IDH野生型膠質瘤在複發時(shí)更具侵入性。他(tā)們的(de)腫瘤細胞顯示出神經元信号程序的(de)增加,這(zhè)表明(míng)神經元的(de)相互作用(yòng)在引發這(zhè)種腫瘤的(de)進展中可(kě)能發揮了(le)作用(yòng)。他(tā)們還(hái)發現通(tōng)常由替莫唑胺(temozolomide)等藥物(wù)治療誘發的(de)高(gāo)突變(hypermutation),以及産生腫瘤抑制蛋白的(de)CDKN2A基因的(de)缺失,與這(zhè)兩種膠質瘤亞型複發時(shí)腫瘤細胞的(de)增殖有關。在IDH野生型和(hé)IDH突變型膠質瘤中,這(zhè)種高(gāo)突變與幹細胞樣腫瘤細胞(stem-like neoplastic cell)的(de)數量增加有關。這(zhè)些細胞的(de)生長(cháng)降低了(le)患者的(de)總體生存率。這(zhè)些作者指出,“總的(de)來(lái)說,這(zhè)些結果表明(míng),複發時(shí)的(de)遺傳進化(huà)可(kě)以改變膠質瘤細胞,使其朝著(zhe)與預後不良有關的(de)更多(duō)增殖表型發展。”Ormond說,“治療抵抗性仍然是膠質瘤患者的(de)一個(gè)嚴重障礙,爲了(le)提高(gāo)生活質量和(hé)生存率,需要克服它。”他(tā)說,這(zhè)些發現将使醫生能夠以新的(de)藥物(wù)和(hé)治療方法更好地治療這(zhè)種癌症。
在一項新的(de)針對(duì)小鼠的(de)研究中,來(lái)自斯坦福大(dà)學醫學院的(de)研究人(rén)員(yuán)發現一種利用(yòng)患者自身的(de)經過基因修飾的(de)免疫細胞來(lái)攻擊癌細胞的(de)癌症治療方法,當可(kě)以通(tōng)過口服藥物(wù)進行開啓和(hé)關閉時(shí),會更安全和(hé)更有效。相關研究結果發表在2022年5月(yuè)12日的(de)Cell期刊上,論文标題爲“Enhanced safety and efficacy of protease-regulated CAR-T cell receptors”。

論文通(tōng)訊作者、布萊根婦女(nǚ)醫院神經病學系運動障礙科主任Vikram Khurana博士說,“我們的(de)研究爲α-突觸核蛋白提供了(le)新的(de)見解,這(zhè)種蛋白被認爲是帕金森病和(hé)相關疾病産生的(de)核心。目前的(de)治療方法靶向這(zhè)種蛋白,但是它的(de)功能一直不明(míng)确。傳統上,α-突觸核蛋白被認爲在與細胞膜結合和(hé)稱爲囊泡的(de)運輸結構中發揮了(le)作用(yòng)。但我們的(de)研究表明(míng)α-突觸核蛋白有雙重身份。”Khurana及其同事們的(de)最初線索來(lái)自于α-突觸核蛋白毒性的(de)酵母和(hé)果蠅模型,并通(tōng)過對(duì)人(rén)類細胞、患者衍生的(de)神經元和(hé)人(rén)類遺傳學的(de)研究得(de)到證實。他(tā)們發現α-突觸核蛋白與囊泡相互作用(yòng)的(de)部分(fēn)也(yě)與稱爲處理(lǐ)小體(processing body, P-body)的(de)結構結合,其中P-body是細胞中通(tōng)過信使RNA(mRNA)調節基因表達的(de)分(fēn)子機器。在由源自攜帶α-突觸核蛋白基因突變的(de)PD患者的(de)誘導性多(duō)能幹細胞産生的(de)神經元中,P-body的(de)生理(lǐ)結構和(hé)功能喪失,mRNA遭受異常調控。同樣的(de)情況也(yě)發生在來(lái)自患者死後大(dà)腦(nǎo)的(de)組織樣本中。人(rén)類基因分(fēn)析支持了(le)這(zhè)些發現的(de)疾病相關性:在P-body基因中積累突變的(de)患者似乎有更高(gāo)的(de)PD風險。
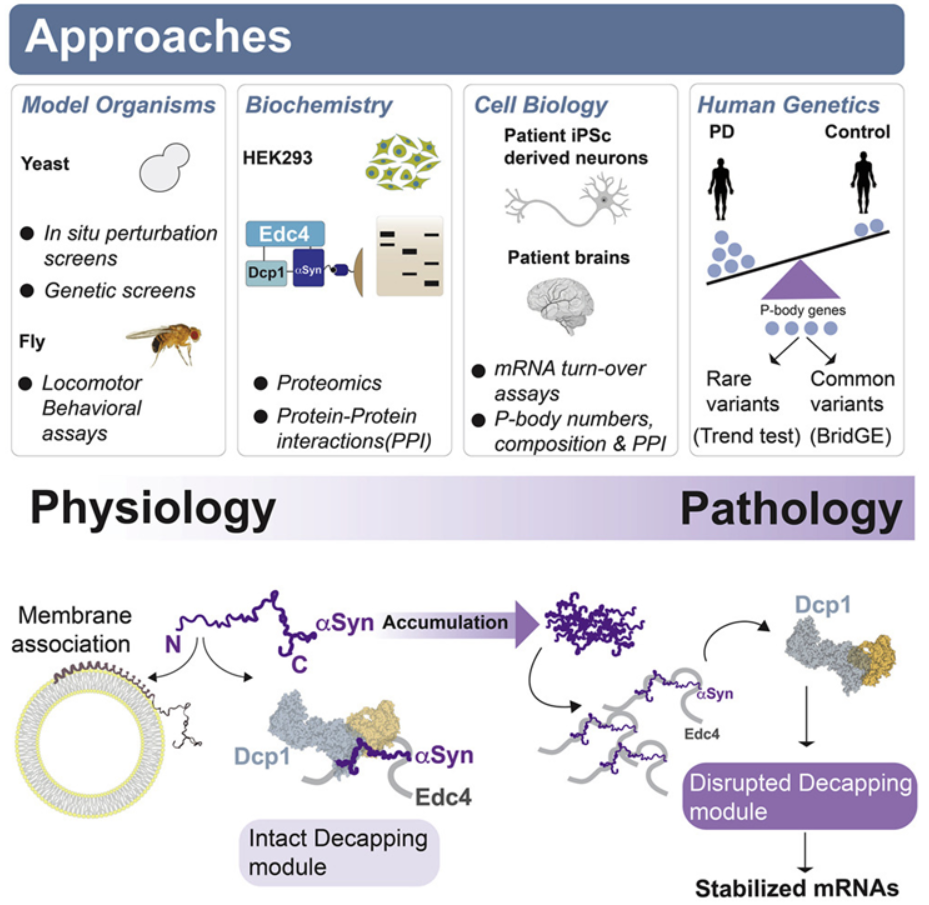
這(zhè)些作者将α-突觸核蛋白描述爲一種“切換開關”,調節著(zhe)兩種非常不同的(de)功能:囊泡運輸和(hé)基因表達。在疾病狀态下(xià),這(zhè)種平衡被打破。這(zhè)些發現對(duì)PD治療方法的(de)開發有潛在的(de)影(yǐng)響。他(tā)們指出,需要更清楚地了(le)解哪些P-body組分(fēn)可(kě)能是治療幹預的(de)最佳靶标。正在進行的(de)遺傳學研究旨在确定哪些患者可(kě)能最适合這(zhè)類幹預,以及這(zhè)種新發現的(de)途徑對(duì)PD患者的(de)疾病風險和(hé)疾病進展的(de)貢獻有多(duō)大(dà)。論文第一作者、布萊根婦女(nǚ)醫院神經病學系Erinc Hallacli博士說,“如果我們希望能夠開發針對(duì)α-突觸蛋白的(de)治療方法,那麽我們需要了(le)解這(zhè)種蛋白的(de)作用(yòng)以及降低其水(shuǐ)平或活性的(de)潛在後果。這(zhè)篇論文提供了(le)重要信息,填補了(le)我們對(duì)這(zhè)種蛋白的(de)知識空白,這(zhè)可(kě)能有利于臨床轉化(huà)。”
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。
返回列表













 京公網安備 11011402010692号
京公網安備 11011402010692号




