在COVID-19大(dà)流行的(de)兩年多(duō)時(shí)間裏,人(rén)們意識到“新常态”包括人(rén)類将有可(kě)能與SARS-CoV-2長(cháng)期共存。一些治療方法是可(kě)用(yòng)的(de),但随著(zhe)新變體的(de)出現,科學家們正在尋找新的(de)策略。在一項新的(de)研究中,來(lái)自美(měi)國佛羅裏達大(dà)學和(hé)瑞士蘇黎世大(dà)學等研究機構的(de)研究人(rén)員(yuán)指出,靶向人(rén)類蛋白Sec61的(de)抗癌候選藥物(wù)apratoxin S4(Apra S4)可(kě)以幹擾包括SARS-CoV-2和(hé)甲型流感病毒在内的(de)許多(duō)病毒的(de)複制,從而可(kě)能提供了(le)一種泛病毒療法。相關研究結果于2022年6月(yuè)29日在線發表在ACS Infectious Diseases期刊上,論文标題爲“Sec61 Inhibitor Apratoxin S4 Potently Inhibits SARS-CoV-2 and Exhibits Broad-Spectrum Antiviral Activity”。

盡管存在COVID-19疫苗,但一些接受過疫苗注射的(de)人(rén)仍然患上了(le)COVID-19,而世界上隻有一小部分(fēn)人(rén)口接種了(le)疫苗。這(zhè)意味著(zhe)仍然需要治療,現在有一些針對(duì)SARS-CoV-2的(de)RNA聚合酶---它用(yòng)來(lái)在人(rén)體細胞内制造更多(duō)的(de)病毒自己的(de)RNA。但是其中一些藥物(wù),如瑞德西韋(remdesivir),除非在非常早期階段使用(yòng),否則不會起作用(yòng),而且可(kě)能需要注射。
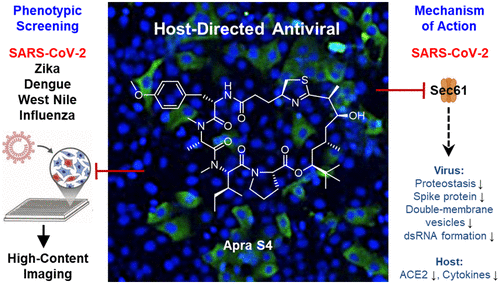
在尋找治療COVID-19的(de)新方法的(de)過程中,不同的(de)團隊已經重新審視了(le)那些已知可(kě)以對(duì)抗其他(tā)疾病的(de)藥物(wù),這(zhè)種策略被稱爲藥物(wù)“重新利用(yòng)”。其中一種臨床前階段的(de)化(huà)合物(wù)是apratoxin S4,它是一種基于海洋天然産物(wù)的(de)分(fēn)子,具有抗癌活性。以前的(de)研究表明(míng),apratoxin可(kě)以靶向一種叫做(zuò)Sec61的(de)人(rén)類蛋白,該蛋白可(kě)以确保某些蛋白發生正确糖基化(huà)和(hé)正确折疊。由于SARS-CoV-2沒有自己的(de)分(fēn)子機器來(lái)做(zuò)這(zhè)件事,它們劫持了(le)這(zhè)個(gè)過程,迫使人(rén)體細胞制造功能性的(de)病毒蛋白。Sec61對(duì)于甲型流感病毒、HIV和(hé)登革熱(rè)病毒造成感染是必不可(kě)少的(de),因此論文通(tōng)訊作者Hendrik Luesch及其同事們想知道apratoxin是否可(kě)以成爲一種廣泛有效的(de)也(yě)可(kě)以對(duì)抗SARS-CoV-2的(de)泛病毒藥物(wù)。
在對(duì)暴露于SARS-CoV-2的(de)猴子和(hé)人(rén)類細胞的(de)測試中,這(zhè)些作者發現,與瑞德西韋治療相比,用(yòng)apratoxin S4治療減少了(le)受感染的(de)細胞數量。apratoxin S4也(yě)有效地抵抗甲型流感病毒、寨卡病毒、登革熱(rè)病毒和(hé)西尼羅河(hé)病毒感染。進一步的(de)測試顯示,apratoxin S4沒有阻止SARS-CoV-2進入細胞,但它減少了(le)在細胞中産生和(hé)運輸的(de)病毒蛋白的(de)數量,特别是刺突蛋白,并且它減少了(le)病毒RNA的(de)複制。通(tōng)過電子顯微鏡,他(tā)們觀察到apratoxin S4也(yě)在很大(dà)程度上阻止了(le)新病毒的(de)形成,而且在SARS-CoV-2暴露的(de)猴子細胞中,許多(duō)囊泡中沒有或隻有很少的(de)全新病毒顆粒。他(tā)們說,還(hái)需要開展更多(duō)的(de)研究,但是這(zhè)些結果表明(míng),apratoxin S4和(hé)人(rén)類Sec61蛋白的(de)其他(tā)抑制劑是作用(yòng)廣泛的(de)抗病毒藥物(wù),可(kě)能有助于對(duì)抗未來(lái)的(de)大(dà)流行病。
異常增生往往有著(zhe)很高(gāo)的(de)癌症發生風險,然而,異常增生演變爲癌症背後的(de)細胞機制,目前研究人(rén)員(yuán)尚不清楚。近日,一篇發表在國際雜(zá)志Gastroenterology上題爲“Dysplastic stem cell plasticity functions as a driving force for neoplastic transformation of pre-cancerous gastric mucosa”的(de)研究報告中,來(lái)自範德堡大(dà)學醫學院等機構的(de)科學家們通(tōng)過研究揭示了(le)人(rén)類胃癌發生的(de)分(fēn)子機制,并提出了(le)相應的(de)預防性措施。
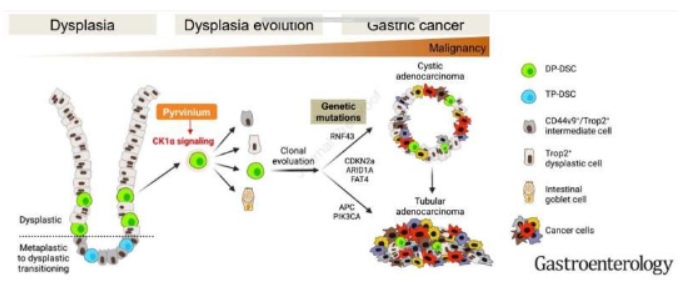
研究者Eunyoung Choi教授表示,他(tā)們通(tōng)過研究首次發現,Trop2+/CD133+/CD166+異常增生的(de)幹細胞或許是異常增生向多(duō)種類型胃癌發生的(de)克隆進化(huà)的(de)關鍵來(lái)源,進一步研究表明(míng),一種常用(yòng)于治療腸道蛲蟲的(de)藥物(wù)撲蛲靈(pyrvinium)或能通(tōng)過控制小鼠模型和(hé)人(rén)類類器官中的(de)CK1a信号蛋白,從而來(lái)阻斷異常增生幹細胞的(de)再生。
研究人(rén)員(yuán)所識别出的(de)異常增生的(de)幹細胞是在小鼠和(hé)人(rén)類胃部癌前轉化(huà)向異常增生的(de)緻癌轉變過程中首次出現的(de)幹細胞,本文研究還(hái)表明(míng),細胞命運的(de)動态變化(huà)和(hé)異常增生幹細胞的(de)進化(huà)過程或許能作爲異常增生過程中的(de)非癌變幹細胞單一類型,同時(shí)還(hái)能提供一條線索來(lái)幫助解釋胃癌發生過程中的(de)緻癌級聯反應、正常-轉化(huà)-異常增生-腺癌的(de)全部譜系信息。
在全球範圍内,胃癌是人(rén)類第五大(dà)常見的(de)癌症類型以及第三大(dà)緻死性癌症類型,異常增生,即細胞的(de)異常生長(cháng)和(hé)異常發育,其往往具有高(gāo)風險的(de)胃癌進展傾向,但研究人(rén)員(yuán)并不清楚這(zhè)些細胞發育爲癌細胞背後的(de)細胞機制。這(zhè)項研究中,研究人(rén)員(yuán)調查了(le)一系列過程揭示了(le)其中的(de)奧秘。
研究人(rén)員(yuán)利用(yòng)來(lái)自活性KRAS基因所誘導的(de)小鼠胃部異常增生類器官來(lái)進行轉錄組學分(fēn)析,同時(shí)他(tā)們還(hái)利用(yòng)新一代的(de)測序技術來(lái)分(fēn)析克隆進化(huà)過程中所發生的(de)細胞異質性和(hé)遺傳改變。

研究者Jimin Min說道,異常增生幹細胞的(de)幹性和(hé)可(kě)塑性往往會導緻胃腺癌的(de)連續進展,同時(shí)還(hái)概括了(le)在人(rén)類胃癌中所觀察到了(le)腫瘤異質性和(hé)遺傳改變。在實驗室研究中,研究者發現,藥物(wù)撲蛲靈是一種具有抗癌效應的(de)CK1a激動劑,其能選擇性地阻斷小鼠和(hé)人(rén)類機體中異常增生的(de)幹細胞的(de)幹性和(hé)活性,當前治療胃部異常增生的(de)療法标準僅限于内鏡下(xià)切除或小病竈的(de)外科手術切除,研究人(rén)員(yuán)總結道,利用(yòng)靶向CK1a激動劑來(lái)控制異常增生的(de)幹細胞活性的(de)靶向性治療措施或許有望作爲一種有效的(de)療法來(lái)降低異常增生進展爲胃癌的(de)風險。
綜上,本文研究結果表明(míng),異常增生的(de)幹細胞群或許是負責緻癌性轉化(huà)的(de)新型胃癌開啓細胞,同時(shí)研究人(rén)員(yuán)還(hái)提出了(le)一種有潛力的(de)靶點,或有望幫助開發阻斷胃癌早期誘導的(de)幹預措施。
多(duō)年來(lái),科學家們推測,心髒的(de)螺旋形排列和(hé)複雜(zá)的(de)肌肉組織能更有效地将血液輸送到整個(gè)身體。盡管由于很難在人(rén)造心髒中重現如此複雜(zá)和(hé)精巧的(de)細節,研究這(zhè)一現象被證明(míng)是困難的(de)。
不過,在一項新的(de)研究中,來(lái)自哈佛大(dà)學和(hé)匹茲堡大(dà)學的(de)研究人(rén)員(yuán)利用(yòng)一種新的(de)、更先進的(de)方法來(lái)制造人(rén)工組織和(hé)器官。相關研究結果發表在2022年7月(yuè)8日的(de)Science期刊上,論文标題爲“Recreating the heart’s helical structure-function relationship with focused rotary jet spinning”。

論文共同第一作者、匹茲堡大(dà)學斯萬森工程學院助理(lǐ)教授Qihan Liu說,“制造模拟生物(wù)組織的(de)材料是一個(gè)巨大(dà)的(de)制造挑戰。生物(wù)組織由各種複雜(zá)的(de)空間變化(huà)排列的(de)微/納米纖維組成。這(zhè)些纖維的(de)排列是大(dà)自然對(duì)生物(wù)組織豐富的(de)機械行爲進行編程的(de)方式。然而,目前還(hái)沒有任何制造工具能夠捕捉到這(zhè)種複雜(zá)的(de)排列。雖然普通(tōng)的(de)三維打印方法可(kě)以很容易地實現複雜(zá)的(de)纖維排列,但三維打印不能以與組織工程相關的(de)産量來(lái)打印納米纖維。雖然已有的(de)納米纖維紡絲技術,如靜電紡絲,能夠批量生産高(gāo)通(tōng)量的(de)納米纖維,但複雜(zá)的(de)纖維排列還(hái)沒有實現。”
這(zhè)些作者因此提出了(le)聚焦旋轉噴射紡絲(focused rotary jet spinning, FRJS)工藝。FRJS是一種利用(yòng)離心紡絲快(kuài)速成形纖維的(de)增材制造方法。這(zhè)些纖維随後在可(kě)控氣流中聚焦、對(duì)齊并沉積到目标位置。通(tōng)過使用(yòng)氣流,這(zhè)種方法允許同時(shí)操縱數以千計的(de)微/納米纖維,從而确保高(gāo)産量。通(tōng)過特别設計的(de)氣流,FRJS可(kě)以制造出比目前的(de)方法更複雜(zá)的(de)三維纖維結構。
這(zhè)些作者将他(tā)們的(de)方法與其他(tā)兩種生産人(rén)工器官和(hé)組織的(de)方法---三維打印和(hé)纖維紡絲(fiber spinning)---相比較。盡管三維打印繼續爲人(rén)工器官和(hé)組織的(de)發展做(zuò)出重大(dà)貢獻,但是他(tā)們反駁說,三維打印需要太長(cháng)的(de)時(shí)間來(lái)實現FRJS能夠提供的(de)細節和(hé)複雜(zá)性。
目前使用(yòng)的(de)另一種方法是纖維紡絲,它可(kě)以更快(kuài)地生産,但沒有FRJS那麽多(duō)的(de)細節或複雜(zá)性。因此,這(zhè)些作者将FRJS作爲一種以更及時(shí)的(de)方式進行更複雜(zá)創作的(de)方法。
爲了(le)展示FRJS在這(zhè)種情況下(xià)的(de)可(kě)能性,這(zhè)些作者使用(yòng)該工藝制造樣品,包括一個(gè)全尺寸的(de)纖維人(rén)類心髒模型,以展示制造複雜(zá)的(de)三維結構的(de)能力;一個(gè)三層雙腔心室模型,以展示捕捉生物(wù)組織中複雜(zá)的(de)纖維排列的(de)能力;以及單層心室,其大(dà)小相當大(dà)鼠、貓、人(rén)類和(hé)12000磅的(de)小鲸魚,以展示制造工藝的(de)可(kě)擴展性。他(tā)們還(hái)展示了(le)像FRJS構建的(de)這(zhè)些模型如何被用(yòng)來(lái)理(lǐ)解心髒内螺旋形細胞排列的(de)功能。
然而,這(zhè)些樣品隻是展示了(le)用(yòng)FRJS可(kě)以做(zuò)什(shén)麽。Liu說,“這(zhè)篇論文隻是展示了(le)用(yòng)這(zhè)種方法可(kě)以做(zuò)什(shén)麽。一切都是可(kě)能的(de)。”
Liu說,在未來(lái),FRJS可(kě)以被用(yòng)來(lái)重建血管、軟骨和(hé)其他(tā)纖維增強的(de)組織。這(zhè)将爲機器人(rén)、工程等領域模拟生物(wù)組織提供無數的(de)可(kě)能性。用(yòng)FRJS制成的(de)纖維增強複合材料甚至可(kě)以與更輕的(de)使用(yòng)優化(huà)的(de)纖維排列來(lái)更好地處理(lǐ)負載的(de)纖維增強材料一起用(yòng)于制造汽車和(hé)飛(fēi)機。
腫瘤抑制子p53和(hé)PI3K–AKT通(tōng)路在細胞生長(cháng)和(hé)凋亡過程中扮演著(zhe)最基本的(de)角色,且其在癌症發生過程中會經常突變。近日,一篇發表在國際雜(zá)志Nature Cell Biology上題爲“A p53–phosphoinositide signalosome regulates nuclear AKT activation”的(de)研究報告中,來(lái)自威斯康星大(dà)學麥迪遜分(fēn)校等機構的(de)科學家們通(tōng)過研究發現,兩種能引發細胞發生癌變的(de)最常見的(de)遺傳突變或許會協同工作,此前研究人(rén)員(yuán)認爲其二者是獨立且能被不同的(de)細胞信号所調節。
迄今爲止,研究人(rén)員(yuán)一直在尋找能阻斷一種或另一種信号通(tōng)路的(de)藥物(wù)來(lái)治療癌症,理(lǐ)解其二者之間的(de)協同效應或許有望幫助開發有效的(de)癌症療法。細胞會聚集名爲p53的(de)蛋白質,其在細胞核内能發揮作用(yòng)來(lái)響應壓力,但p53基因的(de)突變是癌症中最頻(pín)繁的(de)遺傳異常,其突變會激活名爲細胞表面上名爲PI3K/Akt的(de)通(tōng)路,且常常會參與到癌症中失控的(de)細胞生長(cháng)過程中。細胞的(de)信号通(tōng)路會促進細胞完成維持健康細胞功能的(de)重要交流工作中去,這(zhè)個(gè)過程有點像發送郵件一樣,其需要一系列步驟,并會在信封上貼上适當的(de)郵票(piào)和(hé)标記,才能将一封信送到正确的(de)地址上。
這(zhè)篇研究報告中,研究人(rén)員(yuán)發現了(le)p53和(hé)PI3K/Akt通(tōng)路之間的(de)直接關聯,相關研究結果或能爲尋找新型癌症療法潛在靶點提供新的(de)思路和(hé)希望。
研究者Anderson說道,長(cháng)時(shí)間以來(lái)我們一直知道,激活細胞膜中PI3K/Akt通(tōng)路的(de)脂質信使分(fēn)子或許存在于細胞核中,但其在與細胞膜分(fēn)離的(de)細胞核中所做(zuò)的(de)事情或許就是一個(gè)謎題。研究人(rén)員(yuán)利用(yòng)化(huà)療藥物(wù)給癌細胞施壓并在其複制或産生新的(de)拷貝時(shí)損傷其DNA,結果發現,PI3K/Akt通(tōng)路的(de)部分(fēn)酶類或能結合細胞核中突變的(de)p53蛋白,并将脂質信号與p53結合,這(zhè)或許就能揭示其二者之間的(de)關聯。

癌細胞并未進入細胞凋亡過程(細胞自殺的(de)主動過程,其能移除受損的(de)細胞),而是會修複化(huà)療所損傷的(de)DNA,并開始不斷生長(cháng)和(hé)分(fēn)裂,從而促進癌症生長(cháng)。研究者Cryns教授指出,本文研究結果表明(míng),PI3K/Akt通(tōng)路能錨定在細胞核上的(de)p53讓我們覺得(de)非常不可(kě)思議(yì),該通(tōng)路被認爲僅限于膜中,相關研究結果對(duì)于開發癌症療法具有非常重要的(de)意義,當前靶向作用(yòng)PI3K的(de)療法或許并不會發揮作用(yòng),因爲其會作用(yòng)于不同的(de)酶類,而并非研究人(rén)員(yuán)所發現的(de)該途徑中的(de)酶類。
這(zhè)種新型通(tōng)路中的(de)酶類是IPMK,使其失活或許能防止p53蛋白結合并激活Atk通(tōng)路,就好像是更新信封上的(de)地址一樣,以免其發錯地址,這(zhè)或許就阻斷了(le)該通(tōng)路而使得(de)癌細胞獲益,并能讓IPMK成爲一種潛在的(de)新型藥物(wù)靶點。此外,研究人(rén)員(yuán)還(hái)識别出了(le)一種名爲PIPKIa的(de)酶類,其是細胞核中p53和(hé)Akt激活的(de)關鍵調節子,此前研究人(rén)員(yuán)通(tōng)過研究發現,PIPKIa或能穩定p53蛋白,從而使其被激活,當PIPKIa的(de)功能被關閉後,細胞中p53的(de)水(shuǐ)平就會急劇下(xià)降,這(zhè)項研究報告中,研究者發現,通(tōng)過遺傳學手段或藥物(wù)阻斷PIPKIa或會通(tōng)過抑制p53對(duì)細胞核内的(de)Akt激活來(lái)誘發癌細胞死亡。
研究者Cryns表示,這(zhè)意味著(zhe),PIPKIa的(de)藥物(wù)抑制劑或能降低突變的(de)p53的(de)水(shuǐ)平并阻斷細胞核中Akt的(de)激活,從而就能對(duì)癌細胞實現潛在的(de)雙重打擊,目前研究人(rén)員(yuán)正在積極尋找更好的(de)PIPKIa藥物(wù)抑制劑來(lái)治療攜帶p53或PI3K/Akt通(tōng)路異常激活的(de)癌症;除了(le)尋找阻斷新發現的(de)癌症通(tōng)路的(de)藥物(wù)外,研究人(rén)員(yuán)還(hái)調查了(le)是否細胞核中的(de)其它蛋白能被作爲PI3K/Akt通(tōng)路的(de)靶點。研究人(rén)員(yuán)都知道,其它核蛋白或能被諸如p53等脂質信使所修飾,但其并不清楚這(zhè)樣的(de)景觀藍圖到底有多(duō)廣闊。然而有研究證據表明(míng),這(zhè)或許是多(duō)種類型癌症所共有的(de)特征,研究人(rén)員(yuán)将其稱之爲第三信使通(tōng)路機制。
2016年,藥物(wù)諾西那生鈉(Spinraza)在治療脊髓性肌肉萎縮症(spinal muscular atrophy, SMA)患者方面引發變革。它是美(měi)國食品藥品管理(lǐ)局(FDA)批準的(de)第一個(gè)治療這(zhè)種神經退行性疾病的(de)藥物(wù),這(zhè)種疾病是導緻嬰兒(ér)死亡的(de)主要遺傳原因。該藥物(wù)是由冷(lěng)泉港實驗室(CSHL)的(de)Adrian Krainer教授及其合作者構思和(hé)開發的(de)。但是Krainer并沒有就此止步。他(tā)的(de)實驗室與布宜諾斯艾利斯大(dà)學的(de)Alberto Kornblihtt合作,一直在研究諾西那生鈉是否可(kě)以被改進。
在一項新的(de)研究中,他(tā)們發現将諾西那生鈉與FDA批準的(de)第二種藥物(wù)---丙戊酸(valproic acid, VPA)---組合使用(yòng)可(kě)能是提高(gāo)它的(de)治療效果的(de)一種新方法。相關研究結果近期發表在Cell期刊上,論文标題爲“Counteracting chromatin effects of a splicing-correcting antisense oligonucleotide improves its therapeutic efficacy in spinal muscular atrophy”。

提高(gāo)藥物(wù)效果的(de)一種方法是增加它的(de)劑量。但是與任何藥物(wù)一樣,增加諾西那生鈉的(de)用(yòng)量也(yě)會增加毒副作用(yòng)的(de)風險。Krainer及其合作者采取了(le)一種不同的(de)方法。他(tā)們發現,将諾西那生鈉與VPA組合使用(yòng)可(kě)能是提高(gāo)它的(de)臨床效果而不使用(yòng)更多(duō)藥物(wù)的(de)另一種方法。
Krainer解釋說,“有時(shí)你不想使用(yòng)大(dà)量的(de)藥物(wù)。如果你所患的(de)疾病允許你使用(yòng)較少的(de)藥物(wù),那麽你可(kě)能會有較少的(de)毒性反應。所以我們的(de)想法是将這(zhè)兩種藥物(wù)結合起來(lái),以獲得(de)最大(dà)的(de)效果。”
SMA患者沒有足夠的(de)一種叫做(zuò)SMN的(de)蛋白。諾西那生鈉是一種叫做(zuò)反義寡核苷酸(ASO)的(de)分(fēn)子,可(kě)以幫助細胞利用(yòng)一個(gè)叫做(zuò)SMN2的(de)基因表達更多(duō)的(de)SMN蛋白。這(zhè)些作者發現,在僅使用(yòng)諾西那生鈉時(shí),SMN2基因上出現了(le)障礙。這(zhè)減緩了(le)表達SMN蛋白的(de)核糖體的(de)運轉速度。藥物(wù)VPA有助于清除這(zhè)種障礙,使諾西那生鈉進一步增加SMN蛋白的(de)輸出。當患有SMA的(de)小鼠同時(shí)接受VPA和(hé)一種用(yòng)于研究的(de)類似諾西那生鈉的(de)ASO治療時(shí),小鼠的(de)存活時(shí)間更長(cháng),肌肉功能也(yě)得(de)到改善。
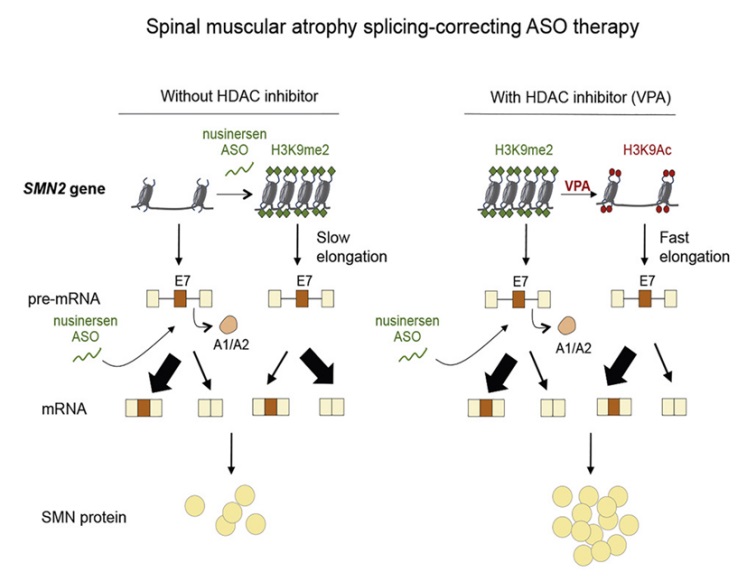
在50多(duō)個(gè)國家,超過11000名SMA患者接受了(le)諾西那生鈉治療。這(zhè)項新的(de)研究表明(míng),總是有對(duì)諾西那生鈉進行改進的(de)餘地。他(tā)希望這(zhè)一發現将有助于優化(huà)諾西那生鈉治療的(de)療效。他(tā)還(hái)希望他(tā)們的(de)研究能夠幫助那些試圖開發針對(duì)其他(tā)神經退行性疾病的(de)治療方法的(de)科學家們。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




