在一項新的(de)研究中,來(lái)自美(měi)國加州大(dà)學洛杉矶分(fēn)校和(hé)加州大(dà)學舊(jiù)金山分(fēn)校的(de)研究人(rén)員(yuán)通(tōng)過使用(yòng)允許組合使用(yòng)在一種實驗中大(dà)規模篩選基因變異的(de)新測試方法,确定了(le)阿爾茨海默病和(hé)一種罕見的(de)相關大(dà)腦(nǎo)疾病---進行性核上性麻痹(progressive supranuclear palsy, PSP)---的(de)多(duō)個(gè)新風險基因。相關研究結果發表在2022年8月(yuè)19日的(de)Science期刊上,論文标題爲“Functional regulatory variants implicate distinct transcriptional networks in dementia”。

這(zhè)項新的(de)研究還(hái)提出了(le)一種修訂後的(de)新模型,顯示常見的(de)基因變異雖然單獨對(duì)疾病的(de)影(yǐng)響很小,但一起可(kě)能通(tōng)過破壞整個(gè)基因組的(de)特定轉錄程序而提高(gāo)疾病的(de)風險。
通(tōng)常情況下(xià),科學家們憑借全基因組關聯研究(GWAS)調查一大(dà)群人(rén)的(de)基因組,以确定增加疾病風險的(de)基因變異。這(zhè)是通(tōng)過測試與疾病相關的(de)染色體或基因座上的(de)标記來(lái)完成的(de)。每個(gè)基因座平均有幾十個(gè)---有時(shí)是幾百個(gè)或幾千個(gè)---共同的(de)遺傳标記,這(zhè)些标記是共同遺傳的(de),與疾病有關,這(zhè)就使得(de)人(rén)們很難确定哪些是真正導緻疾病的(de)功能性變異。
确定因果變異及其影(yǐng)響的(de)基因是現代遺傳學和(hé)生物(wù)醫學的(de)一個(gè)主要挑戰。這(zhè)項新的(de)研究爲解決這(zhè)一問題提供了(le)一個(gè)有效的(de)路線圖。
在這(zhè)項新的(de)研究中,這(zhè)些作者進行了(le)已知最早用(yòng)來(lái)研究神經退行性疾病的(de)高(gāo)通(tōng)量測試方法之一。他(tā)們進行了(le)大(dà)規模并行報告基因檢測(massively parallel reporter assay, MPRA),同時(shí)測試了(le)與阿爾茨海默病相關的(de)25個(gè)位點和(hé)與PSP相關的(de)9個(gè)位點的(de)5706個(gè)基因變異。PSP是一種比阿爾茨海默病更罕見的(de)神經系統疾病,但有類似的(de)病理(lǐ)特征。
從這(zhè)種測試中,這(zhè)些作者以很高(gāo)的(de)信心确定了(le)320個(gè)功能性的(de)基因變異。爲了(le)驗證這(zhè)一結果,他(tā)們在多(duō)種細胞類型中對(duì)這(zhè)些高(gāo)可(kě)信的(de)基因變異中的(de)42個(gè)進行了(le)彙集CRISPR篩選(pooled CRISPR screen)。
論文通(tōng)訊作者、加州大(dà)學洛杉矶分(fēn)校人(rén)類遺傳學、神經學和(hé)精神病學教授Daniel H. Geschwind博士說,“我們結合了(le)多(duō)項先進技術,使我們能夠進行高(gāo)通(tōng)量的(de)生物(wù)學實驗,我們不是一次做(zuò)一個(gè)實驗,而是以一種彙集的(de)形式并行做(zuò)數千個(gè)實驗。這(zhè)使我們能夠應對(duì)這(zhè)一挑戰,即如何從與一種疾病相關的(de)數千個(gè)基因變異中确定哪些基因變異是功能性的(de)以及它們影(yǐng)響哪些基因。”
他(tā)們的(de)數據提供了(le)證據表明(míng)可(kě)能存在幾個(gè)新的(de)阿爾茨海默病風險基因,包括C4A、PVRL2和(hé)APOC1,以及其他(tā)新的(de)PSP風險基因(PLEKHM1和(hé)KANSL1)。他(tā)們還(hái)能夠驗證幾個(gè)以前确定的(de)風險基因位點。Geschwind說,下(xià)一步将是研究這(zhè)些新發現的(de)風險基因如何在細胞和(hé)模型系統中相互作用(yòng)。
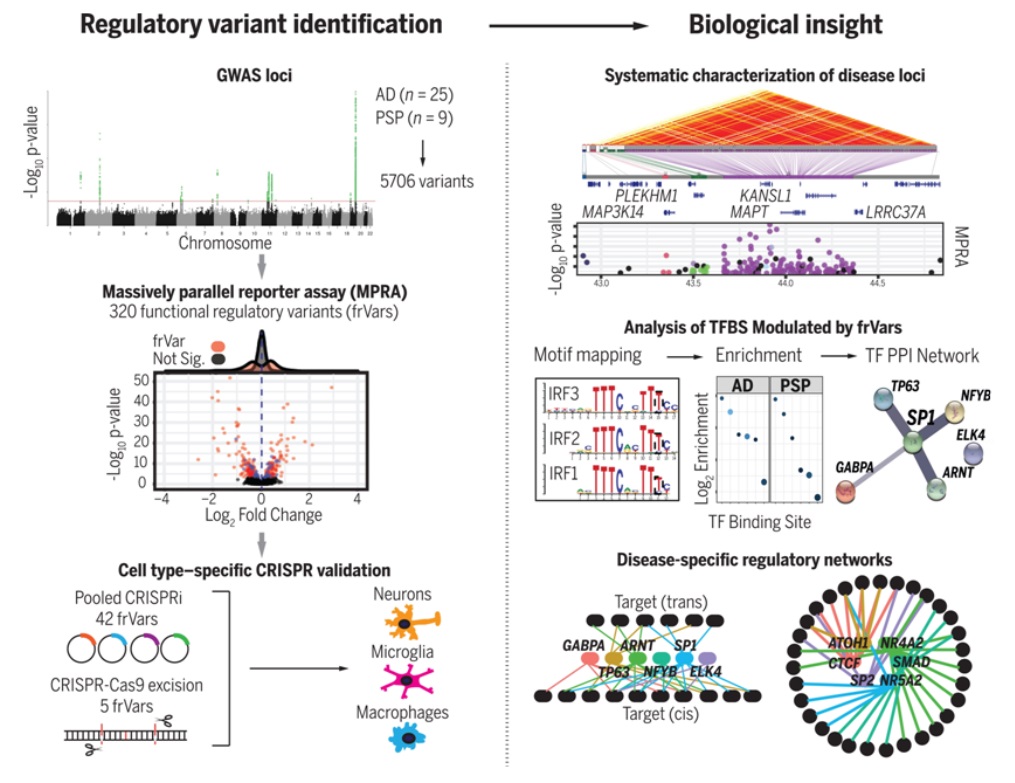
圖爲 大(dà)規模并行的(de)功能基因組學确定了(le)癡呆症中的(de)基因和(hé)機制
Geschwind說,這(zhè)項新的(de)研究提供了(le)原則性的(de)證明(míng),即高(gāo)通(tōng)量測試可(kě)以爲進一步的(de)研究提供一個(gè)“非常有效”的(de)路線圖,但他(tā)強調,這(zhè)些方法必須深思熟慮地與更有針對(duì)性的(de)實驗相搭配,就像在這(zhè)項新的(de)研究中那樣。他(tā)說,“這(zhè)一成功并不意味著(zhe)我們可(kě)以放棄在模型系統中研究單個(gè)基因的(de)那種詳細、謹慎的(de)實驗。這(zhè)隻是全基因組關聯研究和(hé)理(lǐ)解疾病機制之間的(de)關鍵一步。”
論文第一作者Yonatan Cooper說,這(zhè)些作者對(duì)多(duō)種方法的(de)組合使用(yòng)使他(tā)們對(duì)自己的(de)發現更有信心,同時(shí)它也(yě)突出了(le)解釋人(rén)類基因變異所面臨的(de)内在挑戰。Cooper說,“我們相信,多(duō)種方法的(de)組合使用(yòng)對(duì)于未來(lái)在研究和(hé)臨床領域注釋疾病相關變異的(de)工作至關重要。”
這(zhè)些作者還(hái)能夠在PSP中揭示了(le)至少一種機制,即與該疾病相關的(de)多(duō)個(gè)基因座協同破壞了(le)一組核心的(de)轉錄因子。Geschwind說,這(zhè)表明(míng)位于整個(gè)基因組的(de)共同基因變異正在影(yǐng)響特定細胞類型中的(de)特定調節網絡。他(tā)說,這(zhè)一發現确定了(le)新的(de)潛在藥物(wù)靶标,并表明(míng)靶向一個(gè)基因網絡而不是靶向一個(gè)基因可(kě)能是一種有效的(de)方法。
Geschwind說,“我們正在進入一個(gè)新的(de)治療階段---開始有理(lǐ)由考慮靶向整個(gè)基因網絡。”
在一項新的(de)研究中,來(lái)自法國國家科學研究中心、居裏研究所、索邦大(dà)學和(hé)美(měi)國麻省理(lǐ)工學院的(de)研究人(rén)員(yuán)首次能夠物(wù)理(lǐ)作用(yòng)于活細胞中的(de)染色體。通(tōng)過使用(yòng)磁鐵使染色體受到不同的(de)力,他(tā)們發現染色體實際上在細胞分(fēn)裂階段之外是非常流動的(de),幾乎是液态的(de)。這(zhè)一發現是由于首次對(duì)活細胞核中的(de)染色體進行了(le)直接的(de)機械操
作而實現的(de)。相關研究結果發表在2022年7月(yuè)29日的(de)Science期刊上,論文标題爲“Live-cell micromanipulation of a genomic locus reveals interphase chromatin mechanics”。

在此之前,染色體---它們是非常長(cháng)的(de)DNA分(fēn)子--被認爲是像松散的(de)毛線球一樣糾纏在一起,并形成一種凝膠。這(zhè)項新研究中報告的(de)觀察結果提供了(le)一個(gè)非常不同的(de)形象。染色體是流動的(de),能夠自由移動,不受構成細胞核的(de)其他(tā)成分(fēn)的(de)限制,并且能夠自我重組。
爲了(le)得(de)出這(zhè)些結論,這(zhè)些作者将磁性納米顆粒附著(zhe)在活細胞中染色體的(de)一小部分(fēn)上。然後,借助于細胞外的(de)微型磁鐵,他(tā)們拉伸染色體,施加不同程度的(de)力。利用(yòng)這(zhè)種方法,他(tā)們首次在活細胞中成功地測量了(le)染色體對(duì)外部力的(de)反應。
通(tōng)過這(zhè)些實驗,這(zhè)些作者能夠看到,在細胞核中天然施加的(de)力的(de)範圍---例如由複制DNA的(de)酶施加的(de)力---足以大(dà)大(dà)改變染色體的(de)構象。在物(wù)理(lǐ)學和(hé)生物(wù)學之間的(de)這(zhè)一重大(dà)發現,改變了(le)迄今爲止已建立的(de)染色體表述。它也(yě)爲我們理(lǐ)解生物(wù)過程、染色體的(de)生物(wù)物(wù)理(lǐ)學和(hé)基因組的(de)組裝增加了(le)新的(de)内容。
在受損的(de)肌肉中,肌肉幹細胞必須與免疫細胞一起工作以完成修複過程,然而這(zhè)些細胞如何協調以确保在制造新的(de)肌纖維之前有效地清除死亡組織,仍然是未知數。在一項新的(de)研究中,來(lái)自加拿大(dà)渥太華大(dà)學等研究機構的(de)研究人(rén)員(yuán)揭示了(le)控制肌肉修複的(de)一種獨特的(de)細胞通(tōng)信形式。他(tā)們發現,一種用(yòng)于化(huà)妝品和(hé)骨關節炎注射的(de)叫做(zuò)透明(míng)質酸(hyaluronic acid)的(de)天然物(wù)質是控制這(zhè)種基本相互作用(yòng)的(de)關鍵分(fēn)子。相關研究結果發表在2022年8月(yuè)5日的(de)Science期刊上,論文标題爲“JMJD3 activated hyaluronan synthesis drives muscle regeneration in an inflammatory environment”。

論文通(tōng)訊作者、渥太華大(dà)學教授Jeffrey Dilworth博士說,“當肌肉受損時(shí),免疫細胞迅速進入這(zhè)種組織并在肌肉幹細胞開始修複之前清除損傷是非常重要的(de)。我們的(de)研究顯示,肌肉幹細胞已準備好立即開始修複,但免疫細胞将這(zhè)些幹細胞維持在靜止狀态,同時(shí)完成清理(lǐ)工作。大(dà)約40小時(shí)後,一旦清理(lǐ)工作完成,肌肉幹細胞的(de)内部警報就會響起,使它們能夠醒來(lái)并開始修複。”
Dilworth博士及其研究團隊确定透明(míng)質酸是這(zhè)個(gè)内部警報的(de)關鍵成分(fēn),它告訴肌肉幹細胞何時(shí)醒來(lái)。當肌肉損傷發生時(shí),肌肉幹細胞開始産生并給自己塗上透明(míng)質酸。一旦這(zhè)種塗層變得(de)足夠厚,它就會阻止免疫細胞的(de)休眠信号,并導緻肌肉幹細胞醒來(lái)。
Dilworth團隊利用(yòng)小鼠和(hé)人(rén)體組織,還(hái)發現了(le)肌肉幹細胞如何利用(yòng)Has2基因上的(de)表觀遺傳标志控制透明(míng)質酸的(de)産生。具體而言,他(tā)們确定了(le)表觀遺傳酶KDM6B/JMJD3在肌肉修複過程中建立肌肉幹細胞和(hé)浸潤免疫細胞之間通(tōng)信的(de)重要作用(yòng)。他(tā)們發現,在應對(duì)肌肉損傷時(shí),KDM6B/JMJD3去除轉錄抑制性組蛋白修飾H3K27me3,使肌肉幹細胞産生透明(míng)質酸,然後所産生的(de)透明(míng)質酸被整合到肌肉幹細胞的(de)胞外基質中。胞外基質的(de)這(zhè)種重塑使肌肉幹細胞能夠接受來(lái)自浸潤免疫細胞的(de)信号,從而啓動肌肉再生。
論文第一作者、Dilworth博士的(de)研究助理(lǐ)Kiran Nakka博士說,“有趣的(de)是,衰老與慢(màn)性炎症、肌肉無力以及肌肉幹細胞喚醒和(hé)修複損傷的(de)能力降低有關。如果我們能找到一種方法來(lái)增強老年人(rén)肌肉幹細胞中的(de)透明(míng)質酸産生,它可(kě)能有助于肌肉修複。”
這(zhè)些作者指出,透明(míng)質酸的(de)這(zhè)種再生效果似乎取決于它是否由肌肉幹細胞産生。該團隊目前正在研究對(duì)肌肉幹細胞表觀遺傳學進行修飾的(de)藥物(wù)是否可(kě)以用(yòng)來(lái)增加它們的(de)透明(míng)質酸産生。
早期發育中的(de)基因突變與一些精神疾病有關,如自閉症和(hé)精神分(fēn)裂症,其症狀通(tōng)常在兒(ér)童和(hé)成年早期表現出來(lái)。然而,突變有兩種類型:一種是遺傳性的(de),另一種是受精後自發發生或由環境誘發的(de),并可(kě)能持續一生。
在一項新的(de)研究中,來(lái)自美(měi)國耶魯大(dà)學、梅約診所約和(hé)翰霍普金斯大(dà)學醫學院的(de)研究人(rén)員(yuán)在研究冷(lěng)凍的(de)死後人(rén)類大(dà)腦(nǎo)中的(de)那些非遺傳性突變(也(yě)稱爲體細胞突變)時(shí)發現,大(dà)約6%的(de)大(dà)腦(nǎo)更有可(kě)能積累大(dà)量的(de)這(zhè)些突變,而且這(zhè)些“高(gāo)突變(hypermutation)”的(de)大(dà)腦(nǎo)往往是40歲或以上的(de)人(rén)。相關研究結果發表在2022年7月(yuè)29日的(de)Science期刊上,論文标題爲“Analysis of somatic mutations in 131 human brains reveals aging-associated hypermutability”。

這(zhè)些作者将這(zhè)一現象歸因于具有突變的(de)細胞系超過了(le)其他(tā)細胞系,類似于骨髓中的(de)可(kě)導緻老年人(rén)患上血癌的(de)克隆性造血。
論文共同通(tōng)訊作者、耶魯大(dà)學兒(ér)童研究中心神經科學教授Flora Vaccarino說,“這(zhè)是第一次大(dà)規模研究人(rén)類大(dà)腦(nǎo)的(de)體細胞突變,我們沒有想到會在老年人(rén)群中發現這(zhè)種高(gāo)突變性。”
在這(zhè)項新的(de)研究中,這(zhè)些作者在131個(gè)人(rén)類大(dà)腦(nǎo)中尋找體細胞突變,其中44個(gè)來(lái)自沒有已知疾病的(de)受試者,19個(gè)患有多(duō)發性抽動綜合征(Tourette syndrome),9個(gè)患有精神分(fēn)裂症,59個(gè)患有自閉症。雖然大(dà)多(duō)數大(dà)腦(nǎo)有20至60個(gè)非遺傳性突變,但大(dà)約6%的(de)大(dà)腦(nǎo)有數百個(gè)突變;這(zhè)些高(gāo)突變的(de)大(dà)腦(nǎo)大(dà)多(duō)來(lái)自60歲或以上的(de)人(rén)。在60歲或以上的(de)人(rén)的(de)大(dà)腦(nǎo)中,高(gāo)突變的(de)大(dà)腦(nǎo)占16%,而在40歲以下(xià)的(de)人(rén)的(de)大(dà)腦(nǎo)中隻有2%。這(zhè)些高(gāo)突變與任何疾病都沒有關系。
然而,老年大(dà)腦(nǎo)中高(gāo)突變數量的(de)增加使科學家們推測,大(dà)量的(de)突變可(kě)能與阿爾茨海默病和(hé)/或腦(nǎo)癌有關。
對(duì)自閉症供者的(de)大(dà)腦(nǎo)進行的(de)仔細檢查顯示,體細胞突變與大(dà)面積DNA的(de)缺失以及轉錄因子與DNA調控元件結合和(hé)調節基因活性的(de)能力的(de)破壞有關。
這(zhè)些作者還(hái)強調,盡管在這(zhè)項研究中沒有發現體細胞突變與精神分(fēn)裂症和(hé)多(duō)發性抽動綜合征之間的(de)聯系,但需要更多(duō)的(de)研究來(lái)排除它們在這(zhè)些疾病産生中的(de)作用(yòng)。
在一項新的(de)研究中,來(lái)自美(měi)國耶魯大(dà)學的(de)研究人(rén)員(yuán)開發了(le)一種替莫唑胺(temozolomide, TMZ)類似物(wù),作爲治療膠質瘤的(de)化(huà)療藥物(wù)使用(yòng)。相關研究結果發表在2022年7月(yuè)29日的(de)Science期刊上,論文标題爲“Mechanism-based design of agents that selectively target drug-resistant glioma”。

在這(zhè)篇論文中,這(zhè)些作者描述了(le)這(zhè)種TMZ類似物(wù)以及它是如何殺死腦(nǎo)瘤細胞的(de)。澳大(dà)利亞悉尼大(dà)學兒(ér)童醫學研究所的(de)Roger Reddel和(hé)Adel Aref在同期Science期刊上發表了(le)一篇标題爲“Targeting brain cancer”的(de)觀點類型文章(zhāng),概述了(le)這(zhè)些作者所進行的(de)研究工作。
膠質母細胞瘤(GBM)是人(rén)類最常見的(de)腦(nǎo)瘤類型,也(yě)是最緻命的(de),隻有5%的(de)患者在診斷後能活五年。對(duì)GBM患者的(de)治療包括放射治療和(hé)化(huà)療藥物(wù)替莫唑胺(TMZ)。這(zhè)些治療通(tōng)常是爲了(le)延長(cháng)生命,而不是拯救生命。在這(zhè)項新的(de)研究中,他(tā)們開發出一種TMZ類似物(wù),迄今已被證明(míng)比TMZ更有效地殺死GBM細胞。
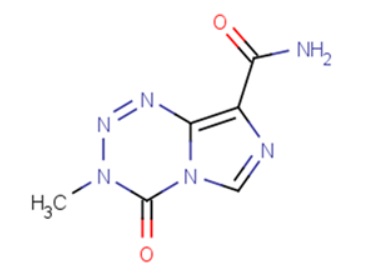
圖爲 替莫唑胺化(huà)學結構式
這(zhè)些作者指出,TMZ的(de)作用(yòng)是利用(yòng)GBM的(de)一個(gè)弱點---GBM細胞缺乏O6-甲基鳥嘌呤甲基轉移酶(O6-methylguanine methyl transferase, MGMT),即一種修複DNA的(de)蛋白。用(yòng)TMZ治療會導緻DNA損傷的(de)發生,從而導緻癌細胞自我毀滅---癌細胞死亡,而健康的(de)腦(nǎo)細胞則通(tōng)過自我愈合而存活。不幸的(de)是,患者往往會對(duì)這(zhè)種藥物(wù)産生抗藥性,從而降低其有效性,直到它不再有用(yòng)。在這(zhè)項新的(de)研究中,他(tā)們開發出一種TMZ類似物(wù),它也(yě)會導緻DNA損傷和(hé)癌細胞自我毀滅,但他(tā)們做(zuò)了(le)一個(gè)改變,防止腫瘤細胞對(duì)它産生抗性。
這(zhè)些作者進行的(de)改變涉及添加一種鏈間交聯劑,顧名思義,它涉及在DNA鏈之間建立連接,但它是以一種允許健康細胞逆轉這(zhè)一過程的(de)方式進行的(de)。另一方面,在癌細胞中,這(zhè)種連接對(duì)于GBM細胞來(lái)說太強了(le),無法克服,因此它們最終會自我毀滅--至少在小鼠模型中是這(zhè)樣。他(tā)們認爲,最終的(de)結果是一種将不允許在DNA錯配修複途徑中出現突變的(de)TMZ類似物(wù),這(zhè)意味著(zhe)GBM細胞應該沒有辦法産生抗藥性。
文章(zhāng)轉載自生物(wù)谷,系出于傳遞更多(duō)信息之目的(de),轉載内容不代表本站立場(chǎng)。如有侵權請及時(shí)聯系,我們将立即進行删除處理(lǐ)。




 京公網安備 11011402010692号
京公網安備 11011402010692号




